-
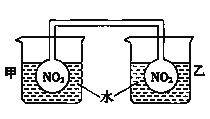
可逆反应2NO2 (g) ⇌N2O4 (g) ΔH= −56.9 kJ·mol−1在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。某同学的部分实验报告如下。
| 
| 1.向左侧烧杯中加入NH4NO3晶体,甲瓶的红棕色变浅。 2.向右侧烧杯中加入CaO固体,乙瓶的红棕色变深。 |
下列说法不正确的是
A.甲瓶的红棕色变浅,说明平衡2NO2 (g)⇌N2O4 (g)向正反应方向移动
B.可根据现象判断NH4NO3晶体溶于水吸热,CaO固体溶于水放热
C.甲瓶中反应的化学平衡常数(K)增大
D.乙瓶中由于反应的化学平衡常数(K)改变,使Qc<K,平衡发生移动
-
下列关于反应能量的说法正确的是( )
A.由2NO2(g) N2O4(g) △H=-56.9 kJ/mol,可知将2mol NO2(g)置于密闭容器中充分反应后放出热量为56.9kJ
N2O4(g) △H=-56.9 kJ/mol,可知将2mol NO2(g)置于密闭容器中充分反应后放出热量为56.9kJ
B.101 kPa时2H2(g)+O2(g)==2H2O(l) ΔH=-572 kJ·mol-1,H2的燃烧热为-572 kJ·mol-1
C.同温同压下,H2 (g)+Cl2(g)== 2HCl(g)在光照和点燃条件下的△H相同
D.H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,含1 molNaOH的氢氧化钠溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ的热量
-
下列装置或操作不能达到目的的是

A.装置①用于滴定中和热装置
B.装置②依据褪色快慢比较浓度对反应速率的影响
C.③依据两容器内气体颜色变化,判断反应2NO2(g) N2O4(g)平衡移动的方向
N2O4(g)平衡移动的方向
D.装置④依据U管两边液面的高低判断Na和水反应的热效应
-
可逆反应
 在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
(1)甲烧杯中 球的红棕色变浅,说明平衡
球的红棕色变浅,说明平衡 向______________(填“正反应”或“逆反应”)方向移动,所以
向______________(填“正反应”或“逆反应”)方向移动,所以 晶体溶于水是__________________(填“放热”或“吸热”)过程。
晶体溶于水是__________________(填“放热”或“吸热”)过程。
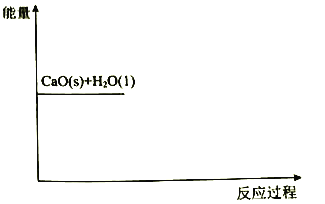
(2)根据乙烧杯中的现象,补全 与
与 反应过程的能量变化示意图_____。
反应过程的能量变化示意图_____。
-
反应N2O4(g)⇌2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示.下列说法错误的是( )

A.A、B、C三点中气体颜色最深的为C点
B.维持压强不变,由B点到A点反应向正方向进行
C.A、C两点的反应速率:A>C
D.B、C两点化学平衡常数:B<C
-
反应2NO2(g)  N2O4(g) ΔH=-57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的为( )
N2O4(g) ΔH=-57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的为( )
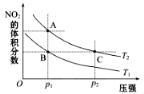
A. A、C两点气体的颜色:A深,C浅
B. A、C两点的反应速率:A>C
C. A、C两点气体的平均相对分子质量:A>C
D. 由状态A到状态B,可以采用降温的方法
-
反应N2O4(g) 2NO2(g) ΔH= +57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法错误的是
2NO2(g) ΔH= +57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法错误的是

A.A、B、C三点中气体 颜色最深的为C点
B.维持压强不变,由B点到A点反应向正方向进行
C.A、C两点的反应速率:A>C
D.B、C两点化学平衡常数:B<C
-
下列有关热化学方程式的叙述,正确的是( )
A.反应物的总能量低于生成物的总能量时,该反应必须加热才能发生
B.由N2O4(g)⇌2NO2(g) ΔH=+56.9kJ·mol-1,可知将1molN2O4(g)置于密闭容器中充分反应后吸收的热量为56.9kJ
C.由:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,可知含1molHCN的稀溶液与含1molNaOH的稀溶液混合,放出热量为57.3kJ
D.已知101kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221kJ·mol-1,则1mol碳完全燃烧放出的热量大于110.5kJ
-
下列说法正确的是
A. 对于2NO2(g) N2O4(g)的平衡体系,压缩体积,增大压强,平衡正向移动,混合气体的颜色变浅
N2O4(g)的平衡体系,压缩体积,增大压强,平衡正向移动,混合气体的颜色变浅
B. 化学平衡正向移动,反应物的转化率一定增大
C. 往平衡体系FeCl3+3KSCN Fe(SCN)3+3KCl中加入适量KCl固体,平衡逆向移动,溶液的颜色变浅
Fe(SCN)3+3KCl中加入适量KCl固体,平衡逆向移动,溶液的颜色变浅
D. C(s)+CO2(g) 2CO(g) ΔH>0,其他条件不变时,升高温度,反应速率v(CO2)和CO2的平衡转化率均增大
2CO(g) ΔH>0,其他条件不变时,升高温度,反应速率v(CO2)和CO2的平衡转化率均增大
-
对于反应2NO2(g)  N2O4(g) ΔH<0,达到平衡后缩小容器体积,下列说法正确的是
N2O4(g) ΔH<0,达到平衡后缩小容器体积,下列说法正确的是
A.平衡逆向移动 B.混合气体颜色比原来深
C.混合气体颜色比原来浅 D.混合气体的平均相对分子质量变小