-
根据题意解答
(1)某实验小组同学进行如下实验,以检验化学反应中的能量变化,据实验现象判断①是_________热反应,②是_________热反应.反应过程___(填“①”或“②”)的能量变化可用图2表示.
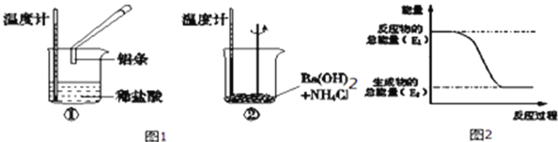
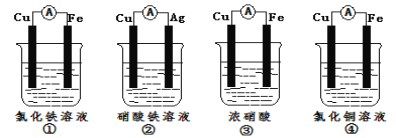
(2)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是_________(填序号).
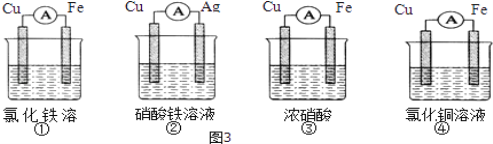
(3)将H2设计成燃料电池,其利用率更高,装置如图4所示(a、b为多孔碳棒),负极通入_______其电极反应式为________________电池总反应为______________
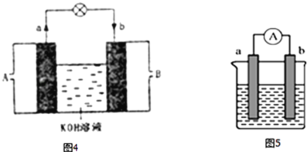

(4)如图5是某化学兴趣小组探究不同条件下化学能转变为电能的装置.
①若两个电极分别是锌、铜,电解质溶液是稀硫酸,正极的电极反应式___________;若电极保持不变,将电解质溶液换成硫酸铜,请将该电池设计为双液原电池画入图6中___________;
②当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠时,该原电池的负极为_______;该原电池的电池总反应为_____________________________.
③若电池的总反应是2FeCl3+Fe 3FeCl2,则可以作正极材料的是________,正极反应式是__________若该电池反应消耗了0.1mol FeCl3,则转移电子的数目为_____。
3FeCl2,则可以作正极材料的是________,正极反应式是__________若该电池反应消耗了0.1mol FeCl3,则转移电子的数目为_____。
-
某实验小组同学进行如下实验,以检验化学反应中的能量变化。
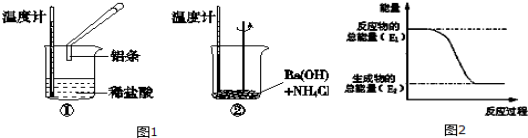
请回答下列问题:(1)实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是 热反应, Ba(OH)2•8H2O与NH4Cl的反应是 热反应.反应过程 (填“①”或“②”)的能量变化可用图2表示。
(2)现有如下两个反应:
(A)NaOH+HCl=NaCl+H2O (B)2FeCl3+Cu=2FeCl2+CuCl2
以上两个反应能设计成原电池的是 , 负极材料为:_______,电解质溶液为:__________,正极的电极反应式为:_________________;负极的电极反应式为:_________________。
-
某实验小组同学进行如下实验,以检验化学反应中的能量变化。请回答下列问题:
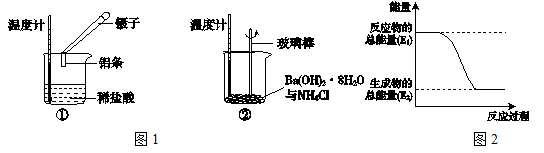
(1)实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是 热反应, Ba(OH)2•8H2O与NH4Cl的反应是 热反应.反应过程 (填“①”或“②”)的能量变化可用图2表示。
(2)现有如下两个反应:
(A)NaOH+HCl=NaCl+H2O (B)2FeCl3+Cu=2FeCl2+CuCl2
以上两个反应能设计成原电池的是 , 负极材料为:____ ___,电解质溶液为:_______ ___,负极的电极反应式为:_________________。
-
某实验小组同学进行如下实验,以检验化学反应中的能量变化。
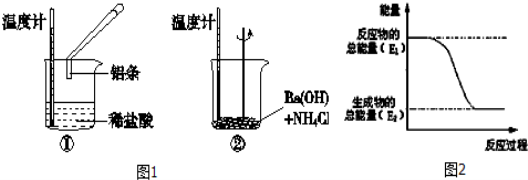
请回答下列问题:
(1)实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应
是 热反应, Ba(OH)2•8H2O与NH4Cl的反应是 热反应.反应过程 (填“①”或“②”)的能量变化可用图2表示。
(2)现有如下两个反应:
(A)NaOH+HCl=NaCl+H2O (B)2FeCl3+Cu=2FeCl2+CuCl2
以上两个反应能设计成原电池的是 , 负极材料为:_______,电解质溶液为:__________,正极的电极反应式为:_________________;负极的电极反应式为:_________________。
-
Ⅰ、某实验小组同学进行如下实验,以检验化学反应中的能量变化。请回答下列问题:
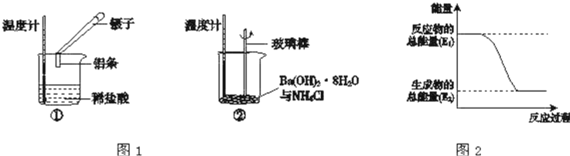
(1)实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是________,Ba(OH)2•8H2O与NH4Cl的反应是________.反应过程________(填“①”或“②”)的能量变化可用图2表示。
(2)现有如下两个反应:A、NaOH+HCl=NaCl+H2O;B、2FeCl3+Cu=2FeCl2+CuCl2,以上两个反应能设计成原电池的是________,负极材料为:________,电解质溶液为:________,负极的电极反应式为:________。
Ⅱ、某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。利用如图装置可验证同主族元素非金属性的变化规律

(1)仪器A的名称为________,干燥管D的作用为________。
(2)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液________(填现象)即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用NaOH溶液吸收尾气。
(3)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中可加________溶液,观察到C中溶液________(填现象),即可证明,反应的离子方程式为:________,但有的同学认为该实验不严谨,应在两装置间添加装有________溶液的洗气瓶,目的是________。
-
某实验小组同学进行如下实验,以检验化学反应中的能量变化。

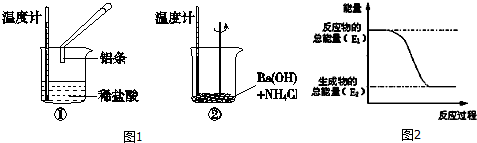
请回答下列问题:
(1)实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是 热反应,Ba(OH)2•8H2O与NH4Cl的反应是 热反应.反应过程 (填“①”或“②”)的能量变化可用图2表示.
(2)现有如下两个反应:(A)NaOH+HCl=NaCl+H2O (B)2FeCl3+Cu=2FeCl2+CuCl2
①以上两个反应能设计成原电池的是
②写出设计原电池正、负极电极反应式 、 .
-
(1)某实验小组同学进行如下实验,以检验化学反应中的能量变化,
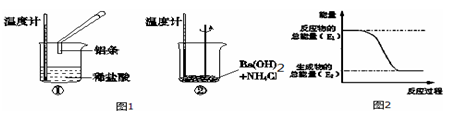
实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是 热反应,Ba(OH)2•8H2O与NH4Cl的反应是 热反应.反应过程 (填“①”或“②”)的能量变化可用图2表示。.
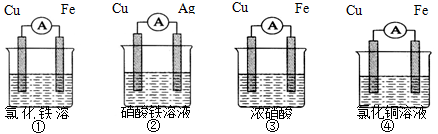
(2)为了验证Fe3 +与Cu2+氧化性强弱,下列装置能达到实验目的的是 (填序号)。
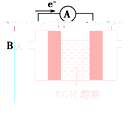
(3)将CH4设计成燃料电池,其利用率更高,装置如下左图所示(a、b为多孔碳棒)。____处电极入口通甲烷(填A或B),其电极反应式为 。

(4)如上右图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
①当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,写出该原电池正极的电极反应式为_____。
②当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该原电池的正极为 ;该原电池的负极反应式为_____________________________。
-
(1)某实验小组同学进行如下实验,以检验化学反应中的能量变化,
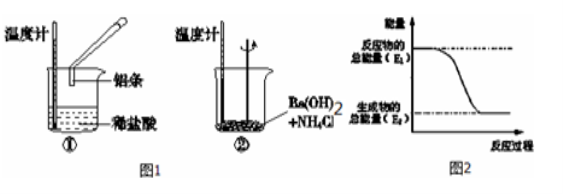
实验中发现,反应后①中的温度升高;②中的温度降低.
由此判断铝条与盐酸的反应是 热反应。
Ba(OH)2•8H2O与NH4Cl的反应是 热反应。
反应过程 (填“①”或“②”)的能量变化可用图2表示。.
(2)为了验证Fe3 +与Cu2+氧化性强弱,下列装置能达到实验目的的是 (填序号)。
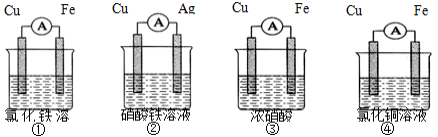
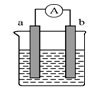
(3)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回 答下列问题:
当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,该原电池的正极为 。
-
某实验小组同学进行如下实验,以检验化学反应中的能量变化。
(1)实验中发现,反应后①中的温度升高;②中的温度降低。由此判断铝条与盐酸的反应是__热反应,Ba(OH)2•8H2O与NH4Cl反应时,需要将固体研细其目的是__,反应过程__(填“①”或“②”)的能量变化可用图表示。
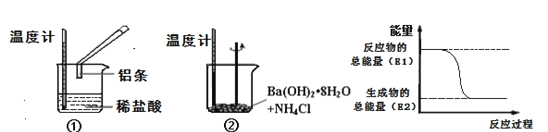
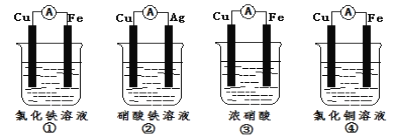
(2)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是__(填序号)。
-
某实验小组同学进行如下实验,以检验化学反应中的能量变化。
(1)实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是______热反应, Ba(OH)2•8H2O与NH4Cl反应时,需要将固体研细其目的是________________.反应过程______ (填“①”或“②”)的能量变化可用图表示。

(2)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是_________(填序号)。
(3)将CH4设计成燃料电池,其利用率更高,装置如图所示(a、b为多孔碳棒)其中____(填A或B)处电极入口通甲烷,其电极反应式为_____________________ 。当消耗标况下甲烷33.6L时,假设能量转化率为90%,则导线中转移电子的物质的量为_________mol。
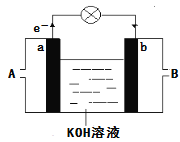
(4)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:

①当电极c为Al、电极d为Cu、电解质溶液为稀硫酸时,写出该原电池正极的电极反应式为_______________。
②当电极c为Al、电极d为Mg、电解质溶液为氢氧化钠溶液时,该原电池的正极为_______;该原电池的负极反应式为_____________________________。



3FeCl2,则可以作正极材料的是________,正极反应式是__________若该电池反应消耗了0.1mol FeCl3,则转移电子的数目为_____。

















