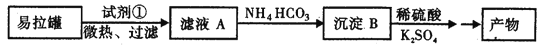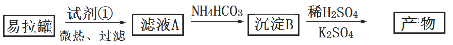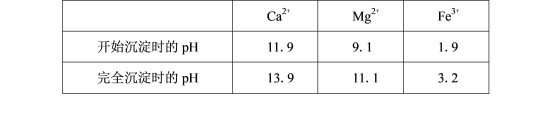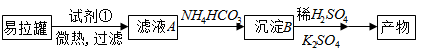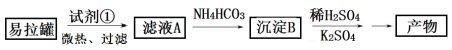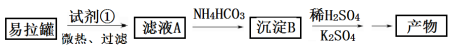-
KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐( 主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
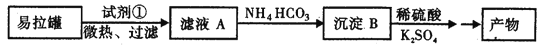
(1)请写出镓(与铝同主族的第四周期元素)的原子结构示意图_________。
(2)为尽量少引入杂质,试剂①应选用______(填标号)。理由是______________。
A.HCl溶液 B.H2SO4 溶液 C.氨水 D.NaOH溶液
(3)沉淀B的化学式为________;将少量明矾溶于水,溶液呈弱酸性,其原因是________(用离子方程式表示)。
(4)科学研究证明NaAlO2 在水溶液中实际上是Na[Al(OH)4](四羟基合铝酸钠),易拉罐溶解过程中主要反应的化学方程式为___________________。
(5)常温下,等pH的NaAlO2 和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍,则两种溶液的pH=__________。
(6)已知室温下,Kw=10×10-14,Al(OH)3 AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
-
KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。



回答下列问题:
(1)为尽量少引入杂质,试剂①应选用NaOH溶液,若选用H2SO4溶液,其后果是_________。
(2)易拉罐溶解过程中主要反应的化学方程式为_______________;滤液A中的某种离子与NH4+,HCO3-均能反应生成沉淀B,该离子与NH4+反应的离子方程式为___________。
(3)Al(OH)3在水中存在两种电离方式,其中:Al(OH)3(aq) AlO2-+H+(aq)+H2O(l) Ka=2.0×10-13(25℃),则25℃时Al(OH)3与NaOH溶液反应的平衡常数K=________________(列出含Kw、Ka的表达式并计算)
AlO2-+H+(aq)+H2O(l) Ka=2.0×10-13(25℃),则25℃时Al(OH)3与NaOH溶液反应的平衡常数K=________________(列出含Kw、Ka的表达式并计算)
(4)明矾与硫磺焙烧时发生反应的化学方程式为:KAl(SO4)2·12H2O+S K2SO4+Al2O3+SO2↑+H2O(未配平),配平后的化学计量数依次为____________;每生成67.2L标准状况下的SO2,转移电子的物质的量为________;焙烧产生的SO2经催化氧化、吸收等过程可制得硫酸,若SO2催化氧化时的转化率为96.0%,则理论上用该法生成硫酸时硫元素的总转化率为__________。
K2SO4+Al2O3+SO2↑+H2O(未配平),配平后的化学计量数依次为____________;每生成67.2L标准状况下的SO2,转移电子的物质的量为________;焙烧产生的SO2经催化氧化、吸收等过程可制得硫酸,若SO2催化氧化时的转化率为96.0%,则理论上用该法生成硫酸时硫元素的总转化率为__________。
-
KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
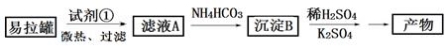
(1)为尽量少引入杂质,试剂①应选用 (填标号)。
A.HCl溶液 B.H2SO4溶液 C.氨水 D.NaOH溶液
(2)生成沉淀B的离子方程式为 ;明矾能用于净水,其原因是 ;往明矾溶液中滴加Ba(OH)2溶液,恰好使溶液中的SO42-完全沉淀的离子方程式为 。
。
-
Ⅰ.KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
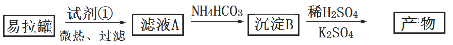
(1)为尽量少引入杂质,试剂①应选用___(填标号)。
a.HCl溶液 b.H2SO4溶液 c.氨水 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为______________________。
(3)沉淀B的化学式为___
II.毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:
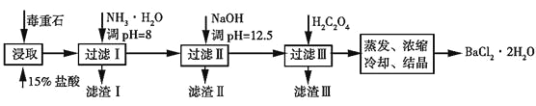
(4)毒重石用盐酸浸取前需充分研磨,目的是___________________________________。
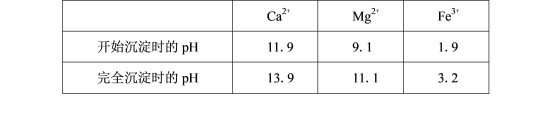
(5)滤渣Ⅱ中含________________(填化学式)。加入H2C2O4时应避免过量,原因是______________________。已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
-
KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
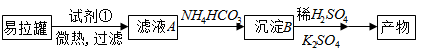
(1)为尽量少引入杂质,试剂①应选用__________(填序号)
A.NaOH溶液 B.H2SO4溶液 C.氨水 D.HCl溶液
(2)易拉罐溶解过程中主要反应的化学方程式为______________;
(3)由滤液A生成沉淀B反应的离子方程式为:_________________;
(4)明矾溶液中滴入Ba(OH)2溶液使SO42-恰好完全沉淀,离子方程式为______________。
-
KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
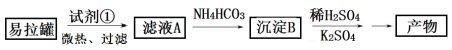
(1)为尽量少引入杂质,试剂①应选用___(填标号)。
a.HCl溶液 b.H2SO4溶液 c.氨水 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为________。
(3)沉淀B的化学式为________;将少量明矾溶于水,溶液呈弱酸性,其原因是__________。
(4)已知:Kw=1.0×10-14,Al(OH)3 AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
-
KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:

(1)为尽量少引入杂质,试剂①应选用___(填标号)。
A.HCl溶液 B.H2SO4溶液 C.氨水 D.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为________。
(3)沉淀B的化学式为________;将少量明矾溶于水,溶液呈弱酸性,其原因是__________。
(4)已知:Kw=1.0×10-14,Al(OH)3  AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
AlO2-+H++H2O K=2.0×10-13。Al(OH)3溶于NaOH溶液反应的平衡常数等于_________。
-
下列是铝的两种重要化合物的生产制备:
I.KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe 、Mg杂质)制备明矾的过程如下图所示。
、Mg杂质)制备明矾的过程如下图所示。
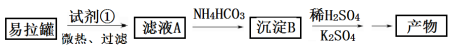
回答下列问题:
(1)为了少引入杂质,试剂①应选用___________(填标号)。
a.HCl溶液 b.H2SO4溶液 c.氨水 d.NaOH溶液
(2)沉淀B的化学式为____________;将少量明矾溶于水,溶液呈弱酸性,其原因是______________。
II.以铝土矿(主要成分是Al2O3,杂质有SiO2、Fe2O3等)为原料,采用拜耳法生产Al2O3的流程如下图所示:
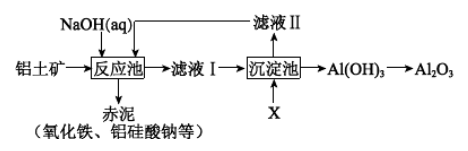
(1)Al2O3可用于电解制Al,其反应的化学方程式是______________________。
(2)调控反应池中钠铝元素之比一定时,Al2O3溶于NaOH,SiO2转化为铝硅酸钠沉淀。Al2O3溶于NaOH的离子方程式是_________________。
(3)该生产过程中,需向沉淀池中加入X。
① X 可为过量的CO2,则滤液II中主要的溶质是____________,为了使滤液II循环利用,应补充的物质是____________(选填字母);
a.CaO b.HCl c.Na2CO3
② X 也可为少量Al(OH)3晶种(晶种可加速沉淀的生成),其优点是_______________。
-
KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,有少量的Fe、Mg杂质)制备明矾的过程如图所示。回答下列问题:

(1)操作1中用到的玻璃仪器有________________。
(2)为尽量少引入杂质,从易拉罐溶解至生成Al(OH)3,过程中,主要发生反应的离子反应方程式为______________,__________________________;试剂②是_______________________________。
(3)已知:常温下KW=1.0×10-14 ,Al(OH)3溶于NaOH溶液反应的平衡常数等于20。则Al(OH)3+H2O⇌[Al(OH)4]-+H+平衡常数K=_________________。
(4)天然水在净化处理过程中加入明矾作混凝剂,水的净化和软化的区别是______________。
(5)普通纸张的主要成分是纤维素,在早期的纸张生产中,常采用纸表面涂敷明矾的工艺,以填补其表面的微孔,防止墨迹扩散。人们发现纸张会发生酸性腐蚀而变脆、破损,严重威胁纸质文物的保存。经分析检验,发现酸性腐蚀主要与造纸中涂覆明矾的工艺有关,请说明理由:_____________________;为保护这些纸质文物,有人建议采取喷洒Zn(C2H5)2的方法,其可以与水反应生成氧化锌和乙烷。用反应方程式表示该方法生成氧化锌及防止酸性腐蚀的原理________________________________。
-
KAl(SO4)2·12H2O(明矾)是一种复盐,应用广泛。采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如图15所示。请回答下列问题:

(1)请写出Al3+的结构示意图:______________________。
(2)试剂①最好选用___________(填序号)。写出A溶解的化学方程式:_________________________。
A.HCl溶液 B.H2SO4溶液 C.NaOH溶液 D.氨水
(3)写出滤液A到沉淀B的离子方程式:______________________;室温下,Al(OH)3 AlO2-+H++H2O K=2.0×10-13, H2CO3的Ka1=1×10-7,Ka2=4×10-11,计算滤液A到沉淀B的平衡常数 K=___________。
AlO2-+H++H2O K=2.0×10-13, H2CO3的Ka1=1×10-7,Ka2=4×10-11,计算滤液A到沉淀B的平衡常数 K=___________。
(4)写出由溶液C得到产物的操作:__________________________________。
(5)常温下,pH值相等的NaAlO2和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍,则两种溶液的pH=___________。