一种镁-过氧化氢燃料电池的原理为Mg + H2O2 + H2SO4=MgSO4+ 2H2O ,其装置如图所示。下列说法错误的是
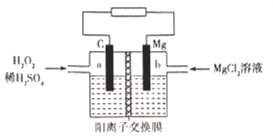
A.a极发生还原反应 B.电子由b极经电解质溶液流向a极
C.Mg2+由右侧经过阳离子交换膜移向左侧 D.b极电极反应式为Mg-2e-=Mg2+
高一化学单选题中等难度题
一种镁-过氧化氢燃料电池的原理为Mg + H2O2 + H2SO4=MgSO4+ 2H2O ,其装置如图所示。下列说法错误的是

A.a极发生还原反应 B.电子由b极经电解质溶液流向a极
C.Mg2+由右侧经过阳离子交换膜移向左侧 D.b极电极反应式为Mg-2e-=Mg2+
高一化学单选题中等难度题
一种镁-过氧化氢燃料电池的原理为Mg + H2O2 + H2SO4=MgSO4+ 2H2O ,其装置如图所示。下列说法错误的是

A.a极发生还原反应 B.电子由b极经电解质溶液流向a极
C.Mg2+由右侧经过阳离子交换膜移向左侧 D.b极电极反应式为Mg-2e-=Mg2+
高一化学单选题中等难度题查看答案及解析
某镁燃料电池以镁片、石墨作为电极,电池反应为Mg+H2O2+H2SO4=MgSO4 +2H2O。电池工作时,下列说法正确的是
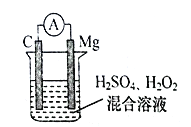
A.镁片的质量减小 B.镁片是电池的正极
C.电子由石墨棒经导线流向镁片 D.该装置将电能转化为化学能
高一化学单选题简单题查看答案及解析
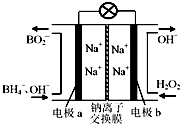
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法错误的是
A.电池放电时Na+从a极区移向b极区
B.电极b采用MnO2,MnO2既作电极材料又有催化作用
C.该电池的负极反应为:BH4-+8OH――8e-=BO2-+6H2O
D.每消耗3molH2O2,转移的电子为3mol
高一化学选择题简单题查看答案及解析
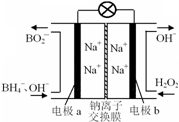
据报道,以硼氢化合物NaBH4(B元素的化合价为十3 价)和H2O2作原料的燃料电池,负极材料采用Pt/C ,正极材料采用MnO2 可用作空军通信卫星电源,其工作原理如图所示。下列说法错误的是( )
A.电池放电时Na+从a极区移向b极区
B.电极b采用MnO2,MnO2既作电极又有催化作用
C.该电池的a 极反应为BH4-+8OH--8e-═BO2-+6H2O
D.每消耗3mol H2O2,转移的电子为3mol
高一化学选择题困难题查看答案及解析
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法错误的是( )
A.电池放电时Na+从a极区移向b极区
B.电极b采用MnO2,MnO2既作电极材料又有催化作用
C.每消耗3mol H2O2,转移的电子为3mol
D.该电池的a极反应为:BH4-+8OH--8e-═BO2-+6H2O
高一化学选择题极难题查看答案及解析
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2做原料的燃料电池,负极材料采用Pt/C.正极材料采用MnO2,可用做空军通信卫星电源,其丁作原理如图所示.下列说法中错误的是( )
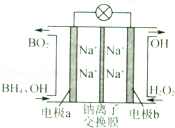
A.电池放电时Na+从a极区移向b极区
B.电极b采用Mn O2,Mn O2既做电极材料又有催化作用
C.该电池的负极反应为BH4-+8OH﹣一8e﹣═BO2-+6H2O
D.每消耗3molH2O2,转移的电子为3mol
高一化学选择题简单题查看答案及解析
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2做原料的燃料电池,负极材料采用Pt/C.正极材料采用MnO2,可用做空军通信卫星电源,其工作原理如图所示。下列说法中不正确的是
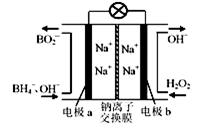
A. 电池放电时Na+从a极区移向b极区
B. 燃料电池是一类能量转化效率高、环境友好的发电装置
C. 该电池的负极反应为BH4-+ 8OH-一8e-═BO2-+ 6H2O
D. 在电池反应中,每消耗3molH2O2,转移电子数为3NA
高一化学选择题困难题查看答案及解析
用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是
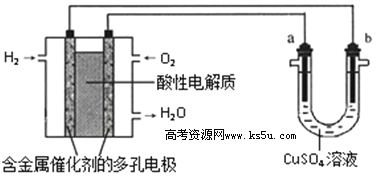
A. 燃料电池工作时,正极反应为:O2 + 2H2O + 4e-= 4OH-
B. a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出
C. a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
D. a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等
高一化学单选题困难题查看答案及解析
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理下图所示,下列说法正确的是
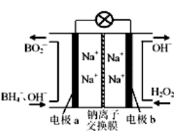
A.电池放电时Na+从a极区移向b极区
B.电极a采用MnO2,放电时它被还原
C.该电池负极的电极反应式为:BH4-+8OH--8e-═BO2-+6H2O
D.放电时,a极区的电极反应生成碱,碱性增强
高一化学选择题中等难度题查看答案及解析
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。下列有关说法正确的是 ( )
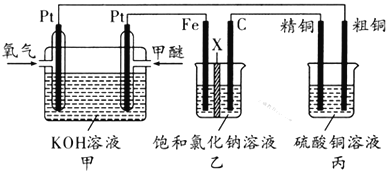
A. 反应一段时间后,乙装置中生成的氢氧化钠在铁极区
B. 乙装置中铁电极为阴极,电极反应式为Fe-2e-Fe2+
C. 通入氧气的一极为正极,发生的电极反应为O2-4e-+2H2O4OH-
D. 反应一段时间后,丙装置中硫酸铜溶液浓度保持不变
高一化学单选题困难题查看答案及解析