-
双极膜由阳离子交换膜、催化剂层和阴离子交换膜组合而成,在直流电场作用下可将水解离,在双极膜的两侧分别得到H+和OH-,将其与阳离子交换膜(阳膜)、阴离子交换膜(阴膜)组合,可有多种应用。
(1)海水淡化:模拟海水淡化,双极膜组合电解装置示意图如下。

①X极是______极(填“阴”或“阳”)。
②电解后可获得较浓的盐酸和较浓的NaOH溶液,上图中双极膜的右侧得到的是______(填“H+”或“OH-”)。
(2)钠碱循环法脱除烟气中的SO2,并回收SO2:
用pH>8的Na2SO3溶液作吸收液,脱除烟气中的SO2,至pH<6时,吸收液的主要成分为NaHSO3,需再生。
Ⅰ.加热pH<6时的吸收液使其分解,回收SO2并再生吸收液。所得的再生吸收液对SO2的吸收率降低,结合离子方程式解释原因:______。
Ⅱ.双极膜和阴膜组合电渗析法处理pH<6时的吸收液,可直接获得再生吸收液和含较高浓度HSO3−的溶液,装置示意图如下。

①再生吸收液从______室流出(填“A”或“B”)。
②简述含较高浓度HSO3−的溶液的生成原理:______。
③与Ⅰ中的方法相比,Ⅱ中的优点是______(列出2条)。
-
工业上可采用惰性电极处理含Na2SO4的废水,得到其它工业产品。其原理如图所示,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。
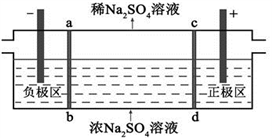
下列叙述不正确的是
A. 通电后中间隔室的SO42-离子向正极区迁移,电解后正极区PH减小
B. ab为阳离子交换膜,负极区得到NaOH溶液
C. 负极区反应为2 H2O–4e–=O2+4H+,负极区溶液pH降低
D. 每有1molO2生成,会有4molNa+进入负极区
-
三室式电渗析祛处理废液(HCl 和FeCl2混合溶液)的原理如图所示,其中X、Y均为离子交换膜。在直流电场的作用下,中间室得到盐酸,阴极区可回收铁。下列说法正确的是
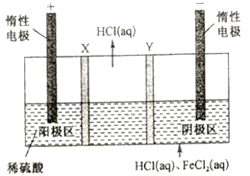
A. X、Y 依次是阴离子透过膜和阳离子透过膜
B. 通电后,阴极区溶液的pH 不断减小
C. 阳极反应式为2H2O-4e-==4H+ + O2 ↑
D. 中间室得到1L 2 mol/L盐酸时,电路中通过1mol电子
-
三室式电渗析法处理含NH4NO3废水的原理如图所示,在直流电场的作用下,两膜中间的NH4+和NO2—可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.工作一段时间后,在两极区均得到副产品NH4NO3.下列叙述正确的是

A. a极为电源负极,b极为电源正极
B. c膜是阴离子交换膜,d膜是阳离子交换膜
C. 阴极电极反应式为2NO3-+12H++10e-=N2 +6H2O
D. 当电路中通过1mol电子的电量时,会有5.6LO2生成
-
电解硫酸钠溶液生产硫酸和烧碱溶液的装置如图所示,a、b均为惰性电极,在直流电场的作用下,中间隔室的Na+、SO42-可分别通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列有关说法正确的是
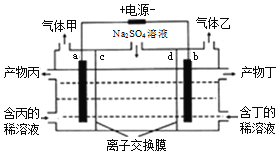
A. a极的电极反应式为2H2O+2e-=H2↑+2OH-
B. c为阳离子交换膜,d为阴离子交换膜
C. 气体乙为O2,产物丁为硫酸
D. 若撤去离子交换膜c、d再电解硫酸钠溶液,则不能制得硫酸和烧碱
-
目前可采用“双极膜组”电渗析法淡化海水,同时获得副产品A和B。其模拟工作原理如图所示。M、N为离子交换膜,在直流电作用下,双极阴阳膜(BP)复合层间的H2O解离成H+和OH-,作为H+和OH-的离子源。下列说法正确的是
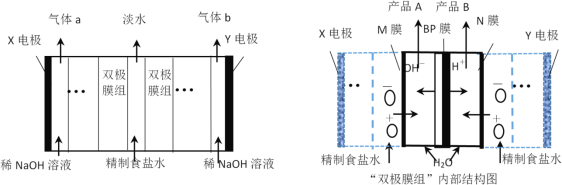
A.Y电极为阳极,电极反应式为2Cl――2e-=Cl2↑
B.M为阳离子交换膜,N为阴离子交换膜,BP膜作用是选择性通过Cl-和Na+
C.电路中每生成0.25 mol气体a,理论上获得副产品A和B各1 mol
D.“双极膜组”电渗析法也可应用于从盐溶液(MX)制备相应的酸(HX)和碱(MOH)
-
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,甲、乙均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是
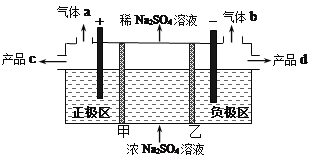
A. 甲为阳离子交换膜,通电后中间隔室的Na+离子向正极迁移
B. 通电后,同温同压下得到的气体a与气体b的体积比约为2:1
C. 通电后,得到的产品c是NaOH,产品d是H2SO4
D. 负极区发生的电极反应为2H2O +2e-=2OH-+H2↑,负极区溶液pH增大
-
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,甲、乙均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是
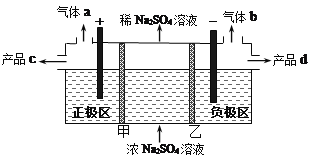
A. 甲为阳离子交换膜,通电后中间隔室的Na+离子向正极迁移
B. 通电后,同温同压下得到的气体a与气体b的体积比约为2:1
C. 通电后,得到的产品c是NaOH,产品d是H2SO4
D. 负极区发生的电极反应为2H2O +2e-=2OH-+H2↑,负极区溶液pH增大
-
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和 可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。
可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。
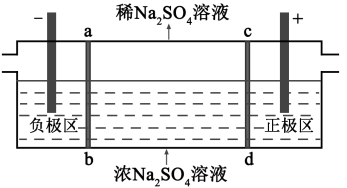
下列叙述正确的是
A.通电后中间隔室的 离子向正极迁移,正极区溶液pH增大
离子向正极迁移,正极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.负极反应为2H2O − 4e– = O2+4H+,负极区溶液pH降低
D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成
-
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。
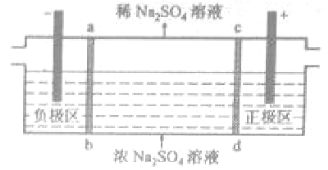
下列叙述正确的是
A.通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B.该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C.负极反应为2 H2O–4e–=O2+4H+,负极区溶液pH降低
D.当电路中通过1mol电子的电量时,会有0.5mol的O2生成










