-
氢能源是公认的零碳消洁能源,用乙醇为原料可通过多种方法制氢,具有理想的应用前景。回答下列问题:
(一)乙醇催化重整制氢
原理:C2H5OH(g)+3H2O(g) 2CO2(g)+6H2(g)△H1
2CO2(g)+6H2(g)△H1
以Ni/凹凸棒石做催化剂,在2L刚性容器中,分别以水醇比为2:1、4:1、6:1、8:1投料(乙醇的起始物质的量相同),反应相同时间测得乙醇转化率随温度变化的关系如图所示。
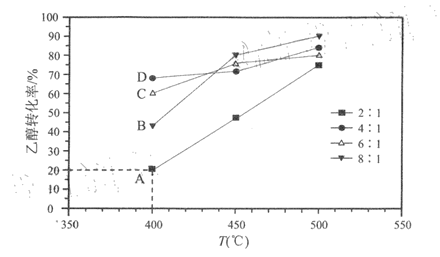
已知:过多的水分子会占据催化剂表面活性位,导致反应速率降低:上图中水醇比为2:1时,各点均已达到平衡状态。
(1)反应热△H1________0(填“>”或“<”)。若乙醇的起始物质的量为n0mol,则K(400℃)=______________(列出计算式)。
(2)400℃时,水醇比过高不利于乙醇转化的原因是____________________________;B、C、D三点中,一定未达到平衡状态的是______________(填标号)。
(二)乙醇氧化制氢
原理:C2H5OH(g)+ O2(g)
O2(g) 2CO2(g)+3H2(g) △H2
2CO2(g)+3H2(g) △H2
(3)已知H2(g)+ O2(g)
O2(g) H2O(g) △H3,则△H2=_____(用含△H1和△H3的式子表示)。在密闭容器中通入一定量的乙醇和氧气,达到平衡状态后增大容器体积,则混合气体的平均相对分子质量将_________(填“增大”“减小”或“不变”)。
H2O(g) △H3,则△H2=_____(用含△H1和△H3的式子表示)。在密闭容器中通入一定量的乙醇和氧气,达到平衡状态后增大容器体积,则混合气体的平均相对分子质量将_________(填“增大”“减小”或“不变”)。
(三)乙醇电解法制氢
乙醇电解法不仅可以利用乙醇本身的氢,还可以从水中获得氢,且电解乙醇所需电压比电解水的理论电压要低很多。
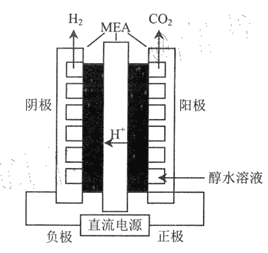
(4)利用如图所示装过(MEA为复杂的膜电极)电解乙醇制氢,阳极的电极反式应为___________,理论上每转移lmol电子,可以产生________L氢气(标准状况下)。
-
氢气是一种理想的绿色能源。利用生物质发酵得到的乙醇制取氢气,具有良好的应用前景。
乙醇水蒸气重整制氢的部分反应过程如下左图所示:
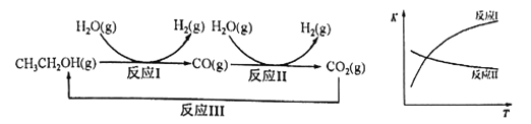
已知:反应Ⅰ和反应Ⅱ的平衡常数随温度变化曲线如上右图所示。
(1)反应Ⅰ中,1molCH3CH2OH(g)参与反应后的热量变化是256kJ。反应1的热化学方程式是_____________________。
(2)反应Ⅱ,在进气比[n(CO):n(H2O)]不同时,测得相应的CO的平衡转化率见下图(各点对应的反应温度可能相同,也可能不同)。
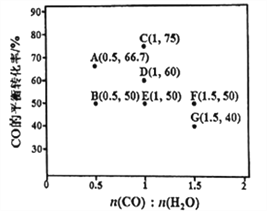
①图中D、E两点对应的反应温度分别为TD和TE判断:TD_______TE (填“<”“=”或“>”)。
②经分析,A、E 和G 三点对应的反应温度相同,其原因是A、E和G三点对应的________相同。
③当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系
是_________________。
(3)反应Ⅲ,在经CO2饱和处理的KHCO3电解液中,电解活化CO2制备乙醇的原理如图所示。

①阴极的电极反应式是____________________。
②从电解后溶液中分离出乙醇的操作方法是_________________。
③直接向KOH溶液中通入CO2,可以获得“经CO2饱和处理的KHCO3电解液”,该过程中浓度先增大后减小的离子是__________________ (填化学式)。
-
氢气是一种理想的绿色能源。利用生物质发酵得到的乙醇制取氢气,具有良好的应用前景。乙醇水蒸气重整制氢的部分反应过程如下图所示:
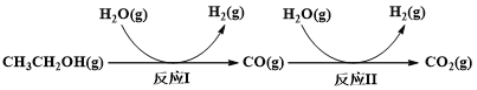
已知:反应I和反应II的平衡常数随温度变化曲线如下图所示。
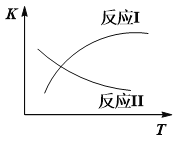
(1)①试说明反应Ⅰ能否发生自发反应______________________________________。
②反应Ⅰ、Ⅱ达平衡后,若在恒温恒压条件下,向体系中充入N2,CO的体积分数会________________(填“上升”、“不变”、“下降”)。
(2)反应II,在进气比[n(CO) : n(H2O)]不同时,测得相应的CO的平衡转化率见下图1
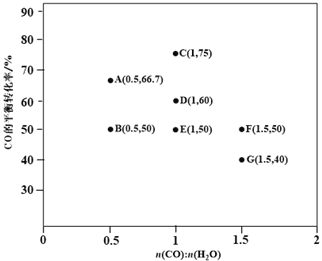
(各点对应的反应温度可能相同,也可能不同)。
③图中D、E两点对应的反应温度分别为TD和TE。判断:TD______TE(填“<”“=”或“>”)。
④经分析计算,A、E和G三点对应的反应温度相同,理由是_________________________。
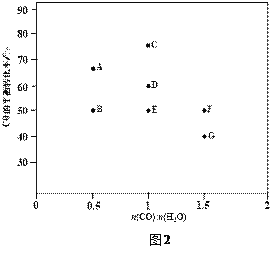
⑤在图2中,画出D点所对应温度下CO平衡转化率随进气比[n(CO) : n(H2O)]的曲线。____________
⑥以熔融Na2CO3为电解质的乙醇燃料电池具有广泛的应用,写出其负极的电极反应方程式。________________________________。
-
甲醇是一种重要的化工原料.

 已知:
已知: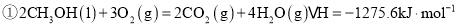

写出表示甲醇燃烧热的热化学方程式 ______ .
 甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景.其反应为:
甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景.其反应为:



 该反应的平衡常数表达式为 ______ .
该反应的平衡常数表达式为 ______ .
 下列措施中能使平衡时
下列措施中能使平衡时 减小的是
减小的是 双选
双选 ______ .
______ .
A.加入催化剂  恒容充入
恒容充入 ,使体系压强增大
,使体系压强增大
C.将 从体系中分离
从体系中分离  恒容再充入
恒容再充入
 甲醇可以氧化成甲酸,在常温下用
甲醇可以氧化成甲酸,在常温下用 NaOH溶液滴定
NaOH溶液滴定
 甲酸溶液过程中,当混合液的
甲酸溶液过程中,当混合液的 时,所消耗的
时,所消耗的 ______
______
 填“
填“ ”或“
”或“ ”或“
”或“ ”
”
 .
.
 利用甲醇燃烧设计为燃料电池,如图所示,则负极电极反应式为 ______ .
利用甲醇燃烧设计为燃料电池,如图所示,则负极电极反应式为 ______ .
 合成甲醇的主要反应为:
合成甲醇的主要反应为: 原料气的加工过程中常常混有一些
原料气的加工过程中常常混有一些 ,为了研究温度及
,为了研究温度及 含量对该反应的影响,以
含量对该反应的影响,以 、CO和
、CO和 的混合气体为原料在一定条件下进行实验.实验数据见下表:
的混合气体为原料在一定条件下进行实验.实验数据见下表:
| 
 体积分数 体积分数
| 
| 
| 
| 
|
| 反应温度 | 225 | 235 | 250 | 225 | 235 | 250 | 225 | 235 | 250 | 225 | 235 | 250 |
| 生成 的碳转化率 的碳转化率 | 
| 
| 
| 
| 
| 
| 
| 
| 
| 
| 
| 
|
由表中数据可得出多个结论.
结论一:在一定条件下,反应温度越高,生成 的碳转化率 ______ .
的碳转化率 ______ .
结论二: ______ .
-
甲醇是一种重要的化工原料。甲醇与水蒸气催化重整可获得清洁能源,具有广泛的应用前景。现有如下实验,在体积为1 L的密闭容器中,充入1mol CH3OH和1molH2O,一定条件下发生反应:CH3OH (g)+ H2O (g)  CO2(g) +3 H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示。
CO2(g) +3 H2 (g),测得CO2和CH3OH(g)的浓度随时间变化如下表所示。
| 时间 物质 | 0 min | 10 min | 30 min | 60 min | 70 min |
| CO2(mol/L) | 0 | 0.2 | 0.6 | 0.8 | 0.8 |
| CH3OH(mol/L) | 1.0 | 0.8 | 0.4 | 0.2 | 0.2 |
①已知:CH3OH (g)+  O2 (g)
O2 (g)  CO2(g) + 2H2 (g) H1= —192.9kJ/mol
CO2(g) + 2H2 (g) H1= —192.9kJ/mol
H2(g)+  O2 (g)
O2 (g)  H2 O(g) H2= —120.9kJ/mol
H2 O(g) H2= —120.9kJ/mol
则甲醇与水蒸气催化重整反应的焓变△H3=_____ 。
②10~30 min内,氢气的平均反应速率v(H2)=___________mol/(L·min)。
③该反应的平衡常数表达式为K=__________________。
④下列措施中能使平衡时n(CH3OH)/n(CO2)减小的是(双选)___________。
A.加入催化剂 B.恒容充入He(g),使体系压强增大
C.将H2(g)从体系中分离 D.再充入1molH2O
(2)甲醇在催化剂条件下可以直接氧化成甲酸。
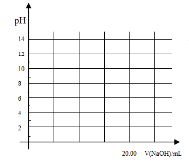
①在常温下,用0.1000 mol/L NaOH溶液滴定20. 00 mL 0.1000 mol/L 甲酸溶液过程中,当混合液的pH=7时,所消耗的V(NaOH)___(填“<”或“>”或“=”) 20. 00 mL。
②在上述滴定操作中,若将甲酸换成盐酸,请在图中的相应位置画出相应的滴定曲线。(1滴溶液约0.04mL)
-
甲醇水蒸气重整制氢方法是目前比较成熟的制氢方法,且具有良好的应用前景。甲醇水蒸气重整制氢的部分反应过程如图所示:
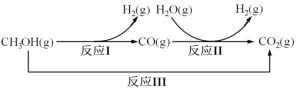
(1)已知一定条件下
反应I:CH3OH(g)==CO(g)+2H2(g) ΔH1=+90.7kJ/mol
反应III:CH3OH(g)+H2O(g) =CO2(g)+3H2(g) ΔH3=+49.5kJ/mol
该条件下反应II的热化学方程式是___。
(2)已知反应II在进气比[n(CO):n(H2O)]不同时,在不同温度(T1、T2)下,测得相应的CO的平衡转化率见图。

①比较T1、T2的大小,并解释原因___。
②A点对应的化学平衡常数是___。
③T1温度时,按下表数据开始反应建立平衡。
| CO | H2O | H2 | CO2 |
| 起始浓度(mol/L) | 2 | 1 | 0 | 0 |
| t时刻浓度(mol/L) | 1.2 | 0.2 | 0.8 | 0.8 |
反应进行到t时刻时,判断v(正)、v(逆)的大小关系为:v(正)__v(逆)(填“>”“<”或“=”)。
④当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系是___。
(3)在经CO2饱和处理的KHCO3电解液中,电解活化CO2可以制备乙醇,原理如图所示。
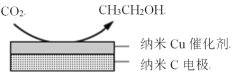
①阴极的电极反应式是___。
②从电解后溶液中分离出乙醇的操作方法是___。
-
甲醇水蒸气重整制氢方法是目前比较成熟的制氢方法,且具有良好的应用前景。甲醇水蒸气重整制氢的部分反应过程如图所示:
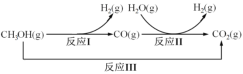
(1)已知一定条件下
反应I:CH3OH(g)=CO(g)+2H2(g) ΔH1=+90.7kJ/mol
反应III:CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH3=+49.5kJ/mol
该条件下反应II的热化学方程式是___。
(2)已知反应II在进气比[n(CO):n(H2O)]不同时,在不同温度(T1、T2)下,测得相应的CO的平衡转化率见图。

①比较T1、T2的大小,T1___T2(填“>”“<”或“=”)。
②A点对应的化学平衡常数是___。
③T1温度时,按下表数据开始反应建立平衡
| CO | H2O | H2 | CO2 |
| 起始浓度(mol/L) | 2 | 1 | 0 | 0 |
| t时刻浓度(mol/L) | 1.2 | 0.2 | 0.8 | 0.8 |
反应进行到t时刻时,判断v(正)、v(逆)的大小关系为:v(正)___v(逆)(填“>”“<”或“=”)。
④当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系是___。
(3)CO2在生产中有着广泛的用途。
①将过量CO2通入KOH溶液中可生成KHCO3,请写出该反应的离子方程式___。
②在经CO2饱和处理的KHCO3弱酸性溶液中,电解活化CO2可以制备乙醇,原理如图所示。该电极为___(填“阴极”或“阳极”),电极反应式是___。
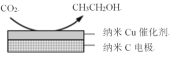
-
应对雾霾污染、改善空气质量需要从多方面入手,如开发利用清洁能源.甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景.回答下列问题:
(1) 与
与 合成甲醇:
合成甲醇: 但是找到合适的催化剂是制约该方法的瓶颈.目前主要使用贵金属催化剂,但是贵金属储量稀少,成本高昂,难以大规模应用,且使用中存在环境污染的风险.最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现
但是找到合适的催化剂是制约该方法的瓶颈.目前主要使用贵金属催化剂,但是贵金属储量稀少,成本高昂,难以大规模应用,且使用中存在环境污染的风险.最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现 电催化还原制备甲醇方向取得重要进展,该反应历程如图所示.
电催化还原制备甲醇方向取得重要进展,该反应历程如图所示.
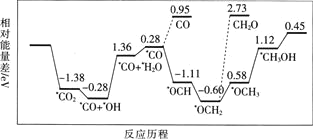
容易得到的副产物有CO和 ,其中相对较多的副产物为________________;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中________
,其中相对较多的副产物为________________;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中________ 填字母
填字母 的能量变化.
的能量变化.
A. B.
B.
C. D.
D.
(2)恒压 容器的容积可变
容器的容积可变 下,
下, 与
与 在催化剂作用下发生反应
在催化剂作用下发生反应
 ,
, 的平衡转化率与温度、压强的关系如图所示.
的平衡转化率与温度、压强的关系如图所示.
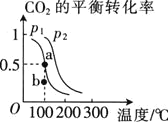
①压强 ________
________ 填“
填“ ”或“
”或“ ”
” .
.
②在 、
、 条件下,b点时
条件下,b点时 ________
________ 填“
填“ ”或“
”或“ ”
” .
.
③已知:反应速率 ,
, 、
、 分别为正、逆反应速率常数,x为物质的量分数,若b点对应的坐标参数为
分别为正、逆反应速率常数,x为物质的量分数,若b点对应的坐标参数为 ,计算b处的
,计算b处的 ________
________ 保留3位有效数字
保留3位有效数字 .
.
(3)焦炭与水蒸气在恒容密闭容器中反应制合成气的主要反应 Ⅰ
Ⅰ 、
、 Ⅱ
Ⅱ 的
的 为以分压表示的平衡常数
为以分压表示的平衡常数 与T的关系如下图所示.
与T的关系如下图所示.
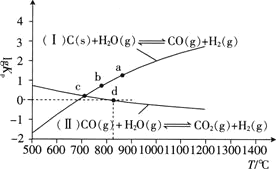
①反应 Ⅱ
Ⅱ 的
的 ________
________ 填“大于”“等于”或“小于”
填“大于”“等于”或“小于” .
.
② 点时,反应
点时,反应 的
的 ________
________ 填数值
填数值 .
.
③在恒容密闭容器中充入 、
、 只发生反应
只发生反应 Ⅱ
Ⅱ ,图中d点处达到平衡时,CO的转化率为________;达到平衡时,向容器中再充入
,图中d点处达到平衡时,CO的转化率为________;达到平衡时,向容器中再充入 、
、 ,重新达到平衡时,CO的平衡转化率________
,重新达到平衡时,CO的平衡转化率________ 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” .
.
-
(1)以甲醇为原料制取高纯H2具有重要的应用价值。甲醇水蒸气重整制氢主要发生以下两个反应:
主反应: ∆H=+49kJ∙mol-1
∆H=+49kJ∙mol-1
副反应: ∆H=+41kJ∙mol-1
∆H=+41kJ∙mol-1
①甲醇蒸气在催化剂作用下裂解可得到H2和CO,则该反应的热化学方程式为_________________,既能加快反应速率又能提高CH3OH平衡转化率的一种措施是______________。
②分析适当增大水醇比 对甲醇水蒸气重整制氢的好处是__________。
对甲醇水蒸气重整制氢的好处是__________。
③某温度下,将n(H2O):n(CH3OH)=1:1的原料气充入恒容密闭容器中,初始压强为P1,反应达平衡时总压强为P2,则平衡时甲醇的转化率为________________(忽略副反应,用含P1、P2的式子表示)。
(2)工业上用CH4与水蒸气在一定条件下制取H2,原理为: ∆H=+203kJ∙mol-1
∆H=+203kJ∙mol-1
①该反应逆反应速率表达式为:v逆=k·c(CO)·c3(H2),k为速率常数,在某温度下测得实验数据如下表:
| c(CO)/mol·L-1 | c(H2)/mol·L-1 | v逆/mol·L-1·min-1 |
| 0.05 | c1 | 4.8 |
| c2 | c1 | 19.2 |
| c2 | 0.15 | 8.1 |
由上述数据可得该温度下,该反应的逆反应速率常数k为_________L3·mol-3·min-1。
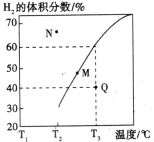
②在体积为3L的密闭容器中通入物质的量均为3mol的CH4和水蒸气,在一定条件下发生上述反应,测得平衡时H2的体积分数与温度关系如图所示:N点v正____________M点v逆(填“大于”或“小于”);Q点对应温度下该反应的平衡常数K=_______________mol2·L-2。平衡后再向容器中加入1molCH4和1molCO,平衡向_____________方向移动(填“正反应”或“逆反应”)。
-
氢气的制取与储存是氢能源利用领域的研究热点。回答下列问题:
(1)直接热分解法制氢
某温度下,2H2O(g) 2H2(g) +O2(g),该反应的平衡常数表达式为K=______。
2H2(g) +O2(g),该反应的平衡常数表达式为K=______。
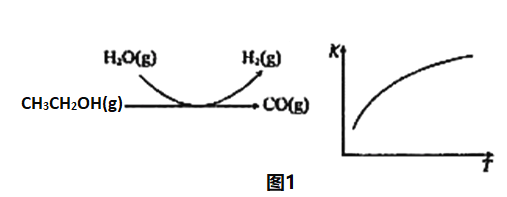
(2)乙醇水蒸气重整制氢
反应过程和反应的平衡常数(K)随温度(T)的变化曲线如图1所示。某温度下,图1所示反应每生成1mol H2(g),热量变化是62 kJ,则该反应的热化学方程式为_____________。
(3)水煤气法制氢
CO(g)+ H2O(g) CO2(g) +H2(g) △H<0
CO2(g) +H2(g) △H<0
在进气比[n(CO):n(H2O)]不同时,测得相应的CO的平衡转化率见图2(图中各点对应的反应温度可能相同,也可能不同)。
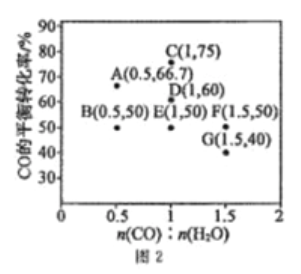
①向2 L恒温恒容密闭容器中加入一定量的CO和0.1mol H2O(g),在图中G点对应温度下,反应经5 min 达到平衡,则平均反应速率v(CO)=________。
②图中B、E 两点对应的反应温度分别为TB和TE,则TB_____TE (填“>”“ <”或“=”)。
③经分析,A、E、G三点对应的反应温度都相同(均为T℃),其原因是A、E、G 三点对应的_________相同。
④当T℃时,若向一容积可变的密闭容器中同时充入3.0 mol CO、1.0 mol H2O(g)、1.0 molCO2和x mol H2,为使上述反应开始时向正反应方向进行,则x应满足的条件是______。
(4)光电化学分解制氢
反应原理如图3,钛酸锶光电极的电极反应式为4OH--4e-=O2↑+2H2O,则铂电极的电极反应式为________________。
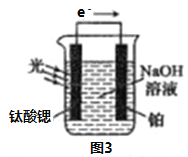
(5)Mg2Cu 是一种储氢合金。350℃时,Mg2Cu 与H2反应,生成MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数约为7.7%)。该反应的化学方程式为______________。
2CO2(g)+6H2(g)△H1

O2(g)
2CO2(g)+3H2(g) △H2
O2(g)
H2O(g) △H3,则△H2=_____(用含△H1和△H3的式子表示)。在密闭容器中通入一定量的乙醇和氧气,达到平衡状态后增大容器体积,则混合气体的平均相对分子质量将_________(填“增大”“减小”或“不变”)。




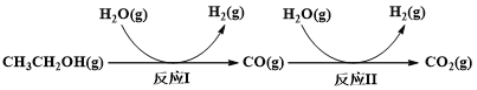




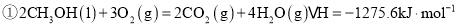
 原料气的加工过程中常常混有一些
原料气的加工过程中常常混有一些












