-
(1)如图是一个化学过程的示意图。
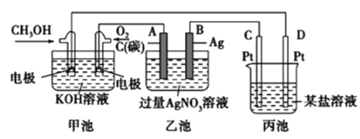
①乙池中总反应的离子方程式____________。
②电解一段时间后,向乙池的溶液中加入________________可恢复为原溶液。
③当乙池中B(Ag)极的质量增加5.40g,此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是________。
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
(2)利用反应Cu+2FeCl3=CuCl2+2FeCl2设计成如图所示原电池,回答下列问题:
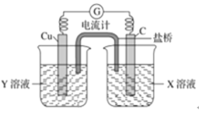
①写出负极的电极反应式:___________。
②图中X溶液是________。
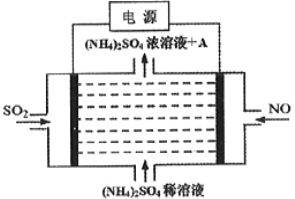
③利用图中设计的原电池为电源可将雾霾中的NO、SO2电解分别转化为NH4+和SO42-,如图所示,则物质A的化学式为_____________,阴极的电极反应式为______________。
-
如图是一个电化学过程的示意图.请回答下列问题:
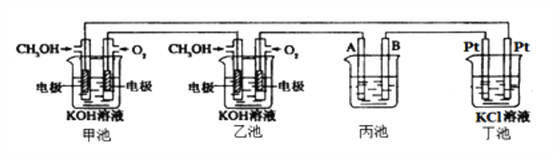
(1)通入CH3OH的电极的电极反应式为__________________.
(2)丙池是铜的精炼池,电解一段时间后烧杯中的溶液浓度会______(填“增大、减小、不变”),A电极反应式_______________________(已知粗铜中含有Zn,Ag杂质).
(3)丁池中滴有酚酞,实验开始后观察到的现象_____________________,丁池采用无隔膜电解,产生的氯气可能会与KOH溶液接触仅得到KClO和H2,则相应的化学反应方程式为____________________________________________________。
(4)若甲、乙两个电池氧气通入量均为20L(标准状况),且反应完全,则理论上通过丁池的电量为__________(法拉第常数F=9.65×l04C•mol-1),丁池最多能产生气体的总体积为______L(标准状况)。
-
某氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如图:
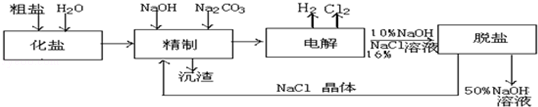
依据图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为 ;与电源负极相连的电极附近,溶液pH值 .(选填:不变、升高或下降)
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为 ;
(3)如果粗盐中SO42﹣含量较高,必须添加钡试剂除去SO42﹣,该钡试剂可以是 (选填a、b、c多选倒扣分)
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为有效除去Ca2+、Mg2+、SO42﹣,加入试剂的合理顺序为 (选填a、b、c多选倒扣分)
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过 、冷却、 (填写操作名称)除去NaCl.
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为 .
-
某电化学装置如图所示(电极a、b均为碳棒)。
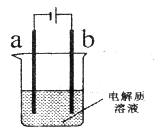
(1)烧杯中盛有饱和NaCl溶液,往烧杯中加几滴酚酞试液,通电发生反应。则电解总反应方程式为_____________。电极a上及附近溶液中的实验现象为_____________。
(2)若烧杯中盛有200mL 0.1mol/L CuSO4溶液。通电反应一段时间,在两极收集到的气体体积相等,则此段时间e-转移的物质的量为_________mol。
-
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图
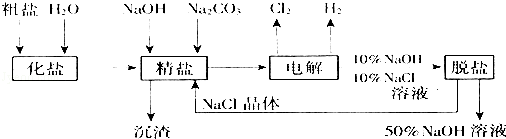
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为 ,与电源负极相连的电极附近,溶液pH (选填“不变”“升高”或“下降”).
(2)为有效除去Ca2+、Mg2+、SO42﹣,加入试剂及合理顺序为
(3)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为 .
(4)用石墨电极作阴极,铁电极作阳极电解水时往往产生大量的红棕色沉淀,请用化学反应解释这一现象: .
-
氯碱厂电解饱和食盐水制取NaOH溶液的工艺流程如图所示,完成下列填空:

(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为________________,与电源负极相连的电极附近,溶液pH________(填“不变”“升高”或“下降”)。
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为_______________ ____、 。
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是_____ (选填a、b、c)。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为了有效地除去Ca2+、Mg2+、SO42-,加入试剂的顺序为________(选填a、b、c)。
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过 、冷却、________(填写操作名称)除去NaCl。
(6)电解饱和食盐水的离子方程式为___________ _______
-
工业上的许多反应工艺来源于实验室里的简单操作,比如用铝土矿(成分为氧化铝、氧化铁)制取铝的过程如图:

请回答下列问题:
(1)写出铝土矿中加入NaOH溶液的反应方程式___。
(2)沉淀C的化学式___,颜色为___,写出它的一种用途___。
(3)操作I、操作II、操作III的名称为___,这个过程用到的玻璃仪器有烧杯、___。
(4)整个生产过程中,除可以循环使用的物质有___(写出3种,填化学式),用此法制取铝的副产品是___(写出2种,填化学式)。
(5)氧化铝熔点高,氯化铝熔点低,工业上为什么不用熔点较低的氯化铝而用熔点更高的氧化铝为原料电解制铝?___。
-
(3分)在硫酸铜溶液中加入过量的氢氧化钠溶液后,再滴入足量乙醛溶液,加热。实验过程中发生的反应的化学方程式为 。
-
由甲醇 、氧气和
、氧气和 溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
(1)写出该电池负极电极反应式______
(2)若以该电池为电源,用石墨作电极电解含有如下离子的溶液。
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),阳极上发生的电极反应为______;阴极收集到的气体体积为(标准状况)______。
(3)若用该电池做电源,用石墨做电极电解硫酸铜溶液,当电路中转移 时,实际上消耗的甲醇的质量比理论上大,可能原因是______。
时,实际上消耗的甲醇的质量比理论上大,可能原因是______。
-
(14分)实验和探究对化学学科的发展起着非常重要的作用
(1)写出下列实验过程中所体现的总的离子反应方程式:
①用PH试纸测得醋酸钠溶液呈碱性:__________
②用石墨做电极,电解硝酸银溶液后,溶液呈酸性:__________
③根据浑浊出现的快慢,探究硫代硫酸钠与酸反应速率的影响因素:__________
(2)已知锌能溶解在NaOH溶液中,产生H2。某同学据此设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S、质量为m1的镀锌铁皮与石墨用导线相连,放入6 NaOH溶液中,判断锌层完全反应的标志是:__________,最后,取出铁片用水冲洗、烘干后称量,得质量为m2,设锌镀层单侧厚度为h,锌的密度为
NaOH溶液中,判断锌层完全反应的标志是:__________,最后,取出铁片用水冲洗、烘干后称量,得质量为m2,设锌镀层单侧厚度为h,锌的密度为 ,则h=__________
,则h=__________
(3)实验室测定绿矾中FeSO4 含量的步骤是:称1g绿矾,用30mL蒸馏水溶解并加入H2SO4溶液和H3PO4溶液,再用0.02mol/L KMnO4标准溶液滴定到溶液刚变成粉红色,停止滴定,消耗标准溶液VmL。反应中涉及的重要化学方程式有:
含量的步骤是:称1g绿矾,用30mL蒸馏水溶解并加入H2SO4溶液和H3PO4溶液,再用0.02mol/L KMnO4标准溶液滴定到溶液刚变成粉红色,停止滴定,消耗标准溶液VmL。反应中涉及的重要化学方程式有:


①绿矾的含量为__________%。
② 的作用是__________。
的作用是__________。








