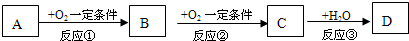-
碳、氮能形成多种氧化物、氢化物。
(1)已知:①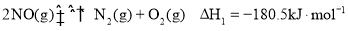
②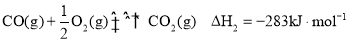
则 与
与 反应生成两种无毒气体的热化学方程式为_____________。
反应生成两种无毒气体的热化学方程式为_____________。
(2)使用高效催化剂可大大减少汽车尾气排放出的 含量,某研究所的科研人员探究了
含量,某研究所的科研人员探究了 时等质量的三种催化剂对
时等质量的三种催化剂对 还原
还原 的催化效果(其他条件相同),所得结果如图所示:
的催化效果(其他条件相同),所得结果如图所示:
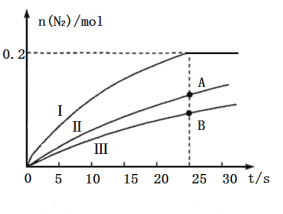
①如果不考虑催化剂价格,则使用催化剂______(填“Ⅰ”“Ⅱ”或“Ⅲ”)最好;A、B两状态下,生成 的速率大小关系是___________。
的速率大小关系是___________。
②若容器容积为2L,开始时加入 、
、 ,在催化剂Ⅰ的作用下达到如图所示平衡,则反应
,在催化剂Ⅰ的作用下达到如图所示平衡,则反应 在该温度下的平衡常数
在该温度下的平衡常数 ______
______ 。
。
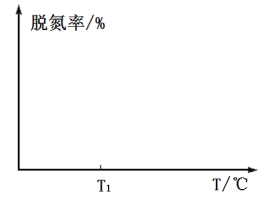
③在如图坐标系中画出使用催化剂Ⅰ(其他条件相同)时,25s时容器内反应的脱氮率( 转化率)与温度的关系图___________。
转化率)与温度的关系图___________。
(3)化学动力学上将一步完成的反应称为基元反应。对于基元反应: ,其速率方程式为
,其速率方程式为 (k为只与温度有关的速率常数),复杂反应(由几个基元反应构成)的速率取决于慢的基元反应。
(k为只与温度有关的速率常数),复杂反应(由几个基元反应构成)的速率取决于慢的基元反应。
①已知反应 ,在温度低于
,在温度低于 时是由两个基元反应构成的复杂反应,该反应的速率方程式为
时是由两个基元反应构成的复杂反应,该反应的速率方程式为 ,则其两个基元反应分别为:Ⅰ.______
,则其两个基元反应分别为:Ⅰ.______ ______;Ⅱ.略,这两个反应中活化能较小的是__________。
______;Ⅱ.略,这两个反应中活化能较小的是__________。
②某科研小组测得 时该反应的
时该反应的 、
、 生成
生成 的速率
的速率 的关系如下:
的关系如下:
| 
| 0.025 | 0.05 | 0.025 |
| 
| 0.04 | 0.04 | 0.12 |
| 
| 
| 
| 
|
则该温度下的反应速率常数 ______
______ 。
。
-
氮的氧化物(用NOx表示)是大气污染物,必须加以处理.
(1)汽车尾气中的CO、NOx采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体.反应化学方程式可表示为:________.
(2)步骤一
工业尾气中氮的氧化物常采用氨催化吸收法,原理是NH3与NOx反应生成无毒的物质.某同学采用以下装置和步骤模拟工业上氮的氧化物处理过程.提供的装置:
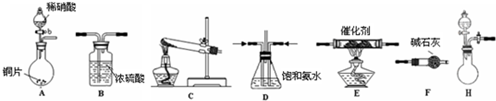
①所提供的装置中能快速、简便制取NH3的装置是:________(填仪器序号).
②若采用C装置制取氨气(控制实验条件相同),情况如下表:
| 试剂组合序号 | 固体试剂(g) | NH3体积(mL) |
| a | 12.0g Ca(OH)2 (过量) | 10.8g NH4Cl | 2688 |
| b | 10.8g (NH4)2SO4 | 2728 |
| c | 12.0g NaOH (过量) | 10.8g NH4Cl | 3136 |
| d | 10.8g (NH4)2SO4 | 3118 |
| e | 12.0g CaO (过量) | 10.8g NH4Cl | 3506 |
| f | 10.8g (NH4)2SO4 | 3584 |
分析表中数据,实验室制NH3产率最高的是:________(填序号),其它组合NH3产率不高的原因是:________.
步骤二.
模拟尾气的处理选用上述部分装置,按下列顺序连接成模拟尾气处理装置:
①A中反应的离子方程式:________.
②D装置作用有:使气体混合均匀、调节气流速度,还有一个作用是:________.
③D装置中的液体可换成________(填序号).
a.CuSO4溶液 b.H2O c.CCl4 d.浓H2SO4
④该同学所设计的模拟尾气处理实验还存在的明显缺陷是:________.
-
氮的氧化物(用NOx表示)是大气污染物,必须加以处理.
(1)汽车尾气中的CO、NOx采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体.反应化学方程式可表示为:________.
(2)步骤一
工业尾气中氮的氧化物常采用氨催化吸收法,原理是NH3与NOx反应生成无毒的物质.某同学采用以下装置和步骤模拟工业上氮的氧化物处理过程.提供的装置:
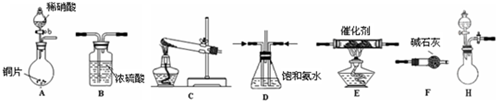
①所提供的装置中能快速、简便制取NH3的装置是:________(填仪器序号).
②若采用C装置制取氨气(控制实验条件相同),情况如下表:
| 试剂组合序号 | 固体试剂(g) | NH3体积(mL) |
| a | 12.0g Ca(OH)2 (过量) | 10.8g NH4Cl | 2688 |
| b | 10.8g (NH4)2SO4 | 2728 |
| c | 12.0g NaOH (过量) | 10.8g NH4Cl | 3136 |
| d | 10.8g (NH4)2SO4 | 3118 |
| e | 12.0g CaO (过量) | 10.8g NH4Cl | 3506 |
| f | 10.8g (NH4)2SO4 | 3584 |
分析表中数据,实验室制NH3产率最高的是:________(填序号),其它组合NH3产率不高的原因是:________.
步骤二.
模拟尾气的处理选用上述部分装置,按下列顺序连接成模拟尾气处理装置:
①A中反应的离子方程式:________.
②D装置作用有:使气体混合均匀、调节气流速度,还有一个作用是:________.
③D装置中的液体可换成________(填序号).
a.CuSO4溶液 b.H2O c.CCl4 d.浓H2SO4
④该同学所设计的模拟尾气处理实验还存在的明显缺陷是:________.
-
(16分)氮的氧化物(用NOx表示)是大气污染物,必须加以处理。
(1)汽车尾气中的CO、NOx采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。反应化学方程式可表示为:______________。
(2)工业尾气中氮的氧化物常采用氨催化吸收法,原理是NH3和NOx反应生成无毒的物质。某同学采用以下装置(见下图)和步骤模拟工业上氮的氧化物处理过程。
Ⅰ.提供的装置。
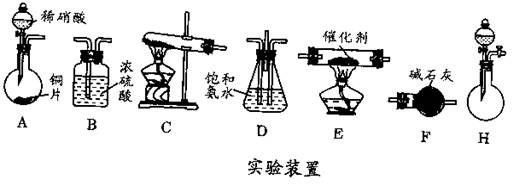
Ⅱ.NH3的制取。
①所提供的装置中能快速、简便制取NH3的装置是:__________(填仪器序号)。
②若采用C装置制取氨气(控制实验条件相同),情况如表所示。
实验记录
| 试剂组合序号 | 固体试剂/g | NH3体积/mL |
| a | 12.0g Ca(OH)2(过量) 10.8g NH4Cl | 2688 |
| b | 12.0g Ca (OH)2(过量) 10.8g(NH4)2SO4 | 2728 |
| c | 12.0g NaOH(过量) 10.8g NH4Cl | 3136 |
| d | 12.0g NaOH(过量) 10.8g (NH4)2SO4 | 3118 |
| e | 12.0g CaO(过量) 10.8g NH4Cl | 3506 |
| f | 12.0g CaO(过量) 10.8g (NH4)2SO4 | 3584 |
分析表中数据,实验室制NH3产率最高的是:___________________(填序号),其他组合NH3产率不高的原因是:____________。
Ⅲ.模拟尾气的处理。
选用上述部分装置,按下列顺序连接成模拟尾气处理装置:

①A中反应的离子方程式:_________。
②D装置作用除使气体混合均匀和调节气流速度以外,还有一个作用是_____________。
③D装置中的液体可换成_________(填序号)。
a.CuSO4溶液 b.H2O c.CCl4 d.浓H2SO4
④该同学所设计的模拟尾气处理实验还存在的明显缺陷是________________。
-
[物质结构与性质]
已知碳元素能形成多种金属碳化物,如碳化钙,俗称为电石。
(1)电石(CaC2)是用CaO与焦炭在电炉中加强热反应生成的,写出此反应的化学方程式 ,CaC2中含有化学键的类型为 ,C22-与N2互为等电子体,C22-的电子式可表示为 ,其中σ键和π键数目之比为 。
(2)已知MgO、CaO的熔点分别为2852℃、2614℃,分析熔点差异的原因是 。
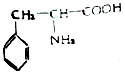
(3)苯丙氨酸是一种重要的氨基酸,其结构如图所示,分子中第一电离能最大的原子价电子排布式是 ,其中碳原子的杂化方式有 。
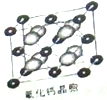
(4)已知CaF2晶体(如图,Ca2+处于面心)的密度为ρg/cm3,NA为阿伏加德常数,相邻的两个Ca2+的核间距为a cm,则CaF2的摩尔质量(M)可以表示为 g/mol。
-
I.为有效控制雾霾,各地积极采取措施改善大气质量。有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。热化学反应方程式为 2NO(g)+2CO(g) N2(g)+2CO2(g) △=-746.5kJ• mol-1,将1.0 mol NO和1.0 mol CO充入一个容积为10L的密闭容器中,反应过程中物质浓度变化如图所示。
N2(g)+2CO2(g) △=-746.5kJ• mol-1,将1.0 mol NO和1.0 mol CO充入一个容积为10L的密闭容器中,反应过程中物质浓度变化如图所示。
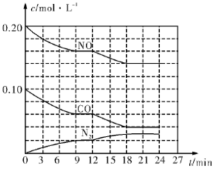
(1)CO在0〜9 min内的平均反应速率w(CO)= mol • L-1•min-1(保留两位有效数字);第12 min时改变的反应条件可能为 。
A.升高温度 B.减小压强 C.降低温度 D.加催化剂
(2)该反应在第24 min时已达到平衡状态,此时C02的体积分数为 (数值保留至小数点后一位),化学平衡常数K= (数值保留至小数点后一位)。
Ⅱ.能源的开发利用与人类社会的可持续发展息息相关。
(1)已知:Fe2O3(s)+3C(s) 2Fe(s)+3CO(g) △H1=a kJ • mol-1
2Fe(s)+3CO(g) △H1=a kJ • mol-1
CO(g) + O2 (g)
O2 (g) CO2 (g) △H2=ckJ• mol-1
CO2 (g) △H2=ckJ• mol-1
4Fe(s)+3O2(g) 2Fe2O3 (s) △H3=c kJ • mol-1
2Fe2O3 (s) △H3=c kJ • mol-1
则C的燃烧热△H=________kJ•mol-1。
(2)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是 (填序号)。
A.C(s )+CO2 (g)=2CO(g)
B.NaOH(aq) + HCl(aq)=NaCl(aq) +H2O(l)
C.2CO(g) +O2(g)=2CO2 (g )
D.2H2O(1 )=2H2(g)+O2(g )
(3 )若以熔融的K2CO3与CO2为反应的环境,依据所选反应设计成一个原电池, 请写出该原电池的负极反应: 。
-
碳和氮、硫是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,SO2会形成酸雨,目前,这些有毒有害气体的处理成为科学研究的重要内容。
(1)已知热化学方程式:
①2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H1
②C(s)+ O2(g)=CO2(g) △H2
③H2(g)+  O2(g)=H2O(l) △H3
O2(g)=H2O(l) △H3
则反应④2C(s)+H2(g)=C2H2(g)的△H 为_________________________。(用含△H1、△H2、△H3关系式表示)
(2)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g) N2+CO2(g) △H<0。在Tl℃时,反应进行到不同时间测得各物质的浓度(单位:mol/L)如下:
N2+CO2(g) △H<0。在Tl℃时,反应进行到不同时间测得各物质的浓度(单位:mol/L)如下:
| 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①10〜20min内,NO的平均反应速率v(NO)=___________,
②30min后,只改变某-条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是________(填字母编号)。
a.通入一定量的NO b.加入一定量的c
c.适当升高反应体系的温度 d.加入合适的催化剂
e.适当缩小容器的体积
③若保持与上述反应前30min的反应条件不变,起始时NO的浓度为2.50mol/L,则反应达平衡时c(NO)
=_________mol/L。NO的转化率______(填“增大”“减小”或“不变”)。
④下列说法中可以说明该反应已达到平衡状态的是_________。
a.体系内混合气体的密度保持不变 b.NO、N2、CO2、的物质的量之比为2∶1∶1
c.容器内气体的总压强保持不变 d. NO体积分数不再改变
(3)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图:

①该电池的负极反应:____________________;
②当甲中消耗2.24LO2(标准状况)时,乙中________ (填“a”或“b”)增重________g。
-
A、B、C、D均为中学化学常见的纯净物,它们之间有如下转化关系(某些生成物已略去)
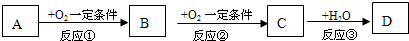
试回答:
(1)若A是非金属元素形成的化合物,且A与B、C在一定条件下都能反应生成一种无毒的气体.请写出下列化学方程式
①C→D______;②A和C反应______.
(2)若A是金属单质.
①向AlCl3溶液中滴加D的水溶液,能看到的现象是______,理由是(用离子方程式表示)______;
②继续向所得溶液中通入足量的CO2气体,可看到的现象是______,写出反应的离子方程式______.
-
A、B、C、D均为中学化学常见的纯净物,它们之间有如下转化关系(某些生成物已略去)
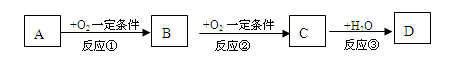 试回答:
试回答:
(1)若A是非金属元素形成的化合物,且A与B、C在一定条件下都能反应生成一种无毒的气体。请写出下列化学方程式
① C→D ________ ;
C→D ________ ;
②A和C反应 ________。
(2)若A是金属单质。
①向AlCl3溶液中滴加D的水溶液,能看到的现象是________,理
由是(用离子方程式表示)____________________________;
②继续向所得溶液中通入足量的CO2气体,可看到的现象是________,
写出反应的离子方程式。
-
A、B、C、D均为中学化学常见的纯净物,它们之间有如下转化关系(某些生成物已略去)
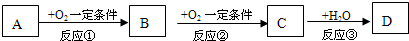
试回答:
(1)若A是非金属元素形成的化合物,且A与B、C在一定条件下都能反应生成一种无毒的气体.请写出下列化学方程式
①C→D______;②A和C反应______.
(2)若A是金属单质.
①向AlCl3溶液中滴加D的水溶液,能看到的现象是______,理由是(用离子方程式表示)______;
②继续向所得溶液中通入足量的CO2气体,可看到的现象是______,写出反应的离子方程式______.
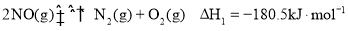
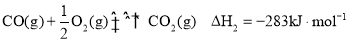
与
反应生成两种无毒气体的热化学方程式为_____________。
含量,某研究所的科研人员探究了
时等质量的三种催化剂对
还原
的催化效果(其他条件相同),所得结果如图所示:

的速率大小关系是___________。
、
,在催化剂Ⅰ的作用下达到如图所示平衡,则反应
在该温度下的平衡常数
______
。
转化率)与温度的关系图___________。

,其速率方程式为
(k为只与温度有关的速率常数),复杂反应(由几个基元反应构成)的速率取决于慢的基元反应。
,在温度低于
时是由两个基元反应构成的复杂反应,该反应的速率方程式为
,则其两个基元反应分别为:Ⅰ.______
______;Ⅱ.略,这两个反应中活化能较小的是__________。
时该反应的
、
生成
的速率
的关系如下:
______
。







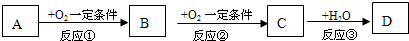
 试回答:
试回答: