-
Zn3(PO4)2·2H2O(溶于酸,难溶于水)是一种无毒害作用的防锈颜料,利用锌浮渣(主要含Zn、ZnO、ZnCl2,还含少量的铁、锰、铜、铅及砷的化合物等)制取Zn3(PO4)2·2H2O的工艺流程如图:

回答下列问题:
(1)“浸出”时,下列措施能提高锌的浸取率的是__(填字母)。
A.用浓硫酸代替稀硫酸 B.适当升高浸取液的温度
C.将“浸渣”再次浸取 D.缩短“浸出”时间
(2)“除锰”时,Mn2+发生反应的离子方程式为__(S2O 被还原为SO
被还原为SO )。
)。
(3)流程中除铁、砷时,当生成8.9gFeOOH和7.8gFeAsO4时,消耗H2O2__mol。
(4)“净化”时加锌粉的目的是__。
(5)“沉锌”时发生反应的化学方程式为__。
(6)“沉锌”至得到“产品”还需要经过的操作是__、洗涤、__。证明产品已洗涤干净的实验方法是__。
(7)Meyer等认为磷酸锌防腐机理是在钢铁表面形成组成近似为Zn2Fe(PO4)2·4H2O的覆盖膜,则在形成该覆盖膜的过程中,负极的电极反应式为__。
-
Zn3(PO4)2·2H2O(溶于酸,难溶于水)是一种无毒害作用的防锈颜料,利用锌浮渣(主要含Zn、ZnO、ZnCl2,还含少量的铁、锰、铜、铅及砷的化合物等)制取Zn3(PO4)2·2H2O的工艺流程如图:
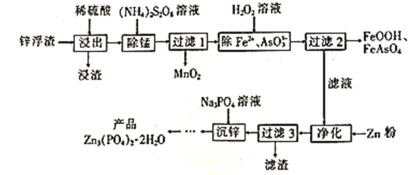
回答下列问题:
(1)“浸出”时,下列措施能提高锌的浸取率的是__(填字母)。
A.用浓硫酸代替稀硫酸 B.适当升高浸取液的温度
C.将“浸渣”再次浸取 D.缩短“浸出”时间
(2)“除锰”时,Mn2+发生反应的离子方程式为__(S2O 被还原为SO
被还原为SO )。
)。
(3)流程中除铁、砷时,当生成8.9gFeOOH和7.8gFeAsO4时,消耗H2O2__mol。
(4)“净化”时加锌粉的目的是__。
(5)“沉锌”时发生反应的化学方程式为__。
(6)“沉锌”至得到“产品”还需要经过的操作是__、洗涤、__。证明产品已洗涤干净的实验方法是__。
(7)Meyer等认为磷酸锌防腐机理是在钢铁表面形成组成近似为Zn2Fe(PO4)2·4H2O的覆盖膜,则在形成该覆盖膜的过程中,负极的电极反应式为__。
-
四水合磷酸锌[Zn3(PO4)2·4H2O],摩尔质量为457g·mol-1,难溶于水]是一种性能优良的绿色环保防锈颜料。实验室以锌灰(含ZnO、CuO、FeO、Fe2O3、SiO2等)为原料制备Zn3(PO4)2·4H2O的流程如图,回答下列问题:

已知:6NH4HCO3+3ZnSO4  ZnCO3·2Zn(OH)2·H2O↓+3(NH4)2SO4+5CO2↑
ZnCO3·2Zn(OH)2·H2O↓+3(NH4)2SO4+5CO2↑
(1)实验前需要将锌灰研磨成粉末状,原因是____。
(2)步骤I中需将溶液pH调至5.1,应选择的最佳试剂是___。(填字母)
a.NaOH b.ZnO c.Ba(OH)2
(3)步骤I滴加KMnO4溶液的目的是___。
(4)步骤Ⅱ中加入的a是___。
(5)步骤Ⅳ的化学方程式是___。
(6)步骤Ⅳ反应结束后得到Zn3(PO4)2·4H2O的操作包括___和干燥。
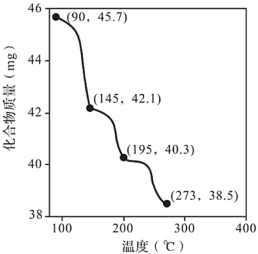
(7)称取45.7mgZn3(PO4)2·4H2O进行热重分析,化合物质量随温度的变化关系如图所示,为获得Zn3(PO4)2·2H2O和Zn3(PO4)2·H2O的混合产品,烘干时的温度范围为___。
-
硫酸铅(PbSO4)广泛应用于制造蓄电池、白色颜料等。利用锌冶炼过程中的铅浮渣生产PbSO4的流程如下:
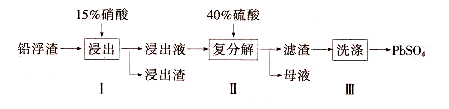
已知铅浮渣的主要成分是PbO、Pb,还含有少量Ag、Zn、CaO和其他不溶于硝酸的杂质。25℃时,Ksp(CaSO4)=4.9x10-5,Ksp(PbSO4)=1.6xl0-8。
(1)已知步骤I有NO气体产生,浸出液中含量最多的阳离子是Pb2+。分别写出PbO、Pb参加反应的化学方程式________。
(2)步骤I需控制硝酸的用量并使Pb稍有剩佘,目的是________。
(3)母液可循环利用于步骤I,其溶质主要是________(填一种物质化学式),若母液中残留的SO42-过多,循环利用时可能出现的问题是________。
(4)产品PbSO4还需用Pb(NO3)2溶液多次洗涤,目的是除去________。
(5)铅蓄电池的电解液是硫酸,充电后两个电极上沉积的PbSO4分别转化为PbO2和Pb,充电时阴极的电极反应式为________。
-
(16分)锌浮渣主要含Zn、ZnO、SiO2、Fe2+、Cd2+、Mn2+,工业上可通过控制条件逐一除去杂质以制备超细活性氧化锌,其工艺流程如下:
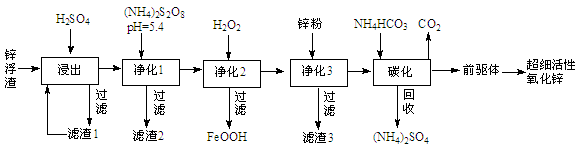
(1)锌浮渣利用硫酸浸出后,将滤渣1进行再次浸出,其目的是 。
(2)净化1是为了将Mn2+转化为MnO2而除去,试写出该反应的离子方程式 。
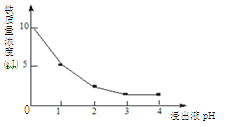
(3)90℃时,净化2溶液中残留铁的浓度受pH影响如图。pH值中等时,虽有利于Fe2+转化为Fe3+,但残留铁的浓度仍高于pH为3~4时的原因是 。
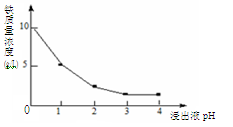
(4)滤渣3的主要成份为 (填化学式)。
(5)碳化在50℃进行,“前驱体”的化学式为ZnCO3•2Zn(OH)2•H2O,写出碳化过程生成“前驱体”的化学方程式 ;碳化时所用NH4HCO3的实际用量为理论用量的1.1倍,其原因一是为了使Zn2+充分沉淀,二是 。
-
(12分)锌浮渣主要含Zn、ZnO、SiO2、Fe2+、Cd2+、Mn2+,工业上可通过控制条件逐一除去杂质以制备超细活性氧化锌,其工艺流程如下:
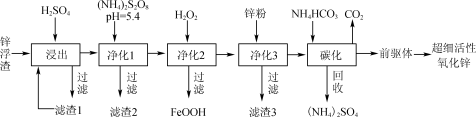
(1)锌浮渣利用硫酸浸出后,将滤渣1进行再次浸出,其目的是____。
(2)净化1是为了将Mn2+转化为MnO2而除去,写出该反应的离子方程式:____。
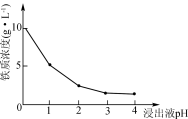
(3)90℃时,净化2溶液中残留铁的浓度受pH影响如右图所示。pH较小时,虽有利于Fe2+转化为Fe3+,但残留铁的浓度仍高于pH为3~4时的原因是____________________________。
(4)滤渣3的主要成分为________(填化学式)。
(5)碳化在50℃进行,“前驱体”的化学式为ZnCO3·2Zn(OH)2·H2O,写出碳化过程生成“前驱体”的化学方程式:____;碳化时所用NH4HCO3的实际用量为理论用量的1.1倍,其原因一是为了使Zn2+充分沉淀,二是____________。
-
锌浮渣主要含Zn、ZnO、SiO2、Fe2+、Cd2+、Mn2+,工业上可通过控制条件逐一除去杂质以制备超细活性氧化锌,其工艺流程如下:
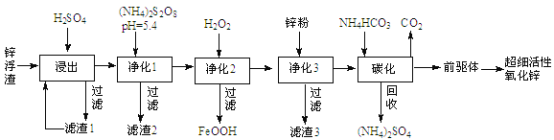
(1)锌浮渣利用硫酸浸出后,将滤渣1进行再次浸出,其目的是_________________。
(2)净化1是为了将Mn2+转化为MnO2而除去,试写出该反应的离子方程式__________。
(3)90℃时,净化2溶液中残留铁的浓度受pH影响如图。pH值中等时,虽有利于Fe2+转化为Fe3+,但残留铁的浓度仍高于pH为3~4时的原因是________________________。
(4)滤渣3的主要成份为___________(填化学式)。
(5)碳化在50℃进行,“前驱体”的化学式为ZnCO3•2Zn(OH)2•H2O,写出碳化过程生成“前驱体”的化学方程式___________________;碳化时所用NH4HCO3的实际用量为理论用量的1.1倍,其原因一是为了使Zn2+充分沉淀,二是_______________________。
-
Mn(H2PO4)2·2H2O是一种白色晶体,易溶于水,常用于机械设备的磷化处理。以软锰矿(主要成分为MnO2,还含有少量的Fe2O3、FeO和Al2O3)为原料制备Mn(H2PO4)2·2H2O的流程如图:
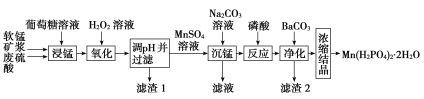
(1)软锰矿要先制成矿浆的目的是__,葡萄糖(C6H12O6)与MnO2反应时,产物为MnSO4、CO2和H2O,该反应中氧化剂与还原剂的物质的量之比为__。
(2)用H2O2溶液“氧化”时发生反应的离子方程式为:__。
(3)已知几种金属离子的氢氧化物开始沉淀和完全沉淀的pH如表,“调pH并过滤”时,应调整的pH范围为__,滤渣1的主要成分为__(填化学式)。
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.8 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
| Mn2+ | 7.8 | 9.8 |
(4)加入磷酸后发生反应的化学方程式为__。
(5)某工厂用上述流程制备Mn(H2PO4)2·2H2O,已知软锰矿中MnO2的含量为87%,整个流程中锰元素的损耗率为9%,则1吨该软锰矿可制得Mn(H2PO4)2·2H2O__t。
-
利用工业炼铅产生的锌灰(主要成分为ZnO、PbO、FeO、MnO2、CuO)可回收制备ZnCl2,工艺流程如下:
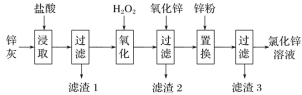
回答下列问题
(1)“浸取”实验中,反应体系的温度、反应时间对锰脱除效果的影响如下表,则适合的温度和反应时间分别是________、________。
表1 温度对锰脱除效果的影响
| 温度/℃ | ρ(Mn2+)/mg/L | 除锰率/% |
| 10 | 0.325 | 87.9 |
| 30 | 0.341 | 89.5 |
| 50 | 0.424 | 84.3 |
| 70 | 0.646 | 76.1 |
表2 反应时间对锰脱除效果的影响
| 时间/h | ρ(Mn2+)/mg/L | 除锰率/% |
| 1.0 | 0.995 | 63.1 |
| 1.5 | 0.794 | 70.6 |
| 2.0 | 0.328 | 87.9 |
| 2.5 | 0.325 | 87.9 |
(2)“滤渣1”的主要成分是________。
(3)H2O2溶液的作用是___________,已知“滤渣2”的主要成分是Fe(OH)3,则氧化锌的作用是____________。“置换”实验中发生反应的离子方程式有Zn+Pb2+=Pb+Zn2+、_________。
(4)由锌灰制取金属锌可采用碱溶解,然后电解浸取液,已知:ZnO溶于NaOH溶液中生成[Zn(OH)4]2−,则阴极的电极反应为____________________________________________。
(5)ZnCl2晶体溶解于饱和Na2CO3溶液中,得到6.46 g的碱式碳酸锌[Znx(CO3)y(OH)z],为了测定其组成,充分加热分解,产生的气体依次通入浓硫酸和碱石灰,质量分别增重了0.72g和0.88g,则该碱式碳酸锌的化学式为________________。
-
利用工业炼铅产生的锌灰(主要成分为ZnO、PbO、FeO、MnO2、CuO)可回收制备ZnCl2,工艺流程如下:

回答下列问题
(1)“浸取”实验中,反应体系的温度、反应时间对锰脱除效果的影响如下表,则适合的温度和反应时间分别是________________、____________________。

(2)“滤渣1”的主要成分是_____________。
(3)H2O2溶液的作用是____________________________________,已知“滤渣2”的主要成分是Fe(OH)3,则氧化锌的作用是_______________________________。“置换”实验中发生的反应的离子方程式有Zn+Pb2+=Ph+Zn2+、___________________________________。
(4)由锌灰制取金属锌可采用碱溶解,然后电解浸取液,已知:ZnO溶于NaOH溶液中生成[Zn(OH)4]2-,则阴极的电极反应为___________________________________。
(5)ZnCl2晶体溶解于饱和Na2CO3溶液中,得到6.46g的碱式碳酸锌[Znx(CO3)y(OH)z,为了测定其组成,充分加热分解,产生的气体依次通入浓硫酸和碱石灰,质量分别增重了0.72g和0.88g,则该碱式碳酸锌的化学式为______________________________。

被还原为SO
)。













