-
CCUS技术是将生产过程中排放的二氧化碳收集起来,进行提纯,继而加以合理利用的一项新技术。下列属于CCUS技术的是
A.将二氧化碳埋到地下,进行地质封存
B.用海水吸收CO2,形成碳酸钙永久沉积
C.二氧化碳通入盐碱湖里,生成矿物盐封存
D.用二氧化碳生产可降解的聚碳酸酯塑料
高二化学单选题简单题查看答案及解析
-
实验室制备乙酸乙酯的过程中,下列装置和操作不合理的是
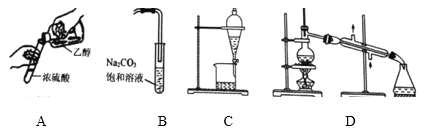
A. A为添加药品 B. B为收集粗产品
C. C为分离粗产品 D. D为提纯产品
高二化学单选题中等难度题查看答案及解析
-
你认为下列行为中有悖于“节能减排,和谐发展”这一主题的是( )
A. 将煤进行气化处理,提高煤的综合利用效率
B. 研究采煤、采油新技术,提高产量以满足工业生产的快速发展
C. 开发太阳能、水能、风能,可燃冰等新能源,减少使用煤、石油等化石燃料
D. 实现资源的“3R”利用观,即减少资源消耗,增加资源的重复使用、资源的循环再生
高二化学单选题简单题查看答案及解析
-
我国科学家成功研发了甲烷和二氧化碳的共转化技术,利用分子筛催化剂高效制得乙酸,下列有关说法正确的是( )
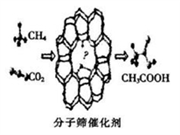
A. 消耗22.4 LCO2可制得1mol乙酸
B. 该反应过程符合“绿色化学”原理,其原子利用率为100%
C. 该反应属于取代反应
D. 反应物和生成物中均含有极性键和非极性键
高二化学选择题中等难度题查看答案及解析
-
金属腐蚀的本质是金属与其接触的其他物质在一定条件下发生氧化还原反应而受到损害。下列不属于化学或电化学防腐方法的是( )
A. 在金属表面涂刷一层油漆
B. 利用电镀技术在金属表面镀上一层其他金属
C. 用阳极氧化处理使铝表面形成致密的氧化物膜
D. 利用特殊工艺在钢铁表面生成一层致密的Fe3O4薄膜
高二化学选择题中等难度题查看答案及解析
-
燃煤技术的改进,有助于合理控制温室效应、环境污染,并能进行资源化利用,还可重新获得燃料或重要工业产品。工业上以煤和水为原料通过一系列转化变为清洁能源氢气和工业原料甲醇。
(1)若碳的燃烧热为393.5kJ·mol-1,氢气的燃烧热为285.8kJ·mol-1。已知反应
C(s)+2H2O(g)
CO2(g)+2H2(g) △H>0,能否求出该反应的△H_______(填“能”或“不能”)。若能则求出其△H(若不能请说明理由):_____________________。
(2)工业上也可以仅利用上述反应得到的CO2和H2进一步合成甲醇,反应方程式为:
CO2(g)+3H2(g)
CH3OH(g)+H2O(g) △H<0
①工业生产过程中CO2和H2的转化率________(填“前者大”、“后者大”、“一样大”或“无法判断”),为了提高甲醇的产率可以采取的措施是____________、____________(填两点)。
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2进行上述反应。测得CO2和CH3OH(g)浓度随时间变化如图所示。
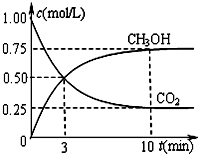
i.用H2表示0-3min内该反应的平均反应速率______________。
ii.该温度下的平衡常数为__________________。10 min后,保持温度不变,向该密闭容器中再充入1 mol CO2(g)和1 mol H2O(g),此时V正 _________V逆(填“>”、“<”或“=”)。
iii.对于基元反应aA+bB
cC+dD而言,其某一时刻的瞬时速率计算公式如下:正反应速率为V正=k正·c(A)a·c(B)b ;逆反应速率为V逆=k逆·c(C)c·c(D)d,其中k正、k逆为速率常数。若将上述反应视为基元反应则在上述条件下k逆∶k正=_________。反应进行到第3 min时V正 :V逆 =________。
高二化学填空题中等难度题查看答案及解析
-
合理利用资源,降低碳的排放,实施低碳经济是今后经济生活主流。
(1)科学家致力于二氧化碳的“组合转化”技术研究,如将H2和CO2以4∶1比例混合通入反应器,适当条件下反应可获得一种能源。完成以下化学方程式:4H2+CO2
________ +2H2O。
(2)汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO被CO还原的化学方程式:_______________。
(3)工业尾气中氮的氧化物常采用碱液吸收法处理。NO与NO2按物质的量之比1∶1被足量KOH溶液完全吸收后只得到一种钾盐,该钾盐的化学式是______________。
(4)CO2合成生产燃料甲醇(CH3OH)是碳减排的新方向。进行如下实验:某温度下在1 L的密闭容器中,充2 mol CO2和6 mol H2,发生:CO2(g)+3H2(g )
CH3OH(g)+H2O(g)。
①能判断该反应已达化学反应限度标志的是______________ (填字母)。
a.CO2百分含量保持不变
b.容器中H2浓度与CO2浓度之比为3:1
c.混合气体的平均相对分子质量保持不变
d.容器中混合气体的质量保持不变
②现测得CO2和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,氢气的平均反应速率v (H2)=______ mol/(L • min),容器中起始的压强与平衡时的压强之比为___________。
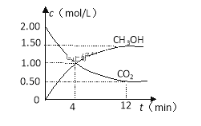
高二化学综合题中等难度题查看答案及解析
-
《可再生能源法》倡导碳资源的高效转化及循环利用。下列做法与上述理念相违背的是
A. 加快石油等化石燃料的开采和使用 B. 大力发展煤的气化及液化技术
C. 以CO2 为原料生产可降解塑料 D. 将秸秆进行加工转化为乙醇燃料
高二化学单选题中等难度题查看答案及解析
-
海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是__________(填物理变化、化学变化);
(2)实验室用MnO2和浓盐酸为原料制备氯气,该反应的化学方程式为________________________________,其中氧化剂是_______还原剂是________。尾气处理的离子方程式为______________________________。
(3)工业上制备漂白粉的化学方程式___________________________________。
(4)将实验室制的氯气配成新制的氯水含有多种微粒,试用方程式或化学式回答下列问题:
将氯水滴加紫色石蕊溶液中,先变红后褪色______________________________(化学方程式)其中,变红后褪色是因为有_________(化学式)生成具有漂白性;
将氯水滴入硝酸银溶液中,有白色沉淀生成__________________________。(离子方程式)
高二化学填空题中等难度题查看答案及解析
-
化学与社会、科学、技术环境密切相关,下列说法不正确的是
A. 高纯度的硅单质广泛用作半导体材料
B. 工业上利用情性电极电解熔融的MgO来制取Mg
C. 合理利用太阳能、风能和氢能等能源有利于实现“低碳经济”
D. 钢铁在潮湿的空气中容易生锈,其主要原因是形成了原电池
高二化学单选题简单题查看答案及解析