-
铁及其化合物用途非常广泛。
(1)已知赤铁矿还原冶炼时是逐级进行的,已知:
(a) 3Fe2O3(s)+CO(g)  2Fe3O4(s)+CO2(g)
2Fe3O4(s)+CO2(g)  H = a kJ·mol-1
H = a kJ·mol-1
(b) Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)  H =b kJ·mol-1
H =b kJ·mol-1
(c) Fe3O4(s)+CO(g)  3FeO(s)+CO2 (g)
3FeO(s)+CO2 (g)  H = c kJ·mol-1
H = c kJ·mol-1
①上述反应(a)平衡常数表达式为K=___________________。
②反应FeO(s)+CO(g)  Fe(s)+CO2(g)
Fe(s)+CO2(g)  H =__________kJ·mol-1(用含a、b、c的代数式表示)。
H =__________kJ·mol-1(用含a、b、c的代数式表示)。
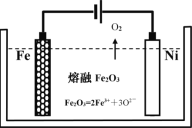
(2)用类似冶炼铝的方法, 在600~1000℃时电解熔融的Fe2O3冶炼铁(装置示意图如图),该法除消耗能量较少外,另一最突出的优点是__________________________________;电解时阳极发生的电极反应为____________。
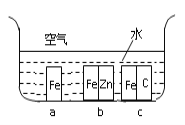
(3)生铁在自然界中可发生析氢腐蚀和吸氧腐蚀,析氢腐蚀的负极的电极反应式为_________;如图所示,纯铁处于a、b、c三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填字母)_____________。
-
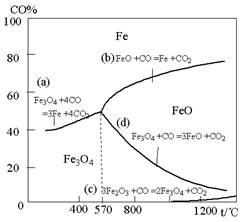
(14分)钢铁工业在我国国民经济中处于十分重要的位置,工业上采用高炉冶炼,常用赤铁矿、焦炭、空气和熔剂(石灰石)作原料。已知赤铁矿被还原剂还原时是逐级进行的,还原时温度及CO、CO2平衡混合气体中CO的体积分数的关系如下图:
(1)铁在元素周期表中位于________________________周期________________________族
(2)在温度低于570℃时,还原分两阶段完成,在温度高于570℃时,依次发生的还原反应有:________________(选用右图中的a、b、c、d填空)
(3)为减少高炉冶铁时,含CO的尾气排放,下列研究方向不可取的是________________________。
(a)其它条件不变,增加高炉的高度
(b)调节还原时的炉温
(c)增加原料中焦炭与赤铁矿的比例
(d)将生成的铁水及时移出
(4)已知下列反应数值:
| 反应序号 | 化学反应 | 反应热 |
| ① | Fe2O3(s)+3CO(g)=2Fe(s)+3CO 2(g) | △H1= -26.7kJ·mol-1 |
| ② | 3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) | △H2= -50.8kJ·mol-1 |
| ③ | Fe3O4(s)+CO(g)=3FeO(s)+CO2 (g) | △H3= -36.5kJ·mol-1 |
| ④ | FeO(s)+CO(g)=Fe(s)+CO2(g) | △H4 |
反应④△H4= kJ·mol-1。
-
化学反应原理在科研和生产中有广泛应用。
(1)已知:3Fe2O3(s)+CO(g)=2Fe3O4(s)+4CO2(g) △H1=-47kJ/mol;
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) △H2=-14kJ/mol。
则Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=________。
(2)煤化工行业中常常通过研究不同温度下反应的平衡常数来解决各种实际问题。将等体积的CO和H2O(g)通入一恒容密闭容器中,发生反应:CO(g)+H2O(g) H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表所示。
H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表所示。
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
① 该反应的平衡常数表达式K=_______,该反应的正反应是_______(填“吸热”或“放热”)反应。
② 若反应在800℃时进行, CO和H2O(g)的起始浓度均为0.020 mol·L-1,则该条件下,CO的平衡转化率为_________。
③ 下列措施中能够提高CO转化率的是______(填字母)
a.降低温度 b.加入催化剂 c.增加CO的浓度 d.加入H2O(g)
-
工业上铁的冶炼是在炼铁高炉中进行的,发生的反应是Fe2O3+3CO=2Fe+3CO2,对于该反应,下列说法正确的是( )
A.该反应是置换反应
B.氧元素的化合价降低
C.Fe2O3发生还原反应
D.CO为氧化剂
-
氧化还原反应在生产、生活中应用广泛。下列反应不属于氧化还原反应的是
A.木炭燃烧:C+O2 CO2
CO2
B.煅烧石灰石:CaCO3 CaO+CO2↑
CaO+CO2↑
C.铁的冶炼:Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
D.电解水:2H2O 2H2↑+O2↑
2H2↑+O2↑
-
铝是一种极为常见而且用途广泛的金属,工业上冶炼铝常用的方法是( )
A.用CO还原
B.铝热法
C.电解法
D.加热分解法
-
铝是一种极为常见而且用途广泛的金属,工业上冶炼铝常用的方法是
A.用CO还原 B.铝热法 C.电解法 D.加热分解法
-
铜的化合物用途非常广泛。已知下列反应:[Cu(NH3)2]++NH3+CO ⇌ [Cu(NH3)3CO]+,2CH3COOH +2CH2=CH2+O2 2CH3COOCH=CH2+2H2O。
2CH3COOCH=CH2+2H2O。
(1)Cu2+基态核外电子排布式为______。
(2)NH3分子空间构型为_______, 其中心原子的杂化类型是______。
(3)CH3COOCH=CH2分子中碳原子轨道的杂化类型是_______,1mol CH3COOCH=CH2中含 键数目为_____。
键数目为_____。
(4)CH3COOH可与H2O混溶,除因为它们都是极性分子外,还因为__________。
(5)配离子[Cu(NH3)3CO]+中NH3及CO中的C与Cu(Ⅰ)形成配位键。不考虑空间构型,[Cu(NH3)3CO]+的结构示意图表示为____
-
(8分)已知:(1)Fe2O3(s) + 3CO(g) == 2Fe(s) + 3CO2(g) △H1= -26.7 kJ/mol
(2)3Fe2O3(s) + CO(g) == 2Fe3O4(s) + CO2(g) △H2= -50.75 kJ/mol
(3) Fe3O4(s) + CO(g) == 3FeO(s) + CO2(g) △H3= -36.5 kJ/mol
计算反应:2FeO(s) + 2CO(g) == 2Fe(s) + 2CO2(g)的△H(要有计算过程)。
-
已知下列热化学方程式:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= —24.8 kJ·mol-1;3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2kJ·mol-1 ;Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +19.4kJ·mol-1则14g CO气体与足量FeO充分反应得到Fe单质和CO2气体时的释放或吸收的热量为
A. 放出11 kJ B. 放出5.5kJ C. 吸收11 kJ D. 吸收5.5 kJ
2Fe3O4(s)+CO2(g)
H = a kJ·mol-1
2Fe(s)+3CO2(g)
H =b kJ·mol-1
3FeO(s)+CO2 (g)
H = c kJ·mol-1
Fe(s)+CO2(g)
H =__________kJ·mol-1(用含a、b、c的代数式表示)。


