-
已知:2H2(g)+O2(g)=2H2O(g);ΔH=-270kJ·mol-1,下列说法错误的是
A.2mol水蒸气分解成2mol氢气与1mol氧气吸收270kJ热量
B.2mol氢气与1mol氧气反应生成2mol液态水放出热量大于270kJ
C.在相同条件下,2mol氢气与1mol氧气的能量总和大于2mol水蒸汽的能量
D.2个氢气分子与1个氧气分子反应生成2个水蒸汽分子放出270kJ热量
-
已知:2H2(g)+O2(g)=2H2O(g);ΔH=-270kJ·mol-1,下列说法错误的是
A.2mol水蒸气分解成2mol氢气与1mol氧气吸收270kJ热量
B.2mol氢气与1mol氧气反应生成2mol液态水放出热量大于270kJ
C.在相同条件下,2mol氢气与1mol氧气的能量总和大于2mol水蒸汽的能量
D.2个氢气分子与1个氧气分子反应生成2个水蒸汽分子放出270kJ热量
-
下列热化学方程式及其有关叙述正确的是( )
A.氢气的燃烧热为285.8kJ·mol-1,则水分解的热化学方程式为2H2O(l)=2H2(g)+O2(g) ΔH =+571.6kJ·mol-1
B.已知2C(石墨,s)+O2(g)=2CO(g) ΔH =+221kJ·mol-1,则石墨的燃烧热110.5kJ·mol-1
C.已知N2(g)+3H2(g)  2NH3(g) ΔH=-92.4kJ·mol-1,则在一定条件下将1mol N2和3mol H2置于一密闭容器中充分反应,放出92.4kJ的热量
2NH3(g) ΔH=-92.4kJ·mol-1,则在一定条件下将1mol N2和3mol H2置于一密闭容器中充分反应,放出92.4kJ的热量
D.已知乙炔的燃烧热为 ,则表示乙炔燃烧热的热化学方程式为
,则表示乙炔燃烧热的热化学方程式为 ΔH=
ΔH=
-
下列说法或表示方法中正确的是( )
A. 等质量的硫蒸气和硫黄分别完全燃烧,后者放出的热量多
B. 氢气的燃烧热为285.5 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)ΔH=-285.5 kJ/mol
C. Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l) ΔH<0
D. 已知中和热为57.3 kJ/mol,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量要大于57.3 kJ
-
下列说法或表示方法中正确的是( )
A.等质量的硫蒸气和硫黄分别完全燃烧,后者放出的热量多
B.氢气的标准燃烧热为285.8kJ•mol-1,则氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l) △H=+285.8kJ•mol-1
C.Ba(OH)2•8H2O(s)+2NH4Cl(s)═BaCl2(s)+2NH3(g)+10H2O(l) △H<0
D.已知中和反应的反应热△H=﹣57.3kJ•mol-1,若将含0.5molH2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量要大于57.3kJ
-
下列说法或表示方法中正确的是( )
A.等质量的硫蒸气和硫磺分别完全燃烧,后者放出的热量多
B.氢气的燃烧热为285.8kJ ·  ,则氢气燃烧的热化学方程式为
,则氢气燃烧的热化学方程式为
2H2(g)+O2(g)=2H2O(l);△H=-285.8 kJ· 
C.Ba(OH)2 · 8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l);△H<0
D.某酸溶液可以与石灰石反应放出CO2,则该酸不一定为强酸。
-
下列说法或表示方法中正确的是( )
A.等质量的硫蒸气和硫磺分别完全燃烧,后者放出的热量多
B.氢气的燃烧热为285.8kJ ·  ,则氢气燃烧的热化学方程式为
,则氢气燃烧的热化学方程式为
2H2(g)+O2(g)=2H2O(l);△H=-285.8 kJ· 
C.Ba(OH)2 · 8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l);△H<0
D.某酸溶液可以与石灰石反应放出CO2,则该酸不一定为强酸。
-
下列说法或表示方法中正确的是
A. 等质量的硫蒸气和硫黄分别完全燃烧,后者放出的热量多
B. 氢气的燃烧热为285.8 kJ·mol-1,则氢气燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(l) ∆H=-285.8 kJ·mol-1
C. Ba(OH)2·8H2O(s)+2NH4Cl(s) = BaCl2(s)+2NH3(g)+10H2O(l) ∆H<0
D. 已知中和热为57.3 kJ·mol-1,若将含0.5mol H2SO4的浓溶液与含1mol NaOH的溶液混合,放出的热量大于57.3 kJ
-
下列说法或表示方法中正确的是
A.等质量的硫蒸气和硫黄分别完全燃烧,后者放出的热量多
B.氢气的燃烧热为285.8 kJ·mol-1,则氢气燃烧的热化学方程式为
2H2(g)+O2(g)=2H2O(l) ∆H=-285.8 kJ·mol-1
C.Ba(OH)2·8H2O(s)+2NH4Cl(s) = BaCl2(s)+2NH3(g)+10H2O(l) ∆H<0
D.已知中和热为57.3 kJ·mol-1,若将含0.5mol H2SO4的浓溶液与含1mol NaOH的溶液混合,放出的热量大于57.3 kJ
-
据报道,某国一集团拟在太空建造巨大的集光装置,把太阳光变成激光用于分解海水制氢:2H2O==== 2H2↑+O2↑ ,下列说法中正确的是
A. 水的分解反应是放热反应
B. 氢气是一级能源
C. 使用氢气作燃料有助于控制温室效应
D. 此反应的目的是用生成的氢气与空气中多余的CO2反应生成甲醇储存起来,改善生存环境
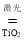 2H2(g)+O2(g)。
2H2(g)+O2(g)。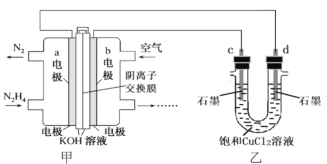
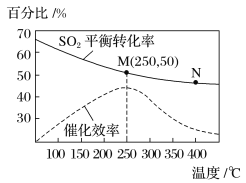
 2CO2(g)+S(g) ΔH,测得温度对SO2的转化率及催化剂效率的影响如图所示:
2CO2(g)+S(g) ΔH,测得温度对SO2的转化率及催化剂效率的影响如图所示: