-
25.(12分)发展储氢技术是氢氧燃料电池推广应用的关键。研究表明液氨是一种良好的储氢物质,其储氢容量可达17.6% (质量分数)。液氨气化后分解产生的氢气可作为燃料供给氢氧燃料电池。氨气分解反应的热化学方程式如下:
2NH3(g)  N2 (g) + 3H2(g) ΔH = +92.4 kJ·mol-1
N2 (g) + 3H2(g) ΔH = +92.4 kJ·mol-1
请回答下列问题:
(1) 氨气自发分解的反应条件是 。(填“高温”、“低温”或“任何条件下”)
(2) 已知:2H2(g)+O2(g)=2H2O(g) ΔH = - 483.6 kJ·mol-1
NH3(l) NH3(g) ΔH = +23.4 kJ·mol-1
NH3(g) ΔH = +23.4 kJ·mol-1
则,反应4NH3(l)+3O2(g)=2N2(g)+6H2O(g)的ΔH = 。
(3) 研究表明金属催化剂可加速氨气的分解。图1为某温度下等质量的不同金属分别催化等浓度氨气分解生成氢气的初始速率。
①不同催化剂存在下,氨气分解反应的活化能最大的是 (填写催化剂的化学式)。
②恒温(T1)恒容时,用Ni催化分解初始浓度为c0的氨气,并实时监测分解过程中氨气的浓度。计算后得氨气的转化率α(NH3)随时间t变化的关系曲线(见图2)。请在图2中画出:在温度为T1,Ru催化分解初始浓度为c0的氨气过程中α(NH3) 随t变化的总趋势曲线(标注Ru-T1)。
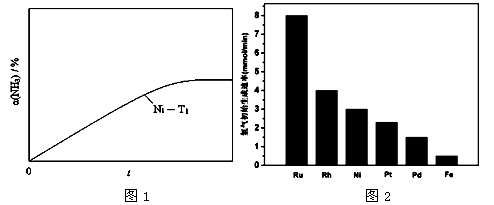
③如果将反应温度提高到T2,请在图2中再添加一条Ru催化分解初始浓度为c0的氨气过程中α(NH3) ~ t的总趋势曲线(标注Ru-T2)
(4) 用Pt电极对液氨进行电解也可产生H2和N2。阴极的电极反应式是 。
(已知:液氨中2NH3(l)  NH2- + NH4+)
NH2- + NH4+)
-
合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一。在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学反应方程式(HAc表示醋酸): Cu(NH3)2Ac+CO+NH3==Cu(NH3)3 (CO) Ac。
请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为________。
(2)配合物Cu(NH3)3 (CO) Ac中心原子的配位数为________,基态铜原子核外电子排布式为_________________。
(3)写出与CO互为等电子体的粒子________ (任写一个) 。
(4)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中,C原子轨道的杂化类型为________;1 mol尿素分子中,σ键的个数为____________。(设NA为阿伏加德罗常数的值)
(5)铜金合金形成的晶胞如图所示,其中Cu、Au原子个数比为________。铜单质晶胞与铜金合金的晶胞相似,晶胞边长为3.61×10-8cm,则铜的密度为________g/cm-3(结果保留3位有效数字)。

-
合成氨是人类科学技术发展史上的一项重大突破,2018年是合成氨工业先驱哈伯(P·Haber)获得诺贝尔奖100周年
(1)合成氨反应是一个可逆反应:N2(g)+3H2(g) 2NH3(g),已知298K时:ΔH=-92.2kJ/mol,ΔS=-198.2J/(K·mol),则根据正反应的焓变和熵变分析,常温下合成氨反应____(填“能”或“不能”)自发进行。实验研究表明,在特定条件下,合成氨反应的速率与参加反应的物质的浓度的关系式如下,v=kc(N2)c1.5(H2)c-1(NH3),k为速率常数,请根据该关系式分析,如果想增大合成氨反应的速率,从浓度的角度可以采用的措施为________。根据合成氨反应的特点,请再说出一项能够提高合成氨反应速率的措施_________。
2NH3(g),已知298K时:ΔH=-92.2kJ/mol,ΔS=-198.2J/(K·mol),则根据正反应的焓变和熵变分析,常温下合成氨反应____(填“能”或“不能”)自发进行。实验研究表明,在特定条件下,合成氨反应的速率与参加反应的物质的浓度的关系式如下,v=kc(N2)c1.5(H2)c-1(NH3),k为速率常数,请根据该关系式分析,如果想增大合成氨反应的速率,从浓度的角度可以采用的措施为________。根据合成氨反应的特点,请再说出一项能够提高合成氨反应速率的措施_________。
(2)研究表明,在Fe催化剂作用下合成氨的反应历程为(*表示吸附态):
化学吸附:N2(g)→2N*;H2(g)→2H*;
表面反应:N*+H* NH*;NH*+H*
NH*;NH*+H* NH2*;NH2*+H*
NH2*;NH2*+H* NH3*
NH3*
脱 附:NH3* NH3(g)
NH3(g)
其中,N2的吸附分解反应速率慢,解决了合成氨的整体反应速率。
实际生产中,合成氨常用工艺条件:Fe作催化剂,控制温度773K,压强3.0×107Pa,原料中N2和H2物质的量之比为1:2.8。请回答:
①分析说明原料中N2过量的理由____________。
②近年来,中国科学院大连化学物理研究所陈平研究团队经过近二十年的积累,先后在催化剂分解、催化氨合成、化学链合成氨等方面取得重要进展。关于合成氨工艺的下列理解,正确的是______。
A.人们对合成氨研究的重要目的之一是要实现氨的低温高效合成
B.控制温度(773K)远于室温,是为了保证尽可能高的平衡转化率和快的反应速率
C.陈平团队首次报道了具有优异低温活性的LiH-3d过渡金属这一复合催化剂体系,它可以大大提高反应的平衡转化率
D.N2的吸附分解反应活化能高,是合成氨反应条件苛刻的重要原因
E.陈平团队构建了一条基于可再生能源的化学链合成氨工艺流程,可以显著提高能效
(3)若N2和H2生成NH3的反应为: N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g),的标准平衡常数
NH3(g),的标准平衡常数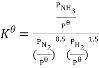 ,其中
,其中 为标准大气压(1×105Pa),
为标准大气压(1×105Pa), 、
、 和
和 为各组分的平衡分压,如P(NH3)=x(NH3) P,P为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。
为各组分的平衡分压,如P(NH3)=x(NH3) P,P为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。
①N2和H2起始物质的量之比为1:3,反应在恒定温度和标准压强下进行,NH3的平衡产率为 ,则
,则 _________(用含
_________(用含 的最简式表示)
的最简式表示)
②根据合成氨反应的特点,标准平衡常数 随温度T升高而逐渐______(填“增大”或“减小”)。
随温度T升高而逐渐______(填“增大”或“减小”)。
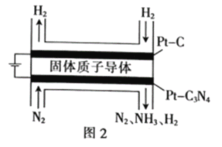
(4)希腊两位科学家曾经采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶体薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图)。钯电极A为______极(填“阴”或“阳”),该极上的电极反应式是___________。
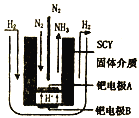
-
合成氨是人类科学技术发展史上的一项重大突破.合成氨反应的化学方程式为N2(g)+3H 2(g)==2NH3(g).一定条件下,在容积固定的密闭容器中反应达平衡后,请回答
(1)若增大N2 的浓度,则化学反应速率_______(填“增大”或“减小”),化学平衡______(填“向正反应方向”、“向逆反应方向”或“不”)移动.
(2)若加入适当的催化剂,则化学反应速率_______(填“增大”或“减小”),化学平衡_____(填“向正反应方向”、“向逆反应方向”或“不”)移动.
(3)若增大NH3 的浓度,则化学反应速率_______(填“增大”或“减小”),化学平衡_______(填“向正反应方向”、“向逆反应方向”或“不”)移动.
-
材料是人类赖以生存和发展的重要物质基础。请回答下列问题:
(1)有机合成材料的出现是材料发展史上的一次重大突破。人们常说的三大合成材料是指__________________、__________________、__________________。
(2)聚氯乙烯的商品名为PVC,其结构简式为____________________,PVC管材中还需要加入具有特殊用途的添加剂,如_______________、________________等,因为PVC具有_____________性,所以由它制得的材料可反复加工、多次使用。
(3)合金是生活中常见的材料,某合金具有密度小、强度高的优良性能,常用于制造门窗框架,该合金中含量最高的金属为_______(填元素符号),该元素在周期表中的位置为______________________________。
(4)玻璃是一种常见的硅酸盐材料,制备普通玻璃的原料有CaCO3、_______和_______。
-
材料是人类赖以生存和发展的重要物质基础,而化学是材料科学发展的基础。材料种类很多,通常可分为金属材料、无机非金属材料(包括硅酸盐材料)、高分子合成材料及复合材料。
(1)钢轨、手术刀、防盗门属于上述材料中的______________。
(2)生活中的玻璃、陶瓷、水泥属于上述材料中的_________,其生产原料不需要使用石灰石的是________________。
(3)我国宇航员身着我国自主研发的宇航服步入太空。据报道,宇航服头盔的主要成分是无色透明、坚韧如钢的工程塑料——聚碳酸酯,该材料属于____________。
(4)很多金属材料因受到腐蚀而造成巨大的经济损失。如钢铁的腐蚀,主要是钢铁在潮湿空气里,铁和碳构成许多微小的___________而受到腐蚀。
(5)写出钢铁发生电化学腐蚀的负极的电极反应式_________________。
-
(10分)材料是人类赖以生存的重要基础物质,而化学是材料科学发展的基础。材料种类很多,通常可分为金属材料、无机非金属材料(包括硅酸盐材料)、高分子合成材料及复合材料。
(1)生活中的玻璃、陶瓷、水泥属于上述材料中的________________,其生产原料不需要使用石灰石的是_____________。塑料制品给人类生活带来很多方便,但塑料制品造成的“白色污染”已成为社会的一大公害。请你提出一项防治“白色污染”的有效措施:
(2)我们常说的三大合成材料是指:塑料、合成纤维和
(3)金属腐蚀会造成巨大的经济损失,钢铁在潮湿的空气中更容易被腐蚀,主要原因是钢铁里的铁和碳构成许多微小的 发生电化学腐蚀。
-
材料是人类赖以生存的重要物质基础,而化学是材料科学发展的基础.材料种类很多,通常可分为金属材料、无机非金属材料(包括硅酸盐材料)、高分子合成材料及复合材料.生活中的玻璃、陶瓷、水泥属于上述材料中的______,其生产原料不需要使用石灰石的是______.塑料制品给人类生活带来很多方便,但塑料制品造成的“白色污染”已成为社会的一大公害,请你提出一项治理“白色污染”的有效措施:______.金属腐蚀会造成巨大的经济损失,钢铁在潮湿的空气中更容易被腐蚀,主要原因是钢铁里的铁和碳构成许多微小的______,发生电化学腐蚀.
-
合成氨是人类科学技术上的一项重大突破,其反应原理为: △H=-92.4kJ·L-1,一种工业合成氨的简易流程图如下:
△H=-92.4kJ·L-1,一种工业合成氨的简易流程图如下:
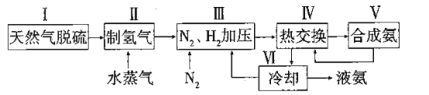
(1)步骤II中制氯气原理如下:
I. △H=+206.4kJ·L-1
△H=+206.4kJ·L-1
II. △H=-41.2kJ·L-1
△H=-41.2kJ·L-1
①对于反应I,一定可以提高平衡体系中H2百分含量,又能加快反应速率的是____________________。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
②利用反应II,将CO进一步转化,可提高H2产量。若1mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18molCO、CO2和H2的混合气体,则CO转化率为_______________。
(2)图1表示500℃、60.0Mpa条件下,原料气投料比平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:________。
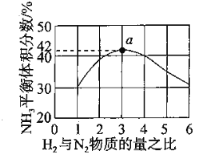
(3)上述流程图中,使合成氨气放出的能量得到充分利用的主要步骤是(填序号)________。简述本流程中提高合成氨原料总转化率的方法:_______________。
-
合成氨是人类科学技术上的一项重大突破,其反应原理为:N2 (g) + 3H2 (g)  2NH3 (g) △H = -92.4 kJ·mol-1 , 一种工业合成氨的简易流程图如下:
2NH3 (g) △H = -92.4 kJ·mol-1 , 一种工业合成氨的简易流程图如下:
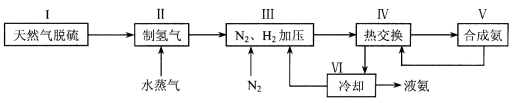
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式 。
(2)步骤Ⅱ中制氢气原理如下:
① CH4 (g) + H2O (g)  CO (g) + 3H2 (g) △H = +206.4 kJ·mol-1
CO (g) + 3H2 (g) △H = +206.4 kJ·mol-1
② CO (g) + H2O (g)  CO2 (g) + H2 (g) △H = -41.2 kJ·mol-1
CO2 (g) + H2 (g) △H = -41.2 kJ·mol-1
写出氢气和二氧化碳气体反应生成甲烷和水蒸气的热化学方程式 。
对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是 。
a.升高温度 b.增大水蒸气浓度
c.加入催化剂 d.降低压强
(3)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号) 。
(4)用氨气制取尿素[CO(NH2)2]的反应为:
2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g) ΔH<0
CO(NH2)2(l)+H2O(g) ΔH<0
某温度下,向容积为100L的密闭容器中通入4mol NH3和2molCO2,该反应进行到40 s时达到平衡,此时CO2的转化率为50%。若保持其它条件不变情况下,请在图中用实线画出使用催化剂时该反应(0~70s)的进程曲线。

(5)25℃时,向a mol NH4NO3固体中滴加b L氨水后溶液恰好呈中性,所滴加氨水的浓度为 mol·L-1(25℃时,NH3·H2O的电离平衡常数Kb=2×10-5)
 N2(g)+3H2(g)的化学平衡常数Kp=_____。 (用平衡分压代替平衡浓度计算,气体分压p分=气体总压p总×体积分数)
N2(g)+3H2(g)的化学平衡常数Kp=_____。 (用平衡分压代替平衡浓度计算,气体分压p分=气体总压p总×体积分数)


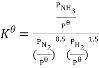 ,其中
,其中



