-
将过量的0.2g铜粉与5mL1 mol•L‾1FeCl3溶液混合,充分振荡,溶液棕黄色变浅,溶液变绿,有灰白色固体出现。通过查阅资料,初步认为灰白色固体可能含CuCl(CuCl白色晶体,不溶于水、硫酸、稀硝酸,溶于氨水、浓盐酸溶液中,生成络合物)。为进一步探究灰白色固体是否含CuCl,进行一系列实验。已知:① CuCl+2NH3•H2O [Cu(NH3)2]++Cl‾+2H2O(无色溶液)② 提供的试剂:稀HNO3、AgNO3溶液、氨水、KSCN溶液
[Cu(NH3)2]++Cl‾+2H2O(无色溶液)② 提供的试剂:稀HNO3、AgNO3溶液、氨水、KSCN溶液
请回答下列问题:
(1)生成CuCl的化学方程式____________________________________。
(2)下列为常见的分离装置(装置中的其他仪器忽略),从上述溶液中分离出固体混合物,应选用的相应装置中的仪器名称是_______________。
A.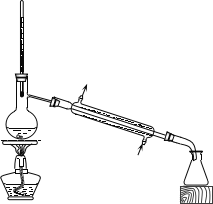 B.
B. 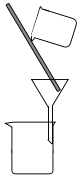 C.
C. D.
D.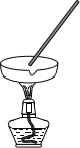 E.
E. F.
F.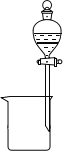
(3)提纯灰白色固体:将固体混合物用蒸馏水洗涤以除去固体表面的Fe3+、Cl‾。为检验固体混合物是否洗涤干净,最佳方案是检验洗涤液中是否含有_______(填离子符号),理由是_____________________________________________。
(4)设计实验检验得到的灰白色固体中含有CuCl,该实验过程中用到的试剂为____________________。
(5)实验测得灰白色固体混合物质量为a g,其中CuCl b g。上述实验过程中还有CuCl2生成,则生成CuCl2的物质的量是____________(列出计算式即可)。
-
向硝酸酸化的2 mL 0.1 mol·L-1 AgNO3溶液(pH=2)中加入过量铁粉,振荡后静置,溶液先呈浅绿色,后逐渐呈棕黄色,试管底部仍存在黑色固体,过程中无气体生成。实验小组同学针对该实验现象进行了如下探究。
Ⅰ.探究Fe2+产生的原因。
(1)提出猜想:Fe2+可能是Fe与________或________反应的产物。(均填化学式)
(2)实验探究:在两支试管中分别加入与上述实验等量的铁粉,再加入不同的液体试剂,5 min后取上层清液,分别加入相同体积和浓度的铁氰化钾溶液。
| 液体试剂 | 加入铁氰化 |
| 钾溶液 | | |
| 1号试管 | 2 mL 0.1 mol·L-1 | |
| AgNO3溶液 | 无蓝色沉淀 | |
| 2号试管 | 硝酸酸化的2 mL 0.1 mol·L-1______溶液(pH=2) | 蓝色沉淀 |
①2号试管中所用的试剂为_________。
②资料显示:该温度下,0.1 mol·L-1 AgNO3溶液可以将Fe氧化为Fe2+。但1号试管中未观察到蓝色沉淀的原因可能为_______。
③小组同学继续进行实验,证明了由2号试管得出的结论正确。实验如下:取100 mL 0.1 mol·L-1硝酸酸化的AgNO3溶液(pH=2),加入铁粉并搅拌,分别插入pH传感器和NO 传感器(传感器可检测离子浓度),得到图甲、图乙,其中pH传感器测得的图示为________(填“图甲”或“图乙”)。
传感器(传感器可检测离子浓度),得到图甲、图乙,其中pH传感器测得的图示为________(填“图甲”或“图乙”)。

④实验测得2号试管中有NH4+生成,则2号试管中发生反应的离子方程式为__________。
Ⅱ.探究Fe3+产生的原因。
查阅资料可知,反应中溶液逐渐变棕黄色是因为Fe2+被Ag+氧化了。小组同学设计了不同的实验方案对此进行验证。
(3)方案一:取出少量黑色固体,洗涤后,______(填操作和现象),证明黑色固体中有Ag。
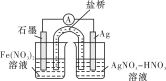
(4)方案二:按下图连接装置,一段时间后取出左侧烧杯中的溶液,加入KSCN溶液,溶液变红。该实验现象________(填“能”或“不能”)证明Fe2+可被Ag+氧化,理由为________。
-
下列叙述正确的是
A.Cu与过量的S混合加热,最终得到CuS
B.将少量 投入
投入 溶液中产生无色气体,同时有白色沉淀生成
溶液中产生无色气体,同时有白色沉淀生成
C.常温下,将27gAl投入足量 的硫酸中,产生
的硫酸中,产生
D.在稀硫酸中加入铜粉,再加入 固体,整个过程中无明显现象
固体,整个过程中无明显现象
-
在250 mL某混合溶液中,HNO3和H2SO4物质的量浓度分别为0.2 mol/L和0.1 mol/L。向该混合溶液中加入1.92 g铜粉,加热充分反应。
(1)写出该反应的离子方程式:___________________。
(2)计算所得溶液中Cu2+的物质的量浓度(写出计算过程,只有结果不得分)。
-
在含有0.4mol HNO3和0.2molHCl的混合酸1L中,加入0.3mol铜粉微热,充分反应后溶液中Cu2+的物质的量为
A.0.15mol B. 0.225mol C. 0.3mol D. 无法计算
-
将质量为m g的铁粉、铜粉和镁粉的混合物,溶于100ml 的12mol•l-1的HNO3溶液(过量),充分反应后所得还原产物为0.09molNO2和0.05molNO,再向所得溶液中加入足量的NaOH溶液至沉淀完全,则沉淀质量为( )
A.(m+1.53)g
B.(m+2.55)g
C.(m+4.08)g
D.mg
-
在某100mL混合酸中,硝酸物质的量浓度为0.4mol/L,硫酸物质的量浓度为0.2mol/L,向其中加入3.2g铜粉,微热,待其充分反应后,溶液中铜离子的物质的量浓度约为
A.0. 15mol/L B.0.3mol/L C.0.5mol/L D.无法计算
-
铁粉、铜粉混合物样品11.6g,逐步加入2.0 mol/L,的硫酸溶液,充分反应后剩余固体质量随加入硫酸溶液体积变化如下表:
| 硫酸溶液/mL | 20.0 | 40.0 | 60.0 | 80.0 |
| 剩余固体/g | 9.36 | 7.12 | 4.88 | 3.20 |
请回答:
(1)样品中铁与铜的物质的量之比n(Fe):n(Cu)=________ 。
(2)在反应后的体系中,再加入4.0mol/L的H2O2溶液25.0mL,并加入足量硫酸溶液.充分反应后溶液中存在的各金属离子的物质的量分别是多少?__________________
-
铁粉、铜粉混合物样品11.6 g,逐滴加入2.0 mol·L-1的硫酸溶液,充分反应后剩余固体质量随加入硫酸溶液体积变化如下表:
| 硫酸溶液/mL | 20.0 | 40.0 | 60.0 | 80.0 |
| 剩余固体/g | 9.36 | 7.12 | 4.88 | 3.20 |
请回答:
(1)样品中铁与铜的物质的量之比n(Fe)∶n(Cu)=________。
(2)在反应后的体系中,再加入4.0 mol·L-1的H2O2溶液25.0 mL,并加入足量硫酸溶液。充分反应后溶液中存在的各金属离子的物质的量分别是多少?__________________________________________。
-
在某100mL混合酸中,HNO3物质的量浓度为0.4mol/L,H2SO4物质的量浓度为0.2mol/L。向其中加入1.92克铜粉微热,待充分反应后,溶液中的Cu2+物质的量浓度为( )
A.0.15mol/L B.0.3mol/L C.0.225mol/L D.无法计算
 [Cu(NH3)2]++Cl‾+2H2O(无色溶液)② 提供的试剂:稀HNO3、AgNO3溶液、氨水、KSCN溶液
[Cu(NH3)2]++Cl‾+2H2O(无色溶液)② 提供的试剂:稀HNO3、AgNO3溶液、氨水、KSCN溶液 B.
B.  C.
C. D.
D. E.
E. F.
F.
