-
Ni2O3主要用作陶瓷、搪瓷和玻璃的着色剂,也可用于镍粉的制造。以镍粉废料为原料制备Ni2O3的工艺如下:
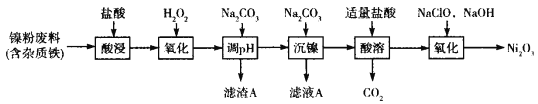
回答下列问题:
(1)Ni2O3中Ni的化合价为___________________________________。
(2)提高“酸浸”、“酸溶”速率时,温度不宜过高,其原因是_________________________。
(3)加入H2O2“氧化”的离子方程式为_________________________________________;滤渣A的主要成分是________________(填化学式)。
(4)工艺中分步加入Na2CO3的作用是________________________________;为提高原料的利用率,应控制加入NaClO与NaOH的物质的量之比为____________________。
-
Ni2O3是灰黑色、有光泽的固体,主要用作陶瓷、搪瓷和玻璃的着色颜料,也可用于制备镍粉。以废镍料为原料提取Ni2O3的工艺流程如图所示。
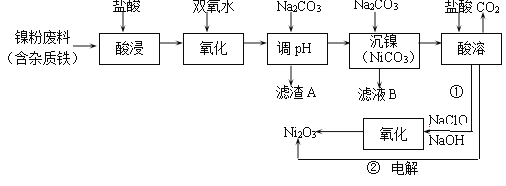
请回答下列问题:
(1)镍的某种化合物NiOOH,其中Ni的化合价为___________。
(2)加入双氧水“氧化”的离子方程式为____________________;滤渣A的主要成分是________________(填化学式)。
(3)步骤①中为了控制“氧化”效率,最佳物质的量之比NaOH/NaClO =________。
(4)步骤②电解法制取Ni2O3,用NaOH调酸溶后溶液的pH至7.5,加入适量Na2SO4后以惰性电极电解。电解过程中产生的Cl2有约40%在弱碱性条件下生成ClO-,再把二价镍氧化为三价镍。加入Na2SO4的作用__________________________;当有n mol二价镍全部转化为三价镍时,外电路中通过电子的物质的量约为____________。
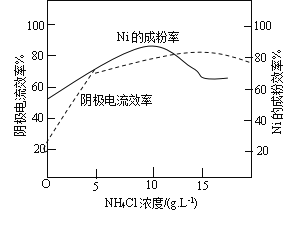
(5)工业上,镍作阳极,电解0.1mol•L-1NiCl2溶液与一定量NH4Cl溶液组成的混合溶液,可得到高纯度、球形的超细镍粉。当其他条件一定时,NH4Cl的浓度对阴极电流效率(电极上实际沉积的物质的量与理论析出量之比)及Ni的成粉的影响如图所示。
① 为获得高纯度的球形超细镍粉,NH4Cl溶液的浓度最好控制为__________g•L-1。
② 当NH4Cl浓度大于15g•L-1时,阴极有气体生成,导致阴极电流效率降低,请结合平衡移动原理解释其原因____。
-
Ni2O3主要用作陶瓷、搪瓷和玻璃的着色颜料,也可用于镍粉的制造,其中一种生产工艺如下(已知还原性:Fe2+>Ni2+):

回答下列问题:
(1) Ni2O3中Ni 的化合价为________________。
(2)为了提高金属镍废料浸出速率,在“酸浸”时可采取的措施有_______________________(写两条)。
(3)若将H2O2溶液改为酸性KMnO4溶液(在该实验条件下,Ni2+不能被KMnO4氧化),则“氧化”过程中的离子方程式为_______________________;加入Na2CO3溶液调pH,产生的“滤渣X”是_____________。
(4)从滤液A中可回收利用的主要物质是___________________;加入NaClO溶液和NaOH溶液,“氧化”生成Ni2O3的离子方程式为_________________________。
(5)工业上用镍为阳极,电解0.05~0.1mol·L-1NiCl2溶液与一定量NH4Cl组成的混合溶液,可得到高纯度、球形的超细镍粉。当其他条件一定时,NH4Cl 的浓度对阴极电流效率及镍的成粉率的影响如下图所示:
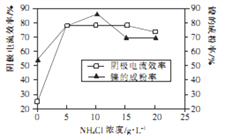
①NH4Cl浓度最好控制为____________g·L-1。
②当NH4Cl浓度大于15g·L-1时,阴极有气体生成,导致阴极电流效率降低,相应的电极反应式
为______________________。
-
三氧化二镍 主要用作陶瓷、玻璃等的着色颜料,也经常用于制造镍电池。查阅资料知:
主要用作陶瓷、玻璃等的着色颜料,也经常用于制造镍电池。查阅资料知:
Ⅰ 工业上利用含镍废料
工业上利用含镍废料 镍、铁、钙、镁合金为主
镍、铁、钙、镁合金为主 制取草酸镍
制取草酸镍 ,再高温煅烧草酸镍制取三氧化二镍。
,再高温煅烧草酸镍制取三氧化二镍。
Ⅱ 草酸的钙、镁、镍盐均难溶于水。
草酸的钙、镁、镍盐均难溶于水。
Ⅲ 、
、 .
.

根据下列工艺流程示意图回答问题。
 加入
加入 发生的主要反应的离子方程式为______,加入
发生的主要反应的离子方程式为______,加入 溶液调pH至
溶液调pH至 ,其目的为______,当加入过量
,其目的为______,当加入过量 后,所得滤液中
后,所得滤液中 ______。
______。
 草酸镍
草酸镍 在热空气中干燥脱水后在高温下煅烧三小时,制得
在热空气中干燥脱水后在高温下煅烧三小时,制得 ,同时获得混合气体。草酸镍受热分解的化学方程式为______。
,同时获得混合气体。草酸镍受热分解的化学方程式为______。
 工业上还可用电解法制取
工业上还可用电解法制取 用NaOH溶液调节
用NaOH溶液调节 溶液的pH至
溶液的pH至 ,加入适量
,加入适量 后采用惰性电极电解。电解过程中产生的
后采用惰性电极电解。电解过程中产生的 有
有 在弱碱性条件下生成
在弱碱性条件下生成 ,再把二价镍氧化为三价镍。
,再把二价镍氧化为三价镍。 氧化
氧化 生成
生成 的离子方程式为______。a mol二价镍全部转化为三价镍时,外电路中通过电子的物质的量为______。
的离子方程式为______。a mol二价镍全部转化为三价镍时,外电路中通过电子的物质的量为______。
 镉镍可充电电池在现代生活中有广泛的应用,其充、放电反应过程按下式进行:
镉镍可充电电池在现代生活中有广泛的应用,其充、放电反应过程按下式进行:

 ,写出该电池充电时阴极的电极反应式______。
,写出该电池充电时阴极的电极反应式______。
-
锡酸钠用作媒染剂,纺织品的防火剂、增重剂,以及制造陶瓷、玻璃和用于镀锡等。以锡锑渣(主要含Sn、Sb、As、Pb的氧化物)为原料,制备锡酸钠(Na2SnO3)的工艺流程图如下:
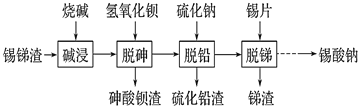
请回答下列问题:
(1) Sb(ⅤA)最高正化合价为_____。
(2) 流程中“脱砷、脱铅、脱锑”均要涉及的分离实验操作是_________。
(3)“碱浸”时,若SnO含量较高,工业上则加入NaNO3除去SnO,且检测到有NH3生成。
①该反应的离子方程式为____________________;
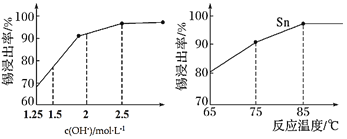
②如图是“碱浸”实验的参数,请选择“碱浸”的合适条件__________。
(4) “脱铅”是从含Na2PbO2的溶液中形成硫化铅渣,其离子方程式为________。
(5) “脱锑”时发生的主要化学反应属于_________。
A.置换反应 B.氧化还原反应 C.非氧化还原反应
(6) 硫酸盐光亮镀锡液成分简单,主要有硫酸亚锡、硫酸等成分。镀锡液中硫酸的作用是__________;镀锡时阳极反应式为______________。
-
锡酸钠用作媒染剂,纺织品的防火剂、增重剂,以及制造陶瓷、玻璃和用于镀锡等。以锡锑渣(主要含Sn、Sb、As、Pb的氧化物)为原料,制备锡酸钠(Na2SnO3)的工艺流程图如下:

请回答下列问题:
(1) Sb(ⅤA)最高正化合价为_____。
(2) 流程中“脱砷、脱铅、脱锑”均要涉及的分离实验操作是_________。
(3)“碱浸”时,若SnO含量较高,工业上则加入NaNO3除去SnO,且检测到有NH3生成。
①该反应的离子方程式为____________________;
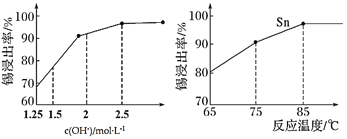
②如图是“碱浸”实验的参数,请选择“碱浸”的合适条件__________。
(4) “脱铅”是从含Na2PbO2的溶液中形成硫化铅渣,其离子方程式为________。
(5) “脱锑”时发生的主要化学反应属于_________。
A.置换反应 B.氧化还原反应 C.非氧化还原反应
(6) 硫酸盐光亮镀锡液成分简单,主要有硫酸亚锡、硫酸等成分。镀锡液中硫酸的作用是__________;镀锡时阳极反应式为______________。
-
MnO2在工业上具有广泛的用途,例如用作干电池去极剂、合成工业的催化剂和氧化剂,玻璃工业和搪瓷工业的着色剂、消色剂、脱铁剂等。
I.在实验室中,可以用MnO2催化分解H2O2或KClO3制备O2。
(1)设计简单的实验验证MnO2对H2O2的分解起催化作用________。
(2)如果用MnO2催化分解KCIO3制备并收集O2,应选用的实验装置是_______。

若用B装置制备少量的NH3,则a中盛放的药品是_______。
II.MnO2是实验室中常见的氧化剂,某化学兴趣小组探究在常温下,MnO2能否氧化酸性NaI溶液。可选用的试剂和仪器有:0.5mol/LNaI溶液,稀硫酸、稀盐酸、CCl4、酒精、分液漏斗、烧杯、漏斗、玻璃棒、酒精灯、温度计、牛角管、锥形瓶、石棉网、铁架台(带铁圈、铁夹)。
实验的步骤如下:
①在小烧杯中加入15mLNaI溶液,加硫酸使其酸化,加适量的MnO2,充分搅拌。
②将所得溶液过滤,观察滤液颜色。
③向滤液中加入5mL萃取剂,充分振荡。
④置于铁架台铁圈上静置。
⑤分液。
⑥将下层得到的含I2溶液进行蒸馏使得到单质I2。
请回答下列问题:
(1)写出步骤①中发生的离子方程式___________。
(2)观察步骤②所得滤液的颜色为_______,初步判定有单质I2生成。
(3)萃取滤液中的碘单质所用的仪器名称为_______,选择的萃取剂是______。
(4)步骤④静置后,观察到的现象是_______。
(5)简述分液的操作:________。
(6)步骤⑥中组装蒸馏装置还缺少的仪器是___________。
-
草酸亚铁为黄色固体,作为一种化工原料, 可广泛用于涂料、染料、陶瓷、玻璃器皿等的着色剂以及新型电池材料、感光材料的生产。合成草酸亚铁的流程如下:

(1)配制(NH4)2Fe(SO4)2溶液时,需加入少量稀硫酸,目的是 。
(2)得到的草酸亚铁沉淀需充分洗涤,检验是否洗涤干净的方法是 。
(3)将制得的产品(FeC2O4·2H2O)在氩气气氛中进行加热分解,结果如下图(TG%表示残留固体质量占原样品总质量的百分数)。
①则A→B发生反应的化学方程式为: 。
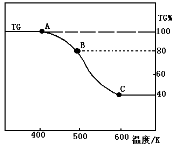
②已知B→C过程中有等物质的量的两种气态氧化物生成,写出B→C的化学方程式 ;
(4)某草酸亚铁样品中含有少量草酸铵。为了测定不纯产品中草酸根的含量,某同学做了如下分析实验:
Ⅰ.准确称量m g样品,溶于少量2mol/L硫酸中并用100mL容量瓶定容。
Ⅱ.取上述溶液20mL,用c mol/L高锰酸钾标准溶液滴定,溶液变为淡紫色,消耗高锰酸钾溶液的体积为V1 mL。
Ⅲ.向上述溶液中加入足量Zn粉,使溶液中的Fe3+恰好全部还原为Fe2+。
Ⅳ.过滤,洗涤剩余的锌粉和锥形瓶,洗涤液并入滤液
Ⅴ.用c mol/L KMnO4溶液滴定该滤液至溶液出现淡紫色,消耗KMnO4溶液的体积V2 mL。
已知:2MnO4-+5H2C2O4+6H+=2Mn2+ +10CO2+8H2O
MnO4-+8H++5Fe2+=5Fe3+ + Mn2++4H2O
回答下列问题:
①若省略步骤Ⅳ,则测定的草酸根离子含量 (填“偏大”、“偏小”或“不变”)。
②m g样品中草酸根离子的物质的量为 (用c,V1,V2的式子表示,不必化简)。
-
(本题满分18分)草酸亚铁为黄色固体,作为一种化工原料,可广泛用于涂料、陶瓷、玻璃器皿等的着色剂以及新型电池材料、感光材料的生产。合成草酸亚铁的流程如下:

(1)配制(NH4)2Fe(SO4)2 6H2O溶液时,需加入少量稀硫酸,目的是_____________。
6H2O溶液时,需加入少量稀硫酸,目的是_____________。
(2)得到的草酸亚铁沉淀需充分洗涤,检验是否洗涤干净的方法是_____________。
(3)将制得的产品(FeC2O4·2H2O)在氩气气氛中进行加热分解,结果如下图(TG%表示残留固体质量占原样品总质量的百分数)。
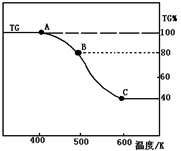
①则A-B发生反应的化学方程式为_____________;
②已知B→C过程中有等物质的量的两种气态氧化物生成,写出B→C的化学方程式_____________;
(4)某草酸亚铁样品中含有少量草酸铵。为了测定不纯产品中草酸根的含量,某同学做了如下分析实验:
Ⅰ.准确称量m g样品,溶于少量2mol/L硫酸中并用100mL容量瓶定容。
Ⅱ.取上述溶液20mL,用c mol/L高锰酸钾标准溶液滴定,溶液变为淡紫色,消耗高锰酸钾溶液的体积为V1 mL。
Ⅲ.向上述溶液中加入足量Zn粉,使溶液中的Fe3+恰好全部还原为Fe2+,过滤。
Ⅳ.洗涤剩余的锌粉和锥形瓶,洗涤液并入滤液。
Ⅴ.用c mol/L KMnO4溶液滴定该滤液至溶液出现淡紫色,消耗KMnO4溶液的体积V2 mL。
回答下列问题:
①已知:草酸(H2C2O4)与酸性高锰酸钾溶液反应,现象是有气泡产生,紫色消失,写出该反应的离子方程式:_____________;
②若省略步骤Ⅳ,则测定的草酸根离子含量 ________________________________(填“偏大”、“偏小”或“不变”)。
③m g样品中草酸根离子的物质的量为_____________(用c,V1,V2的式子表示,不必化简)
-
草酸亚铁为黄色固体,作为一种化工原料,可广泛用于涂料、陶瓷、玻璃器皿等的着色剂以及新型电池材料、感光材料的生产。 合成草酸亚铁的流程如下:
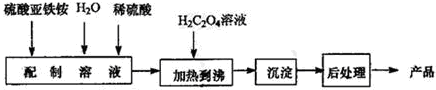
(1)配制(NH4)2Fe(SO4)2 6H2O溶液时,需加入少量稀硫酸,目的是_____________。
6H2O溶液时,需加入少量稀硫酸,目的是_____________。
(2)得到的草酸亚铁沉淀需充分洗涤,检验是否洗涤干净的方法是_____________。
(3)将制得的产品(FeC2O4·2H2O)在氩气气氛中进行加热分解,结果如下图(TG%表示残留固体质量占原样品总质量的百分数)。
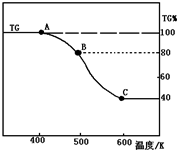
①则A-B发生反应的化学方程式为_____________;
②已知B→C过程中有等物质的量的两种气态氧化物生成,写出B→C的化学方程式_____________;
(4)某草酸亚铁样品中含有少量草酸铵。为了测定不纯产品中草酸根的含量,某同学做了如下分析实验:
Ⅰ.准确称量m g样品,溶于少量2mol/L硫酸中并用100mL容量瓶定容。
Ⅱ.取上述溶液20mL,用c mol/L高锰酸钾标准溶液滴定,溶液变为淡紫色,消耗高锰酸钾溶液的体积为V1 mL。
Ⅲ.向上述溶液中加入足量Zn粉,使溶液中的Fe3+恰好全部还原为Fe2+,过滤,
Ⅳ.洗涤剩余的锌粉和锥形瓶,洗涤液并入滤液
Ⅴ.用c mol/L KMnO4溶液滴定该滤液至溶液出现淡紫色,消耗KMnO4溶液的体积V2 mL。
回答下列问题:
①已知:草酸(H2C2O4)与酸性高锰酸钾溶液反应,现象是有气泡产生,紫色消失,写出该反应的离子方程式:_____________;
①若省略步骤Ⅳ,则测定的草酸根离子含量 (填“偏大”、“偏小”或“不变”)
②m g样品中草酸根离子的物质的量为_____________(用c,V1,V2的式子表示,不必化简)
















