实验室可利用反应Na2S+H2NCN+2H2O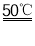 CS(NH2)2+2NaOH在控制溶液pH为10~11时,制取少量CS(NH2)2(硫脲,受热易分解,能溶于水)。实验装置(夹持及加热装置已省略)如图所示。下列说法错误的是
CS(NH2)2+2NaOH在控制溶液pH为10~11时,制取少量CS(NH2)2(硫脲,受热易分解,能溶于水)。实验装置(夹持及加热装置已省略)如图所示。下列说法错误的是
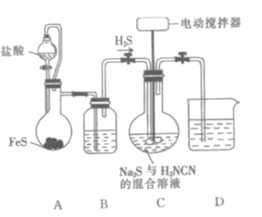
A.装置B中盛放的试剂为饱和NaHS溶液
B.装置C可用水浴加热
C.持续通入H2S,有利于提高反应液中硫脲的含量
D.为获得硫脲晶体可将烧瓶中的反应液蒸发至干
高二化学单选题中等难度题
实验室可利用反应Na2S+H2NCN+2H2O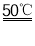 CS(NH2)2+2NaOH在控制溶液pH为10~11时,制取少量CS(NH2)2(硫脲,受热易分解,能溶于水)。实验装置(夹持及加热装置已省略)如图所示。下列说法错误的是
CS(NH2)2+2NaOH在控制溶液pH为10~11时,制取少量CS(NH2)2(硫脲,受热易分解,能溶于水)。实验装置(夹持及加热装置已省略)如图所示。下列说法错误的是

A.装置B中盛放的试剂为饱和NaHS溶液
B.装置C可用水浴加热
C.持续通入H2S,有利于提高反应液中硫脲的含量
D.为获得硫脲晶体可将烧瓶中的反应液蒸发至干
高二化学单选题中等难度题
肼是重要的化工原料。某探究小组利用下列反应制取水合肼(N2H4·H2O):CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4·H2O+NaCl。
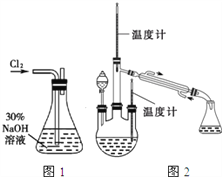
实验一:制备NaClO溶液(实验装置如图1所示)
(1)锥形瓶中发生反应的离子方程式是________________________________________________。
实验二:制取水合肼.(实验装置如图2所示)
已知水合肼具有还原性,被氧化生成氮气。
控制反应温度,将分液漏斗中溶液缓慢滴入三颈烧瓶中,充分反应。加热蒸馏三颈烧瓶内的溶液,收集108~114℃馏分。
(2)分液漏斗中的溶液是______(填标号)。
A.CO(NH2)2溶液 B.NaOH和NaClO混合溶液
选择的理由是____________________________________________________。
实验三:测定馏分中水合肼的质量分数。采用下列步骤:
A.称取馏分5.000g,加入适量NaHCO3固体,加水配成250mL溶液。
B.移取25.00mL溶液于锥形瓶中,加入10 mL水,摇匀。
C.用0.2000 mol·L-1的I2溶液滴定,至溶液出现微黄色且半分钟内不消失,滴定过程中,溶液的pH保持在6.5左右,记录消耗碘的标准溶液的体积。
d.进一步操作与数据处理。
(3)水合肼与碘溶液反应的化学方程式为:_______________________;
(4)滴定过程中,NaHCO3能控制溶液的pH在6.5左右,原因是_______________。
(5)滴定时,碘的标准溶液盛放在___________(填“酸式”或“碱式”)滴定管中;若三次滴定消耗碘的标准溶液的平均体积为18.00 mL,则馏分中水合肼(N2H4·H2O)的质量分数为____________________(保留三位有效数字)。
高二化学实验题困难题查看答案及解析
水合肼 (N2H4·H2O) 常用作还原剂和抗氧剂,其熔点为 -40℃,沸点 118.5℃,极毒。实验室用如下装置制取水合肼(N2H4·H2O)涉及下列反应:
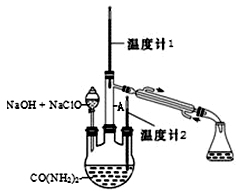
CO(NH2)2+ 2NaOH +NaClO = Na2CO3 + N2H4·H2O + NaCl
N2H4·H2O + 2NaClO = N2↑ + 3H2O + 2NaCl]
请回答下列问题:
(1)配制30%NaOH溶液时,所需玻璃仪器除量筒外,还有 (填标号)。
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2)将Cl2通入30%NaOH溶液制备NaClO的化学方程式 。
(3)实验时,如果将 NaOH 和NaClO的混合溶液一次性加入三颈烧瓶,可能会造成的结果是__________。
(4)实验时可根据_________判断N2H4·H2O开始蒸出。
(5)已知:N2H4·H2O + 2I2= N2↑+ 4HI + H2O。测定水合肼的质量分数可采用下列步骤:
①取1.250g试样,经溶解、转移、定容等步骤,配制250mL溶液。
②移取10.00mL溶液于锥形瓶中,滴入几滴淀粉溶液,加20mL水,摇匀。
③将0.1000mol·L-1碘的标准溶液盛放在__________滴定管中(填“酸式”或“碱式”),当_____________停止滴定,消耗碘的标准溶液为18.00mL,则产品中N2H4·H2O的质量分数为__________。
高二化学实验题简单题查看答案及解析
实验室常利用以下反应制取少量氮气:NaNO2+NH4Cl=NaCl+N2↑+2H2O;关于该反应的下列说法不正确的是( )
A.NH4Cl中的氮元素被还原,发生还原反应
B.NaNO2是氧化剂,NH4Cl是还原剂
C.N2既是氧化产物,又是还原产物
D.每生成2molN2时,转移电子的物质的量为6mol
高二化学单选题中等难度题查看答案及解析
实验室制取少量N2常利用的反应是NaNO2+NH4ClNaCl+N2↑+2H2O,关于该反应的说法正确的是
A.NaNO2是氧化剂 B.生成1 mol N2时转移的电子数是6 mol
C.NH4Cl中的N元素被还原 D.N2既是氧化剂又是还原剂
高二化学选择题中等难度题查看答案及解析
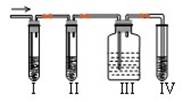
(10分)在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题:
(1)实验室制备乙烯的反应方程式是:
________
(2)I、II、III、IV装置可盛放的试剂是I________;II________;III;IV________。 ________(将下列有关试剂的序号填入空格内)。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(3)能说明SO2气体存在的现象是。
(4)使用装置II的目的是。
(5)使用装置III的目的是。
(6)确定含有乙烯的现象是。
高二化学实验题简单题查看答案及解析
水合肼(N2H4·H2O)又名水合联氨,无色透明,是具有腐蚀性和强还原性的碱性液体,它是一种重要的化工试剂。利用尿素法生产水合肼的原理为:CO(NH2)2+2NaOH+NaClO=N2H4·H2O+Na2CO3+NaCl。
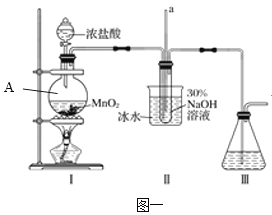
实验1:制备NaClO溶液。(已知:3NaClO2NaCl+NaClO3)
(1)如图一装置A中___(仪器名称)内发生反应的化学方程式为___。
(2)用NaOH固体配制溶质质量分数为30%的NaOH溶液时,所需玻璃仪器除量筒外还有____(填字母)。
a.烧杯 b.容量瓶 c.玻璃棒 d.烧瓶
(3)图中装置Ⅱ中用冰水浴控制温度的目的是____。
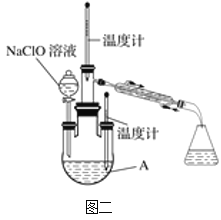
实验2:制取水合肼。
(4)图二中充分反应后,___(填操作名称)A中溶液即可得到水合肼的粗产品。若分液漏斗滴液速度过快,部分N2H4·H2O会参与A中反应并产生大量氮气,降低产品产率。写出该过程反应生成氮气的化学方程式___。
实验3:测定馏分中水合肼的含量。
(5)称取馏分3.0g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH保持在6.5左右),加水配成250mL溶液,移出25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.15mol·L-1的碘的标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。
①滴定时,碘的标准溶液盛放在___(填“酸式”或“碱式”)滴定管中。
②下列能导致馏分中水合肼的含量测定结果偏高的是___(填字母)。
a.锥形瓶清洗干净后未干燥
b.滴定前,滴定管内无气泡,滴定后有气泡
c.读数时,滴定前平视,滴定后俯视
d.盛标准液的滴定管水洗后,直接装标准液
③实验测得消耗I2溶液的平均值为20.00mL,馏分中水合肼(N2H4·H2O)的质量分数___。
高二化学实验题中等难度题查看答案及解析
下列叙述不正确的是( )
A.白铁(镀锌铁)镀层破损后,先被腐蚀的是铁
B.锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
C.钢铁表面常易锈蚀生成Fe2O3·nH2O
D.金属的腐蚀主要是电化学腐蚀
高二化学选择题简单题查看答案及解析
高二化学选择题中等难度题查看答案及解析
某化学兴趣小组利用NaI溶液中通入少量Cl2得到含碘废液,再利用含碘废液获取NaI固体,实验流程如下:
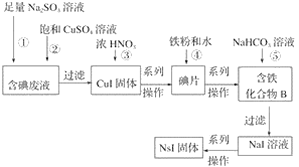
已知反应②:2I﹣+2Cu2+++H2O=2CuI↓+
+2H+。
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、__。
(2)反应③中CuI被氧化,还原产物只有NO2,该反应的化学方程式为__。
当有95.5 g CuI参与反应,则需要标况下__L的O2才能将生成的NO2在水中完全转化为硝酸。
(3)化合物B中含两种元素,铁原子与另一种元素原子的物质的量之比为3∶8,则化合物B的化学式为__。
(4)反应⑤中生成黑色固体和无色气体,黑色固体的俗称为磁性氧化铁,则反应⑤的化学方程式为__。
(5)将足量的Cl2通入含12 g NaI的溶液中,一段时间后把溶液蒸干得到固体的质量为__g。
高二化学综合题简单题查看答案及解析
下列实验操作能达到目的的是( )
①用Na2S溶液和Al2(SO4)3溶液反应制取Al2S3固体
②用加热蒸发K2CO3溶液的方法获得K2CO3晶体
③用Na2S溶液和CuSO4溶液反应制取CuS固体
④加热MgCl2溶液制取MgCl2固体
A.①② B.①③ C.③④ D.②③
高二化学选择题中等难度题查看答案及解析