对于反应aA(g)+bB(g) ⇌cC(g)+dD(g) ΔH,反应特点与对应的图象的说法中不正确的是( )
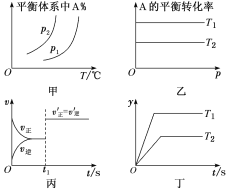
A.图甲中,若p1>p2,则a+b>c+d,ΔH<0
B.图乙中,若T2>T1,则ΔH<0且a+b=c+d
C.图丙中,t1时刻改变的条件一定是使用了催化剂
D.图丁中,若ΔH<0,则纵坐标不可能表示的是反应物的转化率
高二化学单选题中等难度题
对于反应aA(g)+bB(g) ⇌cC(g)+dD(g) ΔH,反应特点与对应的图象的说法中不正确的是( )

A.图甲中,若p1>p2,则a+b>c+d,ΔH<0
B.图乙中,若T2>T1,则ΔH<0且a+b=c+d
C.图丙中,t1时刻改变的条件一定是使用了催化剂
D.图丁中,若ΔH<0,则纵坐标不可能表示的是反应物的转化率
高二化学单选题中等难度题
对于反应aA(g)+bB(g)cC(g)+dD(g) ΔH,反应特点与对应的图像的说法中不正确的是( )
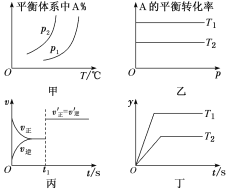
A.图甲中,若p1>p2,则在较低温度下有利于该反应自发进行
B.图乙中,若T2>T1,则ΔH<0且a+b=c+d
C.图丙中,t1时刻改变的条件一定是使用了催化剂
D.图丁中,若ΔH<0,则纵坐标不可能表示的是反应物的转化率
高二化学单选题中等难度题查看答案及解析
对于反应:aA(g)+bB(g)cC(g),反应特点与对应的图象说法正确的是

A.图甲表明:该反应△H<0,若 a+b>c,则 p1>p2
B.图乙表明,该反应 a+b=c,若△H>0,则 T2>T1
C.图丙中,一定是使用了催化剂
D.图丁中,E 点 v(逆)>v(正)
高二化学单选题中等难度题查看答案及解析
对于反应aA(g)+bB(g) ⇌cC(g)+dD(g) ΔH,反应特点与对应的图象的说法中不正确的是( )

A.图甲中,若p1>p2,则a+b>c+d,ΔH<0
B.图乙中,若T2>T1,则ΔH<0且a+b=c+d
C.图丙中,t1时刻改变的条件一定是使用了催化剂
D.图丁中,若ΔH<0,则纵坐标不可能表示的是反应物的转化率
高二化学单选题中等难度题查看答案及解析
反应:aA(g)+bB(g) cC(g)+dD(g)
H,学习小组针对反应特点与对应的图象展开了讨论,其中不正确的是

A. 图①中,若p1>p2,则该反应在较低温度下有利于自发进行
B. 图②中,若T2>T1,则H<0且a+b=c+d
C. 图③中(υ/表示正反应速率,υ//表示逆反应速率),t1时刻改变的条件一定是使用了催化剂
D. 图④中,若H<0,则纵坐标不可能表示的是反应物的转化率
高二化学选择题困难题查看答案及解析
反应:aA(g)+bB(g)cC(g)+dD(g)
H,学习小组针对反应特点与对应的图象展开了讨论,其中不正确的是
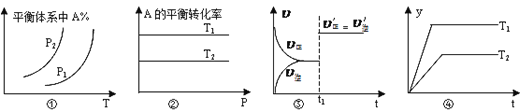
A. 图①中,若p1>p2,则a+b>c+d
B. 图②中,若T2>T1,则H<0且a+b=c+d
C. 图③中,t1时刻改变的条件一定是使用了催化剂
D. 图④中,若H<0,则纵坐标不可能表示反应物的转化率
高二化学单选题中等难度题查看答案及解析
反应:aA(g)+bB(g)cC(g)+dD(g)
H,学习小组针对反应特点与对应的图象展开了讨论,其中不正确的是

A. 图①中,若p1>p2,则a+b>c+d
B. 图②中,若T2>T1,则H<0且a+b=c+d
C. 图③中,t1时刻改变的条件一定是使用了催化剂
D. 图④中,若H<0,则纵坐标不可能表示反应物的转化率
高二化学单选题中等难度题查看答案及解析
下列说法不正确的是
A.能够发生有效碰撞的分子叫做活化分子,活化分子所多出的那部分能量称作活化能。
B.对于某一反应aA + bB =cC + dD,△H单位中的mol-1是指每摩尔(aA + bB =cC + dD)反应。
C.研究有机物的组成、结构、性质、制备方法与应用的科学叫有机化学。
D.甲烷分子具有正四面体结构的原因是碳原子的2s轨道与2p轨道发生sp杂化。
高二化学选择题中等难度题查看答案及解析
下列有关化学反应与能量的说法中不正确的是( )
A.对于反应aA+bB=cC+dD,△H单位中的“每摩尔”是指每摩尔A或每摩尔B
B.化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关
C.化学反应过程中放出或吸收的热量,叫做反应热
D.能量的释放或吸收是以发生变化的物质为基础的,二者密不可分,但以物质为主。
高二化学选择题中等难度题查看答案及解析
根据相应的图象(图象编号与答案一一对应),判断下列相关说法正确的是( )
| 选项 | A | B | C | D |
| 图像 |
|
|
|
|
| 反应 | aX(g)+bY(g)⇌cZ(g) | L(s)+aG(g)⇌bR(g) | aA+bB⇌cC | A+2B⇌2C+3D |
| 操作或条件 | 密闭容器中反应达到平衡,T0时改变某一条件有如图变化所示,则改变的条件一定是加入催化剂 | 反应达到平衡时,外界条件对平衡影响关系如图所示,则正反应为放热反应,且a>b | 物质的百分含量和温度关系如图所示,则该反应的正反应为吸热反应 | 反应速率和反应条件变化关系如图所示,则该反应的正反应为放热反应,A、B、C是气体,D为固体或液体 |
A.A B.B C.C D.D
高二化学单选题中等难度题查看答案及解析
对于平衡体系:aA(g)+bB(g)cC(g)+dD(g);正反应放热,有下列判断,其中正确的是( )
A.若温度不变,容器体积扩大一倍,此时A的浓度是原来的0.45倍,则 a+b>c+d
B.若从正反应开始,平衡时,A、B的转化率相等,则投入A、B的物质的量之比为a:b
C.若平衡体系中共有气体M mol,再向其中充入6 mol B,达到平衡时 气体总物质的量为(M+b)mol,则a+b>c+d
D. a+b=c+d,则当容器温度上升时,平衡向左移动,容器中气体的压强不变
高二化学选择题困难题查看答案及解析