-
铁是生产生活中应用最广泛的一种金属。某化学学习小组在实验室中探究铁钉(主要成分为低碳钢)与热浓硫酸的反应。其探究流程如图所示:
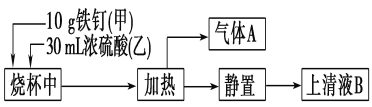
(1)从实验安全的角度考虑,应先向烧杯中加入______(填“甲”或“乙”);根据加入的反应物的量,实验需要选取的烧杯的规格为________(填字母序号)。
a.50 mL b.100 mL c.500 mL d.1 000 mL
(2)上清液B中可能既含Fe3+,又含Fe2+,要检验上清液B中有无Fe2+,应加入的试剂是________(填字母序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.NaOH溶液 d.酸性KMnO4溶液
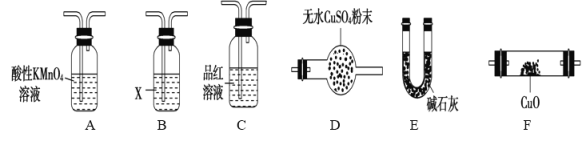
(3)气体A的主要成分是SO2,还可能含有H2和CO2。流程图中“加热”时可能生成CO2的原因是(用化学方程式表示)___________________。利用下列仪器可以同时检验气体A中是否含有H2和CO2(其中的夹持仪器、橡胶管和加热装置已经略去),则仪器的连接顺序是____________
(4)烧杯中的产物之一FeSO4有如下转化关系 (无关物质已略去)。
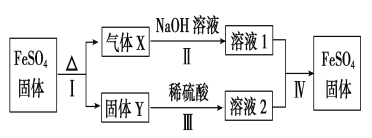
已知:①X由两种化合物组成,将X通入品红溶液,溶液褪色;通入BaCl2溶液,产生白色沉淀。②Y是红棕色的化合物。反应Ⅰ的化学方程式为_________________X通入BaCl2溶液,产生白色沉淀的化学式为________
-
某化学学习小组在实验室中探究铁钉与热浓硫酸的反应。其探究流程如图所示:
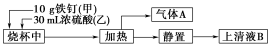
(1)从实验安全的角度考虑,应先向烧杯中加入______(填“甲”或“乙”)。
(2)根据加入的反应物的量,实验需要选取的烧杯的规格为________(填字母序号)。
a.50 mL b.100 mL c.500 mL d.1 000 mL
(3)上述流程图中从“静置”后的混合物中得到上清液B不能采用过滤的操作方法,其原因是__________________________________。
由于铁钉生锈,上清液B中可能既含Fe3+,又含Fe2+,要检验上清液B中有无Fe2+,应加入的试剂是________(填字母序号)。
a.KSCN溶液和氯水
b.铁粉和KSCN溶液
c.NaOH溶液
d.酸性KMnO4溶液
(4)气体A的主要成分是SO2,还可能含有H2和CO2。流程图中“加热”时可能生成CO2的原因是________________(用化学方程式表示)。
利用下列仪器可以同时检验气体A中是否含有H2和CO2(其中的夹持仪器、橡胶管和加热装置已经略去),则仪器的连接顺序是________(填仪器的字母代号),装置A的作用是____________________________,装置B中试剂X的化学式是________。
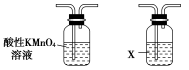
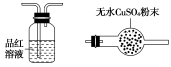
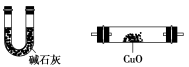
A B C D E F
-
(14分)氨在人类的生产和生活中有着广泛的应用.某化学兴趣小组利用图一装置探究氨气的有关性质。

(1)装置A中烧瓶内试剂可选用 (填序号).B的作用是 .
a.碱石灰 b.生石灰 c.浓硫酸 d.烧碱溶液
(2)连接好装置并检验装置的气密性后,装入药品,然后应先 (填I或Ⅱ).
Ⅰ.打开旋塞逐滴向圆底烧瓶中加入氨水Ⅱ.加热装置C
(3)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为 .该反应证明氨气具有 性.
(4)该实验缺少尾气吸收装置,图二中能用来吸收尾气的装置是 (填装置序号).
(5)氨气极易溶于水,若标准状况下,将2.24L的氨气溶于水配成1L溶液,所得溶液的物质的量浓度为_______mol/L.
-
(12分)氨在人类的生产和生活中有着广泛的应用.某化学兴趣小组利用图一装置探究氨气的有关性质。
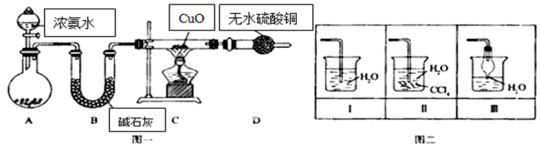
(1)装置A中烧瓶内试剂可选用 (填序号).B的作用是 .
a.碱石灰 b.生石灰 c.浓硫酸 d.烧碱溶液
(2)连接好装置并检验装置的气密性后,装入药品,然后应先 (填I或Ⅱ).
Ⅰ.打开旋塞逐滴向圆底烧瓶中加入氨水Ⅱ.加热装置C
(3)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为 .该反应证明氨气具有 性.
(4)该实验缺少尾气吸收装置,图二中能用来吸收尾气的装置是 (填装置序号).
(5)氨气极易溶于水,若标准状况下,将2.24L的氨气溶于水配成1L溶液,所得溶液的物质的量浓度为_______mol/L.
-
二氧化硫是硫的重要化合物,在生产、生活中有广泛应用,是大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2,可以使用的药品和装置如图所示:
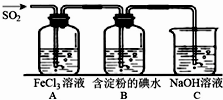
(1)写出由铜和浓硫酸制取SO2的化学方程式_____________________。
(2)装置A中的现象是__________。若要从A中的FeCl3溶液中提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在过滤操作中有用到的玻璃仪器有_______(填编号)。
A酒精灯 B烧瓶 C漏斗 D烧杯 E玻璃棒 F坩埚
(3)根据以上现象,该小组同学认为SO2与FeCl3发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式___________________;
②请设计实验方案检验有Fe2+生成__________________________;
(4)B中蓝色溶液褪色,表明I-的还原性比SO2__________(填“强”或“弱”)。
(5)若C中所得溶液只有一种溶质且pH>7,则溶液中各离子浓度大小顺序为_________。
(6)工业上通过煅烧黄铁矿产生SO2来进一步得到硫酸,已知煅烧1g FeS2产生7.1kJ热量,写出煅烧FeS2的热化学反应方程式____________________。
-
二氧化硫是硫的重要化合物,在生产、生活中有广泛应用,是大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2,可以使用的药品和装置如图所示:
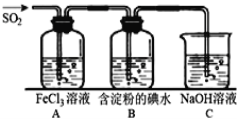
(1)写出由铜和浓硫酸制取SO2的化学方程式_______________________________。
(2)装置A中的现象是__________________________________________________。反应结束后若要从A中的FeCl3溶液中提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在蒸发操作中要用到的主要仪器有_______(填编号)。自然干燥晶体而不烘干晶体的原因是___________________________。
A.酒精灯 B.蒸发皿 C.漏斗 D.烧杯 E.玻璃棒 F.坩埚
(3)根据以上现象,该小组同学认为SO2与FeCl3发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式__________________________;
②请设计实验方案检验有Fe2+生成__________________________;
(4)B中蓝色溶液褪色,表明SO2的还原性比I-_________(填“强”或“弱”)。
-
二氧化硫是硫的重要化合物,在生产、生活中有广泛应用,是大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2,可以使用的药品和装置如图所示:
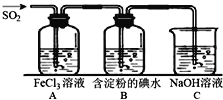
(1)写出由铜和浓硫酸制取SO2的化学方程式_____________________。
(2)装置A中的现象是__________。若要从A中的FeCl3溶液中提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在过滤操作中有用到的玻璃仪器有_______(填编号)。
A酒精灯 B烧瓶 C漏斗 D烧杯 E玻璃棒 F坩埚
(3)根据以上现象,该小组同学认为SO2与FeCl3发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式___________________;
②请设计实验方案检验有Fe2+生成__________________________;
(4)B中蓝色溶液褪色,表明I-的还原性比SO2__________(填“强”或“弱”)。
(5)若C中所得溶液只有一种溶质且pH>7,则溶液中各离子浓度大小顺序为_________。
(6)工业上通过煅烧黄铁矿产生SO2来进一步得到硫酸,已知煅烧1g FeS2产生7.1kJ热量,写出煅烧FeS2的热化学反应方程式____________________。
-
为研究某铁钉与浓硫酸反应生成气体Y的成分,某学习小组做出假设,认为所得气体中除含有SO2外,还可能含有H2和Q气体,并设计了下列实验装置(图中夹持仪器省略)探究气体的成分,为确认Q的存在,需在装置中添加M于( )
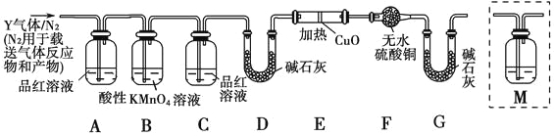
A.A-B之前 B.B-C间 C.C-D间 D.D-E间
-
氯化铁在现代生产和生活中应用广泛。某化学研究性学习小组模拟工业生产流程制备无水氯化铁并对产物做了如下探究实验。
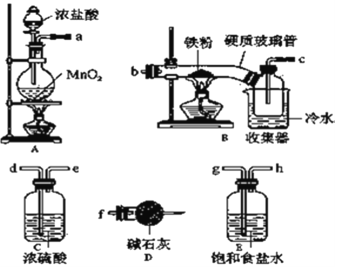
已知:Ⅰ.无水氯化铁在空气中易潮解,加热易升华;
Ⅱ.工业上,向500~600℃的铁屑中通入氯气可生产无水氯化铁;
Ⅲ.向炽热铁屑中通入氯化氢可以生产无水氯化亚铁和氢气。
请回答下列问题:
(1)装置的连接顺序为 _____________(按气流从左向右的方向,填仪器接口字母)。
(2)装置D的作用是 _________;
若缺少装置E对本实验造成的影响是_________________________________________。
(3)工业生产中,会将装置D中的干燥剂换成无水氯化钙,通过装置D后产生的过量氯气再用氯化亚铁溶液吸收,得到氯化铁溶液作为副产品。氯化亚铁溶液因吸收Cl2失去作用而失效,下列试剂中能够检验氯化亚铁溶液是否完全失效的所用的试剂是_____________。
(4)实验结束并冷却后,将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
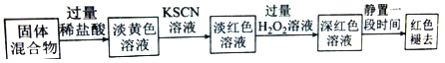
淡红色溶液中加入过量H2O2后溶液红色加深的原因是 __________ (用离子方程式表示)。
| 实验 | 操作 | 现象 |
| 实验甲:取褪色后溶液3等份 | 第1份 | 滴加FeCl3溶液 | 无明显变化 |
| 第2份 | 滴加KSCN溶液 | 溶液变为红色 |
| 第3份 | 滴加稀盐酸和BaCl2 | 产生白色沉淀 |
| 实验乙:取与褪色后溶液同浓度的FeCl3溶液 | 滴加2滴KSCN溶液,溶液变红,再通入O2 | 无明显变化 |
根据实验现象判断,以下说法不正确的是 _____(填选项字母)。
A. 实验甲说明是Fe3+发生了反应而不是SCN—发生反应
B. 实验甲说明是SCN—发生了反应而不是Fe3+发生反应
C.实验甲中第3份溶液中生成的白色沉淀为BaSO4
D.实验乙排除H2O2分解产生的O2氧化SCN—的可能
由实验甲和乙得出的结论为______________________________ 。
-
氯化铁在现代生产和生活中应用广泛。某化学研究性学习小组模拟工业生产流程制备无水氯化铁并对产物做了如下探究实验。

经查阅资料得知:①无 水氯化铁在空气中易潮解,加热易升华;②工业上,向500—600℃的铁屑中通入氯气可生产无水氯化铁;③向炽热铁屑中通入氯化氢可以生产无水氯化亚铁和氢气。
水氯化铁在空气中易潮解,加热易升华;②工业上,向500—600℃的铁屑中通入氯气可生产无水氯化铁;③向炽热铁屑中通入氯化氢可以生产无水氯化亚铁和氢气。
请回答下列问题:
(1)装置的连接顺序为_______________(用a、b、c…h表示)。
(2)若缺少装置E对本实验造成的影响是________________________。
(3)工业生产中,会将D中干燥剂换成无水氯化钙,通过D后产生的过量氯气再用氯化亚铁溶液吸收,得到氯化铁溶液作为副产品。氯化亚铁溶液因吸收C12失去作用而失效,下列试剂中能够检验氯化亚铁溶液是否完全失效的是_______________。
a.硫氰酸钾溶液 b.铁氰化钾溶液 c.高锰酸钾溶液 d.烧碱溶液
(4)实验结束并冷却后,将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物 油(反应过程中不振荡),充分反应后,进行如下实验:
油(反应过程中不振荡),充分反应后,进行如下实验:

淡红色溶液中加入过量H2O2后溶液红色加深的原因是___________________(用离子方程式表示)。
已知红色褪去的同时有气体生成,经检验为O2。该小组对红色褪去的原因进行探究。
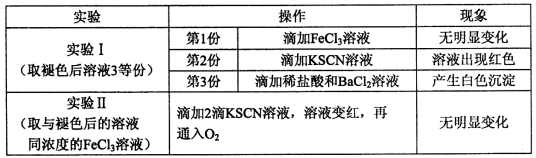
根据实验现象判断,以下说法正确的是_________________________。(填标号)
a.实验I说明是SCN发生了反应而不是Fe3+发生反应
b.实验I说明是Fe3+发生了反应而不是SCN-发生反应
c.实验I中第3份溶液中生成的白色沉淀为BaSO3
d.实验Ⅱ排除H2O2分解产生的O2氧化SCN-的可能
由实验I和Ⅱ得出结论为_______________________________________。

















