-
在古代,人们常用贝壳(主要成分是碳酸钙,杂质不参加反应且不溶于水)和纯碱为原料制取烧碱。某小组同学按如图所示流程进行实验,请你参与讨论并回答相关问题。
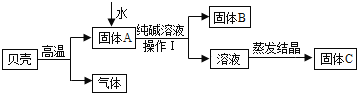
(1)贝壳高温锻烧时,发生反应的化学方程式是_____。
(2)操作I中用到的玻璃仪器有烧杯、_____、玻璃棒。
(3)溶液蒸发结晶得到固体C的过程中,常用玻璃棒搅拌,其目的是_____。
[问题与发现]该小组同学所得到的固体C一定是纯净的NaOH吗?
[猜想与假设]根据反应原理,甲、乙、丙三位同学提出以下猜想:
甲:纯净的NaOH;
乙:NaOH和Na2CO3的混合物;
丙:NaOH和Ca(OH)2的混合物。
[探究与验证]甲、乙、丙三位同学分别设计下列方案,对自己的猜想进行验证。实验操作、现象和结论如表,请参与他们的探究并填写所缺内容。
| 实验操作 | 现象 | 结论 |
| 甲 | 取少量固体C,溶于适量水形成溶液后,滴加几滴酚酞溶液 | 溶液变红 | 猜想成立 |
| 乙 | 取少量固体C,溶于适量水形成溶液后,滴加足量_____(合理即可) | 无气泡产生 | 猜想不成立 |
| 丙 | 取少量固体C,溶于适量水形成溶液后,滴加几滴饱和Na2CO3溶液 | _____ | 猜想成立 |
[反思与评价]同学们认真研究实验流程,讨论后一致认为乙、丙两位同学的方案、现象和推理均正确,请你根据实验流程对甲同学设计的方案进行合理的评价:_____。
-
自然界的矿物中有一种重晶石矿的主要成分是BaSO4,它不溶于任何酸、碱和水,纯净的硫酸钡可供医疗等方面应用,某课外活动小组同学,用重晶石和焦炭为原料,制取纯净硫酸钡,部分流程如下(设矿物中杂质不与焦炭反应,也不溶于水):
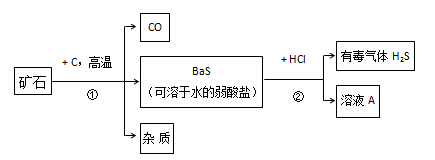
按要求填空:
(1)在步骤①中,哪些元素的化合价升高了,哪些元素化合价降低了?__________________。
(2)写出步骤②溶液A中溶质的化学式:_________________________。
(3)写出利用溶液A中的溶质主要原料制取Ba(OH)2 的化学方程式:_________________。
(4)有同学指出,上述步骤②产生有毒气体H2S,应将方法加以改进,请你提出改进意见,使该实验既不产生H2S又能获得纯净BaSO4,并写出有关反应的化学方程式。
-
食醋、纯碱、食盐均为家庭府房中常用的物质,利用这些物质,不能完成的实验是( )
A.除去热水瓶中的水垢 B.鉴别氯化钙和硝酸钙
C.检验贝壳能否溶于酸 D.检验久置的烧碱是否变质
-
以菱镁矿(主要成分是碳酸镁,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体(MgSO4·7H2O)的流程如下:

(1)“氧化”的过程目的是在酸性溶液中将Fe2+氧化为易被除去的离子,该过程发生反应的离子方程式是 _______________。
(2)“氧化”后的溶液与氨水反应生成的沉淀的化学式________,其颜色是_______。
(3)“过滤”所得滤液中含有的阳离子主要有______和______。
-
我国化学侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下:
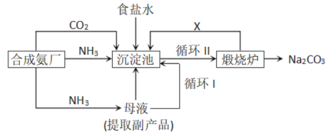
(1)实验室制取氨气的反应方程式为______
(2)上述生产纯碱过程副产品是______。
(3)沉淀池中发生的化学反应方程式是______。
(4)写出上述流程中X物质的电子式______。
(5)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了______(选填循环Ⅰ或循环Ⅱ)的循环。从沉淀池中取出沉淀的操作是_________。
(6)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加________。
-
硫酸镁晶体(MgSO4·7H2O)是一种重要的化工原料。以菱镁矿(主要成分是MgCO3,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体的流程如下:

(1)MgCO3溶于稀硫酸的离子方程式是_________________________。
(2)加入H2O2溶液的目的是____________________(用离子方程式表示)。
(3)已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Mg2+ | Fe2+ | Fe3+ |
| 开始沉淀 | 9.1 | 7.6 | 1.9 |
| 完全沉淀 | 11.1 | 9.7 | 3.2 |
“沉淀”步骤中,用氨水调节溶液pH的范围是______________________________。
(4)“过滤”所得滤液中存在大量的阳离子有Mg2+、____________。
(5)“结晶”步骤中需蒸发浓缩滤液,使用的仪器有铁架台、酒精灯和_________________。
-
氢氧化钾是我国古代纺织业常用的洗涤剂,古人常用贝壳(主要成分是碳酸钙)灼烧后的固体与草木灰在水中相互作用,生成氢氧化钾。在上述反应过程中没有涉及的化学反应基本类型是
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
-
铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制铵明矾晶体的工艺流程如图所示:
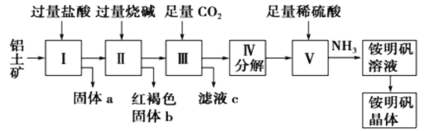
请回答下列问题:
(1)固体a的化学式为___,固体b化学式为___,Ⅲ中通入足量CO2气体发生反应的离子方程式为___。
(2)由Ⅴ制取铵明矾溶液的化学方程式为___。
(3)由I→II→III→IV都要用到的分离方法是___,由铵明矾溶液中制铵明矾晶体的操作是___,___,过滤,洗涤,干燥保存。
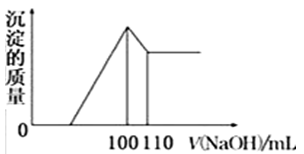
(4)向10gFe2O3、SiO2和Al2O3的混合物中,加入100mL稀硫酸,过滤后,向滤液中加入10mol/LNaOH溶液,产生沉淀的质量和加入NaOH溶液体积的关系曲线如图所示。则混合物中三氧化二铝的质量分数为___。
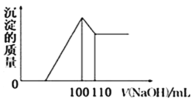
(5)有一种含铁、硅等元素的矿石,其主要成分的化学式为Na2Fe5(OH)2Si8O22,该物质中+2价铁与+3价铁的物质的量之比为___。将mg该矿石用足量的酸溶解后,加入过量铜粉使溶液中的铁元素全部变为Fe2+,过滤后滤液用cmol/L的KMnO4酸性溶液与Fe2+反应,用去VmL溶液。该矿石中铁元素的质量分数为___(用含m、c、V的代数式表示)。
-
铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制铵明矾晶体的工艺流程如图所示:
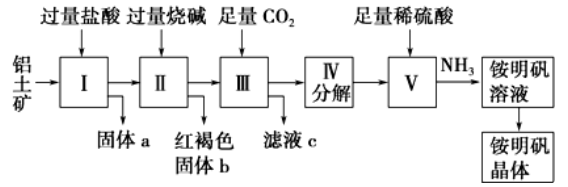
请回答下列问题:
(1)固体a的化学式为____,固体b化学式为____,Ⅲ中通入足量CO2气体发生反应的离子方程式为________________.
(2)由Ⅴ制取铵明矾溶液的化学方程式为______________.
(3)由I→II→III→IV都要用到的分离方法是______,由铵明矾溶液中制铵明矾晶体的操作是______________.
(4)如果先向铝土矿加入过量氢氧化钠,再加入过量盐酸,此时首先出现的固体a是__.
(5)向10gFe2O3、SiO2和Al2O3的混合物中,加入100ml稀硫酸,过滤后,向滤液中加入10mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积的关系曲线如图所示.则混合物中三氧化二铝的质量分数为______.
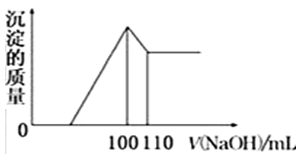
-
铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制铵明矾晶体的工艺流程如图所示:

请回答下列问题:
(1)固体a的化学式为____,固体b化学式为____,Ⅲ中通入足量CO2气体发生反应的离子方程式为________________.
(2)由Ⅴ制取铵明矾溶液的化学方程式为______________.
(3)由I→II→III→IV都要用到的分离方法是______,由铵明矾溶液中制铵明矾晶体的操作是______________.
(4)如果先向铝土矿加入过量氢氧化钠,再加入过量盐酸,此时首先出现的固体a是__.
(5)向10gFe2O3、SiO2和Al2O3的混合物中,加入100ml稀硫酸,过滤后,向滤液中加入10mol/L NaOH溶液,产生沉淀的质量和加入NaOH溶液体积的关系曲线如图所示.则混合物中三氧化二铝的质量分数为______.