如图,在锌、铜和稀硫酸组成的原电池中,正极发生的反应是
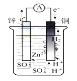
A.Zn - 2e- = Zn2+ B.Cu - 2e- = Cu2+ C.2H+ + 2e- = H2↑ D.Cu2+ + 2e- = Cu
高二化学单选题简单题
如图,在锌、铜和稀硫酸组成的原电池中,正极发生的反应是

A.Zn - 2e- = Zn2+ B.Cu - 2e- = Cu2+ C.2H+ + 2e- = H2↑ D.Cu2+ + 2e- = Cu
高二化学单选题简单题
用锌片、铜片和稀硫酸组成的原电池,正极上发生的电极反应是
A. 2H++2e-=H2↑ B. Zn-2e-=Zn2+
C. 2H2O+O2+4e-=4OH- D. Cu2++2e-=Cu
高二化学选择题中等难度题查看答案及解析
以铜锌为电极,稀硫酸为电解质溶液组成的原电池如图,对其说法正确的是
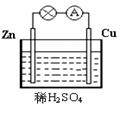
A.负极反应为Zn2++2e-=Zn B.Cu电极上产生无色无味气泡
C.正极反应是Cu2++2e-=Cu D.溶液慢慢变成蓝色
高二化学选择题简单题查看答案及解析
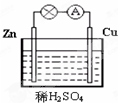
高二化学选择题中等难度题查看答案及解析
铜、锌、稀硫酸、导线可组成原电池,则负极上发生的反应是
A. Cu-2e-=Cu2+ B. Zn-2e-=Zn2+ C. 2H2O+O2+4e-=4OH- D. 2H++2e-=H2
高二化学单选题中等难度题查看答案及解析
由铜、锌和稀硫酸组成的原电池中,下列各叙述正确的是( )
A.溶液中pH由大变小
B.溶液中的SO42-向原电池的正极移动
C.Zn为电池的负极,电极反应:Zn – 2e- == Zn2+
D.在该电池的外电路导线中电子是从铜流向锌
高二化学选择题中等难度题查看答案及解析
Cu﹣Zn稀硫酸组成原电池装置,当导线中有0.5mol电子通过时,理论上两极的变化是
①锌极反应:Zn﹣2e﹣=Zn2+,锌片上产生0.25mol的H2
②铜极反应:2H++2e﹣=H2↑,锌片溶解16.25g
③电流由铜极经导线流向锌极
④溶液中SO42﹣移向铜极.
A.①④ B.③④ C.②③ D.①③
高二化学选择题中等难度题查看答案及解析
如图是Zn和Cu形成的原电池,下列说法正确的是( )

A.正极发生氧化反应
B.SO向负极移动
C.电子是由Zn片通过溶液流向Cu片
D.正极的电极反应式为Zn-2e-=Zn2+
高二化学单选题简单题查看答案及解析
如图为某原电池的结构示意图,下列说法正确的是
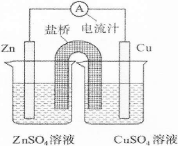
A.原电池工作时,电子从铜极流向锌极
B.原电池工作时,铜电极上发生氧化反应
C.正极反应为Zn—2eˉ=Zn2+
D.原电池工作时的总反应为Zn+Cu2+=Zn2++Cu,该反应一定为放热反应
高二化学选择题中等难度题查看答案及解析
在下图所示的原电池中,正极发生的反应是( )
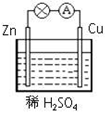
A.H2-2e- ==2H+ B.Cu-2e- == Cu2+
C.2H+ + 2e- == H2↑ D.Zn-2e- == Zn2+
高二化学选择题简单题查看答案及解析
如图是Zn和Cu形成的原电池,则下列结论中正确的是
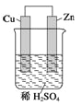
①铜为负极,锌为正极;②铜极上有气泡;③SO42-向铜极移动;④锌发生还原反应;⑤电子的流向是铜到锌;⑥负极反应式:Zn-2e-=Zn2+
A. ①② B. ①④⑥
C. ②④⑥ D. ②⑥
高二化学单选题简单题查看答案及解析