-
Cu﹣Zn稀硫酸组成原电池装置,当导线中有0.5mol电子通过时,理论上两极的变化是
①锌极反应:Zn﹣2e﹣=Zn2+,锌片上产生0.25mol的H2
②铜极反应:2H++2e﹣=H2↑,锌片溶解16.25g
③电流由铜极经导线流向锌极
④溶液中SO42﹣移向铜极.
A.①④ B.③④ C.②③ D.①③
高二化学选择题中等难度题查看答案及解析
-
Cu与Zn用导线连接后浸入稀硫酸组成原电池装置。当导线中有0.5mol电子通过时,理论上两极的变化正确的是
A.锌为负极,锌片溶解32.5g
B.铜为正极,铜片上产生0.25mol的H2
C.电子由铜极经导线流向锌极
D.溶液中SO42-定向移向铜极
高二化学选择题中等难度题查看答案及解析
-
对于锌—铜—稀H2SO4组成的原电池装置中,当导线中有1 mol 电子通过时,理论上的两极变化是( )
①锌片溶解了32.5 g ②锌片增重32.5 g
③铜片上析出1 g H2 ④铜片上析出1 mol H2
A.①和③ B.①和④ C.②和③ D.②和④
高二化学选择题简单题查看答案及解析
-
如图由锌—铜—稀H2SO4组成的原电池装置中,当导线中有0.2 mol电子通过时,理论上两极的变化是( )
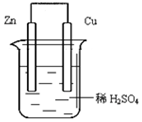
A.铜片增重6.4g B.锌片增重6.5 g
C.铜片上析出0.1 mol O2 D.锌片溶解了6.5 g
高二化学选择题简单题查看答案及解析
-
如图由锌—铜—稀H2SO4组成的原电池装置中,当导线中有0.2 mol电子通过时,理论上两极的变化是
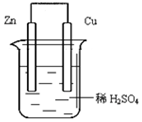
A.铜片增重6.4g B.锌片增重6.5 g
C.铜片上析出0.1 mol O2 D.锌片溶解了6.5 g
高二化学选择题中等难度题查看答案及解析
-
由锌—铜—稀H2SO4组成的原电池装置中,当导线中有0.2 mol电子通过时,理论上两极的变化是
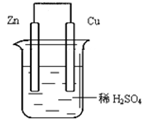
A.铜片增重6.4g B.锌片增重6.5 g
C.铜片上析出0.1 mol O2 D.锌片溶解了6.5 g
高二化学选择题中等难度题查看答案及解析
-
在铜一锌一硫酸构成的原电池中,当导线中有1mol电子通过时,理论上的两极变化是
A.锌片增重32.5g B.锌片溶解32.5g
C.铜片上析出2gH2 D.铜片上析出1mol H2
高二化学选择题简单题查看答案及解析
-
在铜一锌一稀硫酸构成的原电池中,当导线中有1mol电子通过时,理论上的两极变化是
①锌片溶解32.5g ②锌片增重32.5g ③铜片上析出1 gH2 ④铜片上析出1mol H2
A.①③ B.①④ C.②③ D.②④
高二化学选择题中等难度题查看答案及解析
-
在铜一锌一硫酸构成的原电池中,当导线中有1mol电子通时,理论上的两极变化是
①锌片溶解32.5g ②锌片增重32.5g ③铜片上析出1 gH2 ④铜片上析出1mol H2
A. ①③ B. ①④ C. ②③ D. ②④
高二化学选择题中等难度题查看答案及解析
-
在铝—铜—浓硝酸原电池中,当导线中有1mol电子通时,理论上的两极变化是
①铝片溶解9g ②铜片溶解32g ③铜片上析出1 gH2 ④铝片上析出1mol NO2
A.①③ B.①④ C.②③ D.②④
高二化学选择题中等难度题查看答案及解析