-
(12分))氮是一种地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。(1)上图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式。
(2)已知:N2(g)+ O2(g)= 2 NO(g) △H = +180 kJ • mol-1
2NO(g)+2 CO(g)= N2(g) + 2 CO2(g) △H = - 746 kJ • mol-1
则反应CO(g) + O2(g) = CO2(g)的 △H = ________ kJ • mol-1
O2(g) = CO2(g)的 △H = ________ kJ • mol-1
(3)在一固定容积为2L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应: N2(g)+3H2(g) 2NH3(g) △H <0, 若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为________,该反应的平衡常数表达式K =________。
2NH3(g) △H <0, 若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为________,该反应的平衡常数表达式K =________。
(4) 在固定体积的密闭容器中,1.0×103 kPa时反应 N2(g)+3H2(g) 2NH3(g)
2NH3(g)
△H<0 的平衡常数K与温度T的关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 51 | K1 | K2 |
①K1________K2(填写“>”、“=”或“<”)
②下列各项能说明上述合成氨反应一定达到平衡状态的是________(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.NH3的浓度保持不变
c.容器内压强保持不变 d.混合气体的密度保持不变
-
(9分)氮是一种地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。
(1)下图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式________。
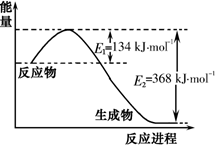
(2)已知:N2(g)+ O2(g)= 2 NO(g) △H = +180 kJ • mol-1
2NO(g)+2 CO(g)= N2(g) + 2 CO2(g) △H = - 746 kJ • mol-1
则反应CO(g) + O2(g) = CO2(g)的 △H = ________ kJ • mol-1
O2(g) = CO2(g)的 △H = ________ kJ • mol-1
(3)在一固定容积为2L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应: N2(g)+3H2(g) 2NH3(g) △H <0, 若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为________,该反应的平衡常数表达式K =________。
2NH3(g) △H <0, 若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为________,该反应的平衡常数表达式K =________。
(4) 在固定体积的密闭容器中,1.0×103 kPa时反应 N2(g)+3H2(g) 2NH3(g)
2NH3(g)
△H<0 的平衡常数K与温度T的关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 51 | K1 | K2 |
①K1________K2(填写“>”、“=”或“<”)
②下列各项能说明上述合成氨反应一定达到平衡状态的是________(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.NH3的浓度保持不变
c.容器内压强保持不变 d.混合气体的密度保持不变
-
(5分)氮是一种地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。
(1)下图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式________

(2) 自1913年工业合成氨投产以来,合成氨工业不断发展,氨又可以进一步制备硝酸,在工业上可进行连续生产。
请回答下列问题:
(1)已知: ①N2(g)+O2(g)=2NO(g) △H1= +180.5kJ/mol
②N2(g)+3H2(g) 2NH3(g) △H2=-92.4kJ/mol
2NH3(g) △H2=-92.4kJ/mol
③2H2(g)+O2(g)=2H2O(g) △H3=-483.6kJ/mol
写出氨气经催化氧化生成一氧化氮气体和水蒸气的热化学方程式:
________
-
氮是一种地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。
(1)下图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式。

(2)已知:N2(g)+ O2(g)=2 NO(g) △H=+180 kJ • mol-1
2NO(g)+2 CO(g)=N2(g) + 2 CO2(g) △H=-746 kJ • mol-1
则反应CO(g) + O2(g)=CO2(g)的 △H= ________ kJ • mol-1。
O2(g)=CO2(g)的 △H= ________ kJ • mol-1。
(3)在一固定容积为2L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应: N2(g)+3H2(g) 2NH3(g) △H <0, 若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为________。
2NH3(g) △H <0, 若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为________。
(4)在固定体积的密闭容器中,1.0×103 kPa时,发生反应 N2(g)+3H2(g) 2NH3(g) △H<0,其平衡常数K与温度T的关系如下表:
2NH3(g) △H<0,其平衡常数K与温度T的关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 51 | K1 | K2 |
① K1________K2(填写“>”、“=”或“<”)
②下列各项能说明上述合成氨反应一定达到平衡状态的是(填字母)。
a、容器内N2、H2、NH3的浓度之比为1:3:2
b、NH3的浓度保持不变
c、容器内压强保持不变
d、混合气体的密度保持不变
-
(14分)氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。
(1)下图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式________。(2分)

(2)已知:
N2(g)+O2(g)=2 NO(g) △H=+180 kJ·mol-1
2NO(g)+2 CO(g)=N2(g)+2 CO2(g)△H=-746 kJ·mol-1
则反应CO(g)+1/2O2(g)=CO2(g)的△H=________kJ·mol-1 (2分)
(3)在一固定容积为2L的密闭容器内加人0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应。N2(g)+3H2(g) 2NH3(g)△H<0,若第5分钟时达到平衡,此时测得NH3的物质的量为0.2mol,则前5分钟的平均反应速率v(N2)为________,平衡时H2的转化率为________,该反应的平衡常数K=________。(6分)
2NH3(g)△H<0,若第5分钟时达到平衡,此时测得NH3的物质的量为0.2mol,则前5分钟的平均反应速率v(N2)为________,平衡时H2的转化率为________,该反应的平衡常数K=________。(6分)
(4)在固定体积的密闭容器中,1.0×103kPa时,反应N2(g)+3H2(g) 2NH3(g) △H<0的平衡常数K与温度T的关系如下表:
2NH3(g) △H<0的平衡常数K与温度T的关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 51 | K1 | K2 |
则K1________K2(填写“>”、“=”或“<”)(2分)
(5)在体积一定的密闭容器中能说明合成氨反应一定达到平衡状态的是________
(填字母)(2分)
a. 容器内N2、H2、NH3的浓度之比为1:3:2 b. NH3的浓度保持不变
c. 容器内压强保持不变 d.. 混合气体的密度保持不变
-
氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。
(1)下图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式_______________________________________。

(2)已知:N2(g)+ O2(g)= 2 NO(g) △H=+180 kJ • mol-1,2NO(g)+2 CO(g)= N2(g)+2 CO2(g) △H = - 746 kJ•mol-1,则反应CO(g) +1/2O2(g)= CO2(g)的△H=_______ kJ•mol-1。
-
氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活有着重要意义。
(1)下图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式____________________。

(2)已知:
N2(g)+O2(g)=2 NO(g) △H=+180 kJ·mol-1
2NO(g)+2 CO(g)=N2(g)+2 CO2(g)△H=-746 kJ·mol-1
则反应CO(g)+1/2O2(g)=CO2(g)的△H=________kJ·mol-1。
(3)在一固定容积为2L的密闭容器内加人0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应。N2(g)+3H2(g) 2NH3(g)△H<0,若第5min时达到平衡,此时测得NH3的物质的量为0.2mol,则前5min的平均反应速率v(N2)为_________,平衡时H2的转化率为_________,该反应的平衡常数K=__________(计算结果保留一位小数)。
2NH3(g)△H<0,若第5min时达到平衡,此时测得NH3的物质的量为0.2mol,则前5min的平均反应速率v(N2)为_________,平衡时H2的转化率为_________,该反应的平衡常数K=__________(计算结果保留一位小数)。
(4)在固定体积的密闭容器中,1.0×103kPa时,反应N2(g)+3H2(g) 2NH3(g) △H <0的平衡常数K与温度T的关系如下表:则K1_________K2(填写“>”、“=”或“<”)
2NH3(g) △H <0的平衡常数K与温度T的关系如下表:则K1_________K2(填写“>”、“=”或“<”)
| T/K | 298 | 398 | 498 |
| 平衡常数K | 51 | K1 | K2 |
(5)在体积一定的密闭容器中能说明合成氨反应一定达到平衡状态的是____(填字母)
a.容器内N2、H2、NH3的浓度之比为1︰3︰2
b.NH3的浓度保持不变
c.容器内压强保持不变
d.混合气体的密度保持不变
-
氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。
(1)下图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式___________________。
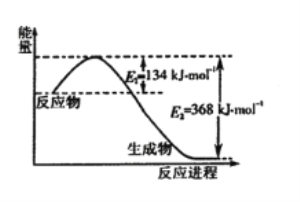
(2)已知:N2(g)+O2(g)=2 NO(g) △H=+178 kJ·mol-1
2NO(g)+2 CO(g)=N2(g)+2 CO2(g)△H=-743kJ·mol-1
则反应CO(g)+1/2O2(g)=CO2(g)的△H=_______kJ·mol-1
(3)在一固定容积为2L的密闭容器内加入1.5 mol的N2和5 mol的H2,在一定条件下发生如下反应:N2+3H2 2NH3,若第5分钟时达到平衡,此时测得NH3的物质的量为2mol,则前5分钟的平均反应速率υ(N2)为_________,平衡时H2的转化率为_________,该反应的平衡常数K=__________。
2NH3,若第5分钟时达到平衡,此时测得NH3的物质的量为2mol,则前5分钟的平均反应速率υ(N2)为_________,平衡时H2的转化率为_________,该反应的平衡常数K=__________。
(4)在体积一定的密闭容器中能说明合成氨反应一定达到平衡状态的是_____;在压强一定的密闭容器中能说明合成氨反应一定达到平衡状态的是_____
a. 容器内N2、H2、NH3的浓度之比为1:3:2 b. NH3的浓度保持不变
c. 容器内压强保持不变 d. 混合气体的密度保持不变
-
氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.
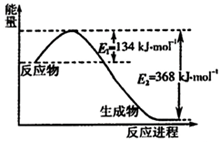
(1)如图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式______.若在反应体系中加入催化剂使反应速率增大,则E1的变化是______,该反应的反应热△H______(填“增大”“减小”或“不变”).
(2)已知:N2(g)+O2(g)=2NO(g)△H=+180kJ•mol-1
2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=-746kJ•mol-1
则反应CO(g)+ O2(g)=CO2(g)的△H=______kJ•mol-1
O2(g)=CO2(g)的△H=______kJ•mol-1
(3)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:N2(g)+3H2O(l)=2NH3(g)+ O2(g)△H=a kJ•mol-1
O2(g)△H=a kJ•mol-1
为进一步研究NH3生成量与温度的关系,测得常压下达到平衡时部分实验数据如下表:
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
此合成反应中,a______0;△s______0,(填“>”、“<”或“=”)
(4)在一固定容积为2L的密闭容器内加人2mol NH3和3mol O2,发生反应4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g),2min后达到平衡,生成1.2mol NO.则前2分钟的平均反应速率v(NH3)为______,平衡时O2的转化率为______,该反应平衡常数的表达式K=______.
(5)某温度下,体积均为0.25L的两个恒容密闭容器中发生下列反应:N2(g)+3H2(g)  2NH3(g)△H=-92.4kJ•mol-1,实验测得反应起始时、达到平衡时的有关数据如下表所示:
2NH3(g)△H=-92.4kJ•mol-1,实验测得反应起始时、达到平衡时的有关数据如下表所示:
容器
编号 | 起始时各物质的物质的量/mol | 反应达平衡时的焓变/kJ•mol-1 |
| N2 | H2 | NH3 |
| A | 1 | 3 | | △H1=-23.1 |
| B | 0.9 | 2.7 | 0.2 | △H2 |
容器B中反应达到平衡状态时的反应热△H2=______.
-
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。
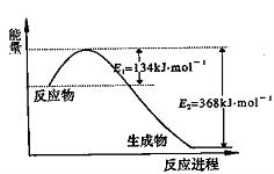
(1)上图是1 mol NO2气体和1 mol CO气体反应生成CO2气体和NO气体过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: ;
已知:N2 (g)+2NO2 (g)  4NO(g) △H=+292.3kJ·mol—1,
4NO(g) △H=+292.3kJ·mol—1,
则反应: 2NO(g)+2CO(g) N2(g)+2CO2(g) 的△H= ;
N2(g)+2CO2(g) 的△H= ;
(2)一定温度下,在体积为2L的恒容密闭容器中充入20 mol NO2和5 mol O2发生反应: 4NO2(g)+O2(g) 2N2O5(g);已知体系中n(NO2)随时间变化如下表:
2N2O5(g);已知体系中n(NO2)随时间变化如下表:
| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |
①写出该反应的平衡常数表达式:K= ,已知:K3000C>K3500C,则该反应是 反应(填“放热”或“吸热”);
②反应达到平衡后,NO2的转化率为 ,若要增大NO2的转化率,可采取的措施有
A.降低温度
B.充入氦气,使体系压强增大
C.再充入NO2
D.再充入4 mol NO2和1 mol O2
③图中表示N2O5的浓度的变化曲线是 ,用O2表示从0~500s内该反应的平均速率v= 。

O2(g) = CO2(g)的 △H = ________ kJ • mol-1
2NH3(g) △H <0, 若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为________,该反应的平衡常数表达式K =________。
2NH3(g)









