-
金属钛被称为铁和铝之后崛起的“第三金属”,常见化合价为+4。它是空间技术、航海、化工、医疗上不可缺少的材料。
工业上用钛铁矿(主要成分FeTiO3)制备金属钛的一种工艺流程如下图(部分产物略去):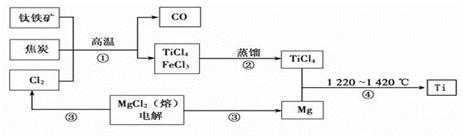
(1)步骤①反应的化学方程式为:2FeTiO3 + 6C + 7Cl2 2FeCl3 + 2TiCl4 + 6CO,还 原剂是 ________ ________ ,每生成1mol TiCl4转移________mol电子。
2FeCl3 + 2TiCl4 + 6CO,还 原剂是 ________ ________ ,每生成1mol TiCl4转移________mol电子。
(2)步骤②分离出TiCl4的方法,利用了TiCl4与FeCl3 ________的不同。
(3)步骤④反应的化学方程式为________________________________,该反应在氩气中进行的理由是______________________________________。
(4)绿色化学提倡物料循环。以上流程中,可用于循环的物质除Cl2、Mg外,还有___。
-
(14分)金属钛被称为铁和铝之后崛起的“第三金属”,常见化合价为+4。它是空间技术、航海、化工、医疗上不可缺少的材料。
Ⅰ.工业上用钛铁矿(主要成分FeTiO3)制备金属钛的一种工艺流程如下图(部分产物略去):
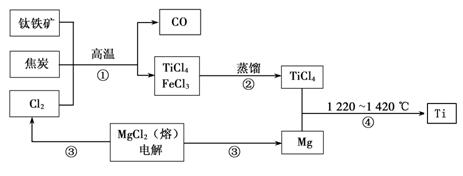
(1)步骤①反应的化学方程式为:2FeTiO3 + 6C + 7Cl2 2FeCl3 + 2TiCl4 + 6CO,还原剂是。
2FeCl3 + 2TiCl4 + 6CO,还原剂是。
(2)步骤②分离出TiCl4的方法,利用了TiCl4与FeCl3________的不同。
(3)步骤④反应的化学方程式为________________________________,该反应在氩气中进行的理由是______________________________________。
(4)绿色化学提倡物料循环。以上流程中,可用于循环的物质除Cl2、Mg外,还有____________。
II. 工业上也可用TiO2通过下述两种方法制备金属钛:
方法一:先将TiO2氯化为TiCl4,再还原得到Ti。
(5)氯化反应TiO2 (s) +2Cl2 (g)  TiCl4(l) + O2 (g) 无法自发正向进行,在反应器中加入碳,则在高温条件下反应可顺利进行。试从化学平衡角度解释,往氯化反应器中加碳的原因:________。
TiCl4(l) + O2 (g) 无法自发正向进行,在反应器中加入碳,则在高温条件下反应可顺利进行。试从化学平衡角度解释,往氯化反应器中加碳的原因:________。
方法二:以熔融盐为电解液电解TiO2获得Ti。其中,碳块为阳极,电极反应式为:2O2ˉ– 4eˉ=O2↑;TiO2作阴极,被还原。
(6)阴极的电极反应式为。
(7)电解过程中需定期向电解槽中加入碳块的原因是________。
-
(15分)金属钛被称为铁和铝之后崛起的第三金属,它是空间技术、航海、化工、医疗上不可缺少的材料。
I、工业上用钛矿石(FeTiO3,含FeO、Al2O3、SiO2等杂质)经过下述反应制得:

其中,步骤②发生的反应为:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O。
(1)净化钛矿石时,是否需要除去杂质FeO?答:_________(填“需要”或“不需要”)
(2)净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中发生反应的离子方程式________。
II、为了提高资源的利用率,减少环境污染,可将氯碱厂、炼钛厂和甲醇厂组成产业链,其关系如下图所示。
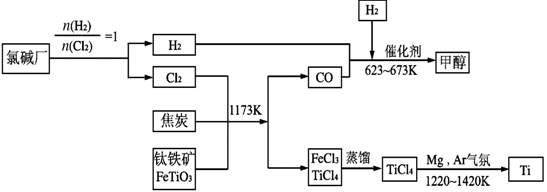
(3)写出钛铁矿经氯化法得到四氯化钛的化学方程式_________________________。
(4)已知:①Mg(s)+Cl2(g)=MgCl2(s);△H=一641 kJ·mol-1
②1/2Ti(s)+Cl2(g)=1/2TiCl4(l);△H=一385 kJ·mol-1
则Mg 与TiCl4反应的热化学方程式为________,
该反应在氩气氛中进行的理由是________。
(5)在上述产业链中,合成192 t 甲醇理论上需额外补充H2t (不考虑生产过程中物质的任何损失)。
-
金属钛被称为铁和铝之后崛起的第三金属,它是空间技术、航海、化工、医疗上不可缺少的材料.为了提高资源的利用率,减少环境污染,可将氯碱厂、炼钛厂和甲醇厂组成产业链,其关系如下图所示.
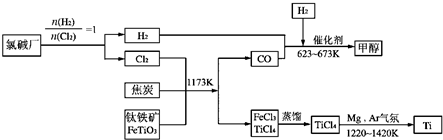
请回答下列问题:
(1)写出钛铁矿经氯化法得到四氯化钛的化学方程式______.
(2)TiCl4暴露在潮湿空气中冒白烟,白烟主要为白色的二氧化钛的水合物H2TiO3,试写出该反应的化学方程式:______.
(3)已知:①Mg(s)+Cl2(g)=MgCl2(s)△H=-641kJ•mol-1
② Ti(s)+Cl2(g)=
Ti(s)+Cl2(g)= TiCl4(l)△H=-385kJ•mol-1
TiCl4(l)△H=-385kJ•mol-1
则Mg 与TiCl4反应的热化学方程式为______,该反应在氩气氛中进行的理由是______.
(4)在上述产业链中,合成96t 甲醇理论上需额外补充H2______t (不考虑生产过程中物质的任何损失).
-
金属钛被称为铁和铝之后崛起的第三金属,它是空间技术、航
 海、化工、医疗上不可缺少
海、化工、医疗上不可缺少
的材料。为了提高资源的利
用率,减少环境污染,可将
氯碱厂、炼钛厂和甲醇厂组
成产业链,其关系如下图所
示。请回答下列问题:
(1)写出钛铁矿经氯化法得到四氯化钛的化学方程式_________________________。
(2)TiCl4暴露在潮湿空气中冒白烟,白烟主要为白色的二氧化钛的水合物H2TiO3,试写出该反应的化学方程式:_________________________________。
(3)已知:①Mg(s)+Cl2(g)=MgCl2(s) △H=一641 kJ·mol-1
②1/2Ti(s)+Cl2(g)=1/2TiCl4(l) △H=一385 kJ·mol-1
则Mg 与TiCl4反应的热化学方程式为________,
该反应在氩气氛中进行的理由是。
(4)在上述产业链中,合成96 t 甲醇理论上需额外补充H2________t (不考虑生
产过程中物质的任何损失)。
-
金属钛被用于航空航天工业、化工、医疗等领域。用钛铁矿(主要成份为FeTiO3) 制取钛并获得副产品绿矾的工艺流程如下:

(1)TiOSO4中钛的化合价为_________,操作I的名称是为_________。
(2)TiOSO4经水解得H2TiO3的化学方程式为_________。
(3)TIO2与焦炭和Cl2在高温下反应得TiCl4井产生还原性气体,相应的化学方程式为_________。
(4)加热Mg与TiCl4得到钛时,Ar的作用是_________。
(5)某厂用3.8吨纯度为40%的钛铁矿制取钛,理论上至少需要氯气______L(标准状况下)。
(6)已知K3[Fe(CN)6](铁氰化钾》和K4[Fe(CN)6]( 亚铁氰化钾)能发生如下反应:3Fe2++ 2[Fe(CN)6]3-= Fe3[Fe(CN)6]2↓(蓝色沉淀),4Fe3++ 3(Fe(CN)6]4-= Fe4[Fe(CN)6]3↓(蓝色沉淀)
①确定绿矾部分被氧化的方法是___________________________。(可供选择的试剂:铁氰化钾溶液、亚铁氧化钾溶液。铁粉、KSCN溶液)
②室温下,将绿矾配成0.1mol·L-1FeSO4溶液,测得溶液的pH=3,请用离子方程式解释原因_____________________,该溶液中c(SO42- )-c(Fe2+)≈_________________ mol·L-1。
-
钒被称为“现代工业味精”,是发展现代工业、现代国防和现代科学技术不可缺少的重要材料。常见的钒氧化物为VO、V2O3、VO2、V2O5,低价氧化钒在空气中易被氧化成高价氧化钒。
请回答下列问题:
(1)已知:
①2V(s)+O2(g)=2VO(s) △H1=-825.6kJ·mol-1
②4VO(s)+O2(g)=2V2O3(s) △H2=-788.8kJ·mol-1
③V2O3(s)+O2(g)=V2O5(s) △H3=-334.6kJ·mol-1
④4V(s)+5O2(g)=2V2O5(s) △H4
据上述反应热效应之间的关系,可知△H4=___。
(2)V2O5是钒氧化物中最重要的,也是最常用的钒化工制品。工业上制备V2O5的一个方法是利用VOCl3水解,则VOCl3中V的化合价为___,水解反应的化学方程式为___。
(3)工业上由V2O5冶炼金属钒常用铝热法,该反应的化学方程式为___。
(4)工业制硫酸常用V2Os作催化剂,已知2SO2(g)+O2(g) 2SO3(g) △H=-196kJ·mol-1,500℃时将2molSO2和1molO2装入一容积恒定的10L密闭容器中,达到平衡时容器中SO3的浓度为0.1mol·L-1。
2SO3(g) △H=-196kJ·mol-1,500℃时将2molSO2和1molO2装入一容积恒定的10L密闭容器中,达到平衡时容器中SO3的浓度为0.1mol·L-1。
①该反应的平衡常数K=___。某温度时,该反应的平衡常数K=50,则该温度___(填“>”“<”或“=”)500℃。
②下列措施能使 的值减小的是___(填字母)。
的值减小的是___(填字母)。
A.升温
B.其他条件不变,再充入2molHe
C.其他条件不变,再充入2molSO2和1molO2
D.不用V2O5作催化剂,改用其他更高效的催化剂
(5)酸性条件下,V2O5和亚硫酸钠发生氧化还原反应生成可溶性的VOSO4,请写出该反应的离子方程式:___。
-
钛被称为继铁、铝之后的第三金属,其单质及化合物在航天、军事、航海、医疗等领域都有着重要的应用。请回答下列问题:
(1)基态Ti 原子的价层电子排布图为________________________。
(2)在TiO、TiN、TiS2、TiCl4等化合物中,S、Cl的电负性大小:S________Cl (填“>”、“<”或“=”)。O、N 的第一电离能大小为O < N,原因是___________________________。
(3)TiCl4的熔点是-23℃,沸点是136℃,可溶于CCl4,该晶体是_______ 晶体。TiCl4中加入大量水,同时加热,可制得二氧化钛的水合物(TiO2·xH2O),再经焙烧可得TiO2,写出生
成二氧化钛水合物(TiO2·xH2O)的化学方程式_________________________________。
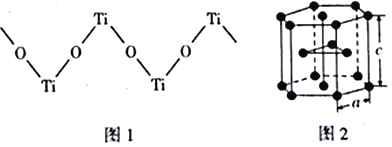
(4)TiO2能溶于浓硫酸并析出一种离子晶体,已知其中阳离子是以链状聚合物形式存在的钛酰阳离子,其结构如下图1所示,其化学式为_____________。阴离子SO42-中硫原子的杂化方式为______________,写出一种与SO42-互为等电子体的分子_____________。
(5)下图2是钛晶体在空间的一种堆积方式,此堆积方式叫______________,钛原子的配位数为____________。已知:a=0.295 nm,c=0.469nm,则该钛晶体的密度为_________g·cm-3(NA表示阿伏加德罗常数的值,列出计算式即可)。
-
金属钛在航天、潜海和医疗方面应用广泛。工业上用钛铁矿(主要成分为钛酸亚铁FeTiO3,含FeO、Fe2O3、SiO2)为原料制TiO2,再由TiO2制得金属Ti
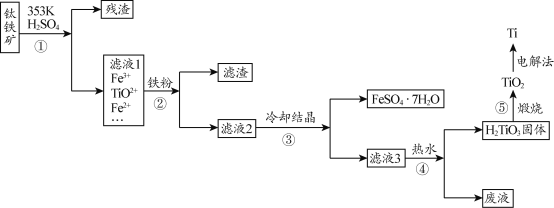
资料:TiO2+会发生水解
(1)步骤②、③、④中,均需用到的操作是_______。(填操作名称)
(2)检验滤液2中是否含Fe3+的方法是:_______。
(3)步骤1中FeTiO3溶于过量硫酸的化学方程式___________。

(4)请结合化学用语解释步骤④中加热水的原因___________。
(5)电解法获得Ti是通过图装置,以熔融CaCl2做电解质
①a为电源的_____(填“正”或“负”)
②在制备钛的过程中石墨电极附近的气泡中除了O2、CO、CO2外还可能有的气体是______________,用化学用语解释原因________________。
(6)测定废液中Fe2+浓度已确认铁元素的回收率:取25.00ml废液于锥形瓶中,用硫酸酸化的xmol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积如图所示:
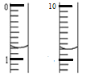
(滴定时发生反应的离子方程式为:5Fe2++MnO4-+8H+→5Fe3++Mn2++4H2O).废液中c(Fe2+)=_________
-
(本题满分18分)钛被称为“二十一世纪金属”,工业上用钛铁矿制备金属钛的工艺流程如下:
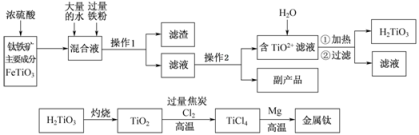
已知:钛铁矿主要成分与浓硫酸反应的主要产物是TiOSO4和FeSO4,TiOSO4遇水会水解.
请回答下列问题:
(1)操作1用到的玻璃仪器除烧杯外还有 ________________________________________________ ,操作2是 ________________ 、过滤,副产品主要成分的化学式为 ________________________________ 。
(2)请结合化学用语解释将TiO2+转化为H2TiO3的原理 ________________________ 。
(3)已知钛的还原性介于铝和锌之间,估计钛能耐腐蚀的原因之一是________________________________________________________,如果可从Na、Zn、Fe三种金属中选一种金属代替流程中的镁,那么该金属跟四氯化钛反应的化学方程式是________________________。
(4)电解TiO2来获得Ti是以TiO2作阴极,石墨为阳极,熔融CaO为电解质,用碳块作电解槽,其阴极反应的电极反应式为 ________________________________________________ 。
(5)为测定溶液中TiOSO4的含量,首先取待测钛液10mL用水稀释至100mL,加过量铝粉,充分振荡,使其完全反应:3TiO2++Al+6H+═3Ti3++AlO3++3H2O,过过滤后,取出滤液20.00mL,向其中滴加2~3滴KSCN溶液作指示剂,用 ________________________________ (填一种玻璃仪器的名称)滴加0.1000mol•L﹣1FeCl3溶液,发生Ti3++Fe3+═Ti4++Fe2+,当溶液出现红色达到滴定终点,用去了30.00mLFeCl3溶液,待测钛液中TiOSO4的物质的量浓度是________________________________________________ 。

2FeCl3 + 2TiCl4 + 6CO,还 原剂是 ________ ________ ,每生成1mol TiCl4转移________mol电子。




 海、化工、医疗上不可缺少
海、化工、医疗上不可缺少




