-
四种短周期元素的性质或结构信息如下表,请根据信息回答下列问题:
(1)C的基态原子的价电子排布式为______元素符号 元素性质或结构信息 A 原子核外L层未成对电子数最多 B 原子半径是短周期主族元素中最大的 C 地壳中含量最多的金属元素 D 原子核外有五种不同能量的电子,且最外层有2对成对电子
(2)元素A的原子核外有______种形状不同的原子轨道,该原子最外层共有______种不同运动状态的电子.
(3)D的最高价氧化物中D原子的杂化类型是______,分子的空间构型为______.
(4)B的氯化物的晶体类型是______,跟它同主族第六周期元素的氯化物相比,熔点较高的是______(填化学式),理由是______.
(5)A的每个双原子分子中含有______键,______键;与其互为等电子体微粒的化学式为______(至少写2各).高三化学解答题中等难度题查看答案及解析
-
[化学--物质结构与性质]
四种常见元素:A、B、C、D为周期表前四周期元素,原子序数依次递增,它们的性质或结构信息如下表.试根据信息回答有关问题.
(1)写出D原子的外围电子排布式______,A、B、C、D四种元素的第一电离能最小的是______(用元素符号表示).元素 A B C D 结构性质
信息基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 原子核外有两个电子层,最外层有3个未成对的电子 基态原子的M层有2对成对的p电子 其原子序数比A、B、C三种元素原子的质子数总和还少1,有+1、+2两种常见化合价
(2)B元素的氢化物的沸点比同主族相邻元素氢化物沸点______(填“高”或“低”).
(3)元素F与A相邻且同主族,它们与氧元素的成键情况如下:
在A和O之间通过双键形成AO2分子,而F和O则不能和A那样形成有限分子,原因是______.A-O A=O F-O F=O 键能(KJ/mol) 360 803 464 640
(4)往D元素的硫酸盐溶液中逐滴加入过量B元素的氢化物水溶液,可生成的配合物,该配合物中不含有的化学键是______(填序号).a.离子键 b.极性键c.非极性键d.配位键 e.金属键
(5)下列分子结构图中的“”表示上述相关元素的原子中除去最外层电子的剩余部分,“
”表示氢原子,小黑点“
”表示没有形成共价键的最外层电子,短线表示共价键.
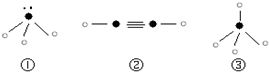
则在以上分子中,中心原子采用sp3杂化形成化学键的是______(填序号);在②的分子中有______个σ键和______个π键.
(6)已知一种分子B4分子结构如图所示,断裂1molB-B吸收aKJ的热量,生成1molB≡B放出bKJ热量.试计算反应:B4(g)═2B2(g)△H=______KJ/mol.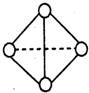
高三化学解答题中等难度题查看答案及解析
-
四种常见元素的性质或结构信息如下表。试根据信息回答有关问题。
元素
A
B
C
D
性质、结构信息
价电子数为5的短周期元素;该元素形成的双原子分子一般情况下很稳定。
基态原子的M层有1对成对的p电子。
第三周期中电离能最小的元素。
原子最外电子层上s电子数等于p电子数。
其一种单质为自然界中硬度最大的非金属单质。
(1)写出元素B基态原子的电子排布图 。
(2)元素A形成的气态氢化物的空间构型为 。(3)元素B和C形成的化合物的电子式是 。
(4)元素D形成的化合物D2H2属于 (填“极性”或“非极性”)分子。
(5)A、C、D三种元素的电负性由小到大的顺序是_________(用元素符号表示)。
高三化学填空题中等难度题查看答案及解析
-
四种短周期元素的性质或结构信息如下表,请根据信息回答下列问题.
(1)A原子的最外层电子排布式______,D原子共有______种不同运动状态的电子;元素 A B C D 性质或结构信息 单质常温下为固体,难溶于水易于溶CS2.能形成2种二元含氧酸. 原子的M层有1个未成对的p电子.核外p电子总数大于7. 单质曾被称为“银色的金子”.与锂形成的合金常用于航天飞行器.单质能溶强酸和强碱. 原子核外电子层上s电子总数比p电子总数少2个.单质和氧化物均为空间网状晶体,具有很高的熔、沸点.
(2)写出C单质与强碱反应的离子方程式______.B与C形成的化合物溶于水后,溶液的pH______7;(填“大于”、“等于”或“小于”)
(3)A,B两元素的氢化物分子中键能较小的是______;分子较稳定的是______;(填分子式)
(4)E、D同主族,位于短周期.它们的最高价氧化物中熔点较低的是______(填分子式或化学式),原因是______.高三化学解答题中等难度题查看答案及解析
-
[选修 3——物质结构与性质]
X、Y、Z、W、Q、R 均为前四周期元素,且原子序数依次增大。其相关信息如下表所示:

回答下列问题:
(1)Y 元素的基态原子的电子排布式为 ,其第一电离能比 Z 元素原子的第一电离能 (填“高”或“低”)
(2)X 的氯化物的熔点比 Q 的氯化物的熔点 (填“高”或“低”),理由是
(3)光谱证实元素 W 的单质与强碱性溶液反应有 W(OH)4]-生成,则 W(OH)4]-中存在 (填字母)
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
(4)含有 X、R 和镁三种元素的某种晶体具有超导性,其结构如下图所示。则该晶体的化学式为 ; 晶体中每个镁原子周围距离最近的 R 原子有 个。
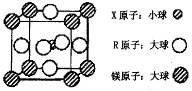
高三化学填空题困难题查看答案及解析
-
【化学—选修3:物质结构与性质】(15分)
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
A元素的核外电子数和电子层数相等,也是原子半径最小的元素
B元素原子的核外p电子数比s电子数少1
C原子的第一至第四电离能分别是:
I1=738kJ/mol I2 = 1451 kJ/mol I3 = 7733kJ/mol I4 = 10540kJ/mol
D原子核外所有p轨道全满或半满
E元素的主族序数与周期数的差为4
F是前四周期中电负性最小的元素
G在周期表的第七列
(1)已知BA5为离子化合物,写出其电子式________
(2)B基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈________形
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,
该同学所画的电子排布图违背了________
(4)G位于________族________区,价电子排布式为
(5)DE3 中心原子的杂化方式为________,用价层电子对互斥理论推测其空间构型为________
(6)检验F元素的方法是________ ,请用原子结构的知识解释产生此现象的原因是________
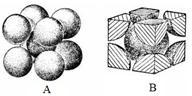
(7)F元素的晶胞如下图所示,若设该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,
F原子的摩尔质量为M,则F原子的半径为________ cm
高三化学填空题简单题查看答案及解析
-
【化学一选修3:物质结构与性质】(15分)
现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题.
A元素原子的核外p电子总数比s电子总数少1
B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期
C原子核外所有p轨道全满或半满
D元素的主族序数与周期数的差为4
E是前四周期中电负性最小的元素
F在周期表的第七列
(1)A基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈
________形
(2)某同学根据上述信息,所画的B电子排布图如图
违背了________原理。
(3)F位于________族区,其基态原子有________种运动状态。
(4)CD3 中心原子的杂化方式为________,用价层电子对互斥理论推测其分子空间构型为________.检验E元素的方法是________
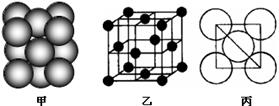
(5)若某金属单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。则晶胞中该原子的配位数为________ ,该单质晶体中原子的堆积方式为四种基本堆积方式中的________.
高三化学填空题简单题查看答案及解析
-
四种短周期元素A、B、C、D的性质或结构信息如下:
信息① 原子半径大小:A>B>C>D
信息② 四种元素之间形成的某三种分子的比例模型及部分性质:



请根据上述信息回答下列问题。
(1)B元素在周期表中的位置________;
(2)BC2分子的电子式________;
(3)A元素的单质与物质甲发生反应的离子方程式________;
(4)丙的钠盐溶液呈______性,用化学用语表示其原因________;
(5)物质丁的元素组成和甲相同,丁分子具有18电子结构。向盛有一定浓度丁溶液的试管中,逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液。滴加过程中的现象是:
①浅绿色溶液变成深棕黄色;
②有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,并放出较多热量,继续滴加溶液,静置一段时间;
③试管底部出现红褐色沉淀。向浊液中再滴入稀硫酸,沉淀溶解,溶液呈黄色。
请用化学方程式或离子方程式及必要的文字解释①、②、③中加点的字。
①________;
②________;
;
③________。
高三化学推断题困难题查看答案及解析
-
四种短周期元素A、B、C、D的性质或结构信息如下:
信息① 原子半径大小:A>B>C>D
信息② 四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题。
(1)B元素在周期表中的位置________,请写出BC2分子的电子式________。
(2)A所在周期中,E元素的单质还原性最强,F元素的某些盐类常用作净水剂。E单质与甲反应有化合物X生成。请写出以下两个反应的离子方程式。
①A元素的单质与物质甲发生的反应________。
②F、C两种元素组成的化合物Y可作为高温结构陶瓷材料,X与Y两种化合物在溶液中发生的反应________。
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构。向盛有一定浓度丁溶液的试管中,逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液。滴加过程中的现象是:
①浅绿色溶液变成深棕黄色,②有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,并放出较多热量,继续滴加溶液,静置一段时间,③试管中出现红褐色。向其中再滴入稀硫酸,红褐色变为黄色。请用化学方程式或离子方程式①、②、③中加点的字。
① ②________③________。
高三化学实验题中等难度题查看答案及解析
-
四种短周期元素A、B、C、D的性质或结构信息如下:
信息①原子半径大小:A>B>C>D
信息②四种元素之间形成的某三种分子的比例模型及部分性质:
请根据上述信息回答下列问题.
(1)B元素在周期表中的位置________;
(2)BC2分子的电子式________;
(3)A元素的单质与物质甲发生反应的离子方程式________;
(4)丙的钠盐溶液呈________性,用化学用语表示其原因________;
(5)物质丁的元素组成和甲相同,丁分子具有18电子结构.向盛有一定浓度丁溶液的试管中,逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液.滴加过程中的现象是:
①浅绿色溶液变成深棕黄色;
②有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,并放出较多热量,继续滴加溶液,静置一段时间;
③试管底部出现红褐色沉淀.向浊液中再滴入稀硫酸,沉淀溶解,溶液呈黄色.
请用化学方程式或离子方程式及必要的文字解释①、②、③中加点的字.
①________________;
②________;________;
③________.________.高三化学填空题中等难度题查看答案及解析