-
根据元素周期律及元素周期表的知识分析,下列关系中不正确的是( )
A. 酸性强弱:H3PO4>H2SO4>HClO4
B. 离子半径大小:F->Na+>Mg2+>Al3+
C. 稳定性大小:SiH4<PH3<H2S<HCl
D. 碱性强弱:NaOH>Mg(OH)2>Al(OH)3
高一化学选择题中等难度题查看答案及解析
-
根据原子结构及元索周期律的知识,下列叙述正确的是( )
A. 由于分子中氢原子数:H2SO4>HClO4,故酸性:H2SO4>HClO4
B. 由子F元素的最低化合价为-1价,故F元素的最高化合价为+7价
C. 硅处于金属与非金属的过渡位置,故硅可用作半导体材枓
D. Cl-、S2-、Ca2+、K+半径逐渐减小
高一化学选择题中等难度题查看答案及解析
-
依据元素周期表判断,下列各组关系中正确的是
A. 稳定性: NH3 > H2O > H2S
B. 氧化性: Cl2 > S > P
C. 酸性: H3PO4 > H2SO4 > HClO4
D. 碱性: Mg(OH)2 > Ca(OH)2 > Ba(OH)2
高一化学选择题简单题查看答案及解析
-
元素在周期表中的位置,反映了元素的原子结构和元素的性质。如图是元素周期表的一部分。
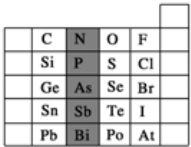
(1)阴影部分元素P在元素周期表中的位置为 。根据元素周期律预测:酸性强弱H3PO4 H3AsO4。(用“>”“<”或“=”表示)
(2)已知阴影部分As元素的原子核内质子数为33,则Sn2+ 的核外电子数为 。
(3)下列说法正确的是 。
A.C、N、O、F的原子半径随着原子序数的增大而增大
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.对于短周期元素,两种简单离子不可能相差3个电子层
D.HF、HCl、HBr、HI的还原性依次减弱
(4)在离子RO3n-中含有x个核外电子,R原子的质量数为A,则R原子中子数是 。
高一化学填空题中等难度题查看答案及解析
-
下列顺序表达正确的是()
A. 酸性强弱:H3PO4 > HNO3 > HClO4
B. 原子半径:Na > Mg > O
C. 热稳定性:H2O> HF> H2S
D. 熔点高低:NaCl>CO2> SiO2
高一化学单选题中等难度题查看答案及解析
-
在通常条件下,下列各组物质的性质排列正确的是
A.酸性:H2SO4﹥H3PO4﹥HClO4
B.水溶性:HCl﹥SO2﹥NH3
C.沸点:乙烷﹥戊烷﹥丁烷
D.氧化性:Cl2 ﹥Br2﹥I2
高一化学选择题中等难度题查看答案及解析
-
砷为第四周期 VA族元素,根据它在元素周期表中的位置推测,下列说法不正确的是
A.砷可以有-3、+3、+5等多种化合价 B.砷原子的第3电子层含有18个电子
C.H3AsO4的酸性比H3PO4弱 D.砷的氢化物的稳定性比磷化氢的强
高一化学选择题简单题查看答案及解析
-
下列说法正确的是( )
A. 原子最外层电子数为2的元素一定处于周期表IIA族
B. 原子序数相差2的两元素不可能处于同一主族
C. 可根据氢化物的稳定性和酸性强弱,来判断非金属元素得电子能力强弱
D. 非金属元素的最高化合价不超过其元素电子的最外层电子数
高一化学单选题中等难度题查看答案及解析
-
下列比较不正确的是( )
A. 酸性强弱: HClO4> H2SO4 > H3PO4 > H4SiO4 B. 原子半径大小: Na > S > O
C. 碱性强弱: KOH > NaOH > LiOH D. 还原性强弱: F- > Cl- > I-
高一化学选择题中等难度题查看答案及解析
-
砷为第4周期第ⅤA族元素,根据它在元素周期表中的位置推测,砷不可能具有的性质是( )
A. 砷在通常情况下是固体
B. 可以存在-3、+3、+5等多种化合价
C. As2O5对应水化物的酸性比H3PO4弱
D. AsH3的稳定性比PH3强
高一化学选择题中等难度题查看答案及解析