-
硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,用途十分广泛。它可以作净水剂,在无机化学工业中,它是制取其它铁化合物的原料。
【査阅资料】隔绝空气加热至500℃时硫酸亚铁铵能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。
【实验探究】某化学小组选用下图所示部分装置进行实验(部分夹持装置略)
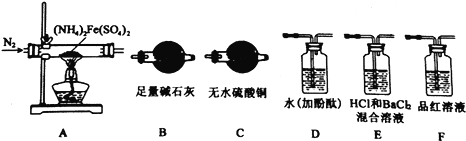
(1)验证分解产物中含有氨气和水蒸气,并探究残留固体成分。
①所选用装置的正确连接顺序为(________)。
A.A-B-C-D B.A-C-B-D C.A-D-B-C D.A-D-C-B
②取A中残留固体,加入适量稀硫酸,使其完全溶解得到溶液B,下列哪组实验能够证明A中残留固体仅为Fe2O3,而不含 FeO 或 Fe3O4(________)
A.向溶液B中滴加酸性高锰酸钾溶液,高锰酸钾溶液不褪色
B.向溶液B中加入苯酚,溶液呈紫色
C.向溶液B中通入足量氯气,加入硫氰酸钾溶液变红色
D.向溶液B中加入铁氰化钾溶液,无现象
(2)探究分解产物中的硫氧化物,连接装置A—E—F—B进行实验。
①实验过程中观察到:E中没有明显现象,F中溶液褪色,据此得出该硫化物是__________。
②实验证明(NH4)2Fe(SO4)2受热分解除上述产物外,还有N2生成,写出A中反应的化学方程式________。
-
硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,用途十分广泛。它可以作净水剂,在无机化学工业中,它是制取其它铁化合物的原料。
【査阅资料】隔绝空气加热至500℃时硫酸亚铁铵能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。
【实验探究】某化学小组选用下图所示部分装置进行实验(部分夹持装置略)
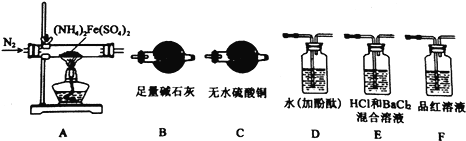
(1)验证分解产物中含有氨气和水蒸气,并探究残留固体成分。
①所选用装置的正确连接顺序为(________)。
A.A-B-C-D B.A-C-B-D C.A-D-B-C D.A-D-C-B
②取A中残留固体,加入适量稀硫酸,使其完全溶解得到溶液B,下列哪组实验能够证明A中残留固体仅为Fe2O3,而不含 FeO 或 Fe3O4(________)
A.向溶液B中滴加酸性高锰酸钾溶液,高锰酸钾溶液不褪色
B.向溶液B中加入苯酚,溶液呈紫色
C.向溶液B中通入足量氯气,加入硫氰酸钾溶液变红色
D.向溶液B中加入铁氰化钾溶液,无现象
(2)探究分解产物中的硫氧化物,连接装置A—E—F—B进行实验。
①实验过程中观察到:E中没有明显现象,F中溶液褪色,据此得出该硫化物是__________。
②实验证明(NH4)2Fe(SO4)2受热分解除上述产物外,还有N2生成,写出A中反应的化学方程式________。
-
硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,用途十分广泛。它可以作净水剂,在无机化学工业中,它是制取其它铁化合物的原料。
【査阅资料】隔绝空气加热至500℃时硫酸亚铁铵能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等。
【实验探究】某化学小组选用下图所示部分装置进行实验(部分夹持装置略)
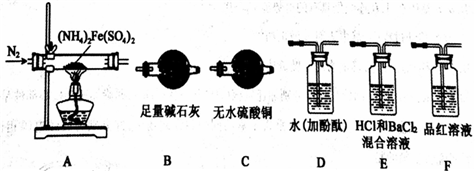
(1)验证分解产物中含有氨气和水蒸气,并探究残留固体成分。
①所选用装置的正确连接顺序为____________________(填装置的字母序号)。
②A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe2O3,而不含 FeO 或 Fe3O4:________________________。
(2)探究分解产物中的硫氧化物,连接装置A—E—F—B进行实验。
①实验过程中观察到:E中没有明显现象,F中溶液褪色,据此得出的结论是__________。
②实验证明(NH4)2Fe(SO4)2受热分解除上述产物外,还有N2生成,写出A中反应的化学方程式_____________________________________________。
(3)已知BaSO3、BaSO4均难溶于水,化学小组利用上述实验分离出的SO2气体,进行与可溶性钡盐溶液反应的探究实验。
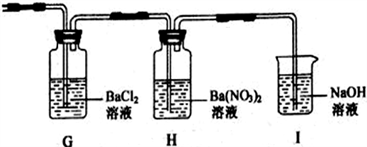
| 序号 | 步骤 | 现象 |
| I | 向上述装置内充SO2气体 | G中:有气泡冒出,产生白色沉淀;H中:有气泡冒出,产生白色沉淀;液面上方先略显红棕色,后逐渐消失 |
| Ⅱ | 从G、H中过滤出白色沉淀,分别加入稀盐酸中 | G、H中的白色沉淀均不溶解 |
①步骤Ⅱ的现象说明实验中产生的白色沉淀是__________(填化学式)。
②关于G中有白色沉淀产生的原因,你认为可能是由于_________________________________。
③写出H中发生反应的离子方程式_________________________________。
-
五水硫酸铜( CuSO4·5H2O) 和六水硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O] 都是重要的化工原料,用途十分广泛。
请回答与这两种物质中元素有关的一些问题。
(1)基态铁原子的核外电子排布式为_______;基态铜原子的电子占据的最高能层符号为_______ 。
(2)氧元素的第一电离能小于氮元素,其原因是_______ 。
(3) SO42-、H2O、NH4+三种微粒中,空间构型为正四面体的是_______;NH4+中氮原子的杂化轨道类型是_______。
(4)写出与SO42-互为等电子体的分子的化学式_______ (写一种)。
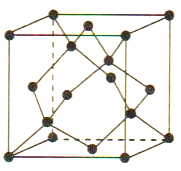
(5)Cu 与Au 的合金可形成面心立方最密堆积的晶体,在该晶胞中Cu 原子处于面心,该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图) 相似,该晶体储氢后的化学式为_______,若该晶体的密度为ρg.cm-3,则晶胞中Cu原子与Au原子中心的最短距离d=_______cm (NA表示阿伏加德罗常数的值)。
-
五水硫酸铜( CuSO4·5H2O) 和六水硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O] 都是重要的化工原料,用途十分广泛。
请回答与这两种物质中元素有关的一些问题。
(1)基态铁原子的核外电子排布式为_______;基态铜原子的电子占据的最高能层符号为_______ 。
(2)氧元素的第一电离能小于氮元素,其原因是_______ 。
(3) SO42-、H2O、NH4+三种微粒中,空间构型为正四面体的是_______;NH4+中氮原子的杂化轨道类型是_______。
(4)写出与SO42-互为等电子体的分子的化学式_______ (写一种)。
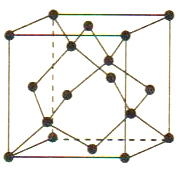
(5)Cu 与Au 的合金可形成面心立方最密堆积的晶体,在该晶胞中Cu 原子处于面心,该晶体具有储氢功能,氢原子可进入到Cu原子与Au原子构成的立方体空隙中,储氢后的晶胞结构与金刚石晶胞结构(如图) 相似,该晶体储氢后的化学式为_______,若该晶体的密度为ρg.cm-3,则晶胞中Cu原子与Au原子中心的最短距离d=_______cm (NA表示阿伏加德罗常数的值)。
-
硫酸亚铁铵品体[(NH4)2Fe(SO4)2·6H2O]又称摩尔盐,是一种重要的化工原料,用途十分广泛。
(1)基态Fe2+的核外电子排布式为_____________________。
(2)氨是合成摩尔盐的重要原料,工业合成氨中,原料气在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收其中的杂质CO气体,其反应方程式为:[Cu(NH3)2]Ac+CO+NH3 [Cu(NH3)3]Ac·CO[醋酸羰基三氨合铜(I)](Ac-=CH3COO-)
[Cu(NH3)3]Ac·CO[醋酸羰基三氨合铜(I)](Ac-=CH3COO-)
①醋酸中碳原子的杂化方式是_________,1mol乙酸分子中含有σ键的数目为_________________。
②C、N、O三种元素的第一电离能由小到大的顺序为___________________________。
③与CO互为等电子体的分子为___________(填化学式),NH3的空间构型为__________________。
(3)N和P都是第VA族元素,其最简单氢化物熔点的大小关系为_________,主要原因是__________________________________。
(4)铁在不同温度范围有不同的晶体结构。室温下铁是简单立方,称为α铁(α-Fe)。当温度升高到912℃,α铁转变为面心立方,称为γ铁(γ-Fe)。当温度继续升高到1394 ℃,γ铁转变为体心立方。称为δ铁(δ-Fe)。
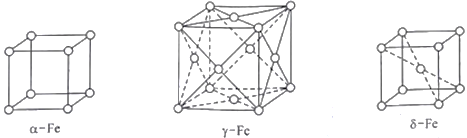
①γ铁晶体中铁原子配位数是____________________。
②δ铁晶体密度为dg·cm-3,则其晶胞参数(边长)为__________cm(阿伏加德罗常数用NA表示)。
-
在无机化工中,硫酸亚铁铵[(NH4)2Fe(SO4)2]是制取其它铁系化合物的原料,如制取氧化伯系颜料、磁性材料和黄血盐等。某化学兴趣小组设计如下实验方案,探究(NH4)2Fe(SO4)2完全分解的产物。
已知:①隔绝空气受热完全分解是氧化还原反应。
②98%浓硫酸能顺利吸收SO3。
Ⅰ.甲同学根据以下流程探究分解的部分产物,试回答下列问题:
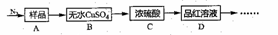
(1)B装置预期的现象是_____;C装置的作用可能是______,D装置可以检验分解产物中是否含有_____。
(2)加热前先通一会儿N2,再关闭气阀,其目的是_______。
Ⅱ.乙同学猜想(NH4)2Fe(SO4)2分解时可能生成了SO3,为了验证他的猜想,小组同学又提供了如右图装置,试回答下列问题:
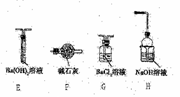
(3)不能选择E和F装置的原因是________。
(4)加热装置A与G、H连接并进行实验,请你提出需要改进的方案________。
(5)已知饱和SO2水溶液中c(SO32-)=6.0×10-8mol•L-1,Ksp(BaSO3)=5.4×10-7。通过计算判断在1.0mol•L-1的BaCl2溶液中,通入足量纯净的SO2能否生成BaSO3沉淀?
(6)当G中出现大量白色沉淀时,并不能说明A中生成了SO3,理由是_______;为了进一步证明是否有SO3生成,请你补充实验方案(不要求写具体的操作过程)_________。
-
硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示)。下列说法错误的是
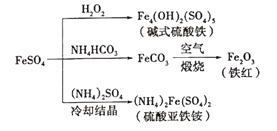
A. 碱式硫酸铁水解能产生Fe(OH)3胶体,可用做净水剂
B. 该温度下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大
C. 可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D. 为防止NH4HCO3分解,生产FeCO3需在较低温度下进行
-
(NH4)2Fe(SO4)2·6H2O俗名摩尔盐,价格便宜,可用来净水或治疗缺铁性贫血等,是一种重要的化工原料。
(1)摩尔盐的水溶液呈 色。
(2)c(Fe2+)相同的摩尔盐和硫酸亚铁两溶液比较,物质的量浓度较大的是 。
(3)甲乙两位同学想测定一瓶摩尔盐的纯度。甲同学设计的实验装置如图1:
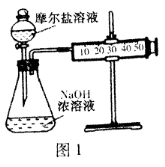
从上图推断甲同学想通过测定 计算摩尔盐的纯度。该方案的不足之处在于 。
(4)乙同学在甲同学的基础上做了改进,其实验装置如图2:
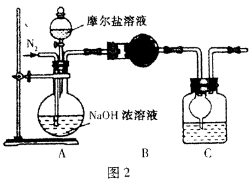
则B与C中的试剂分别是 和 。C中干燥管的作用是 。乙同学称取了10.0g的摩尔盐样品,若实验完毕后测得洗气瓶及瓶内溶液共增重O.68 g,则依此数据推算这份摩尔盐的纯度为 %(答案精确到小数点后第一位)。
-
硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示)。下列说法错误的是
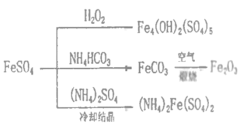
A.FeCO3转化为铁红的化学方程式:4FeCO3+O2 2Fe2O3+4CO2
2Fe2O3+4CO2
B.常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的小
C.制备Fe4(OH)2(SO4)5、Fe2O3、(NH4)2Fe(SO4)2的过程都发生了氧化还原反应
D.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行












