-
已知在元素周期表中,A、B均为前四周期主族元素,且A 位于B 的下一周期。某含氧酸盐X 的化学式为ABO3。请回答:
(1)若常温下B的单质为黄绿色气体。
①A在元素周期表中的位置是_______________________。
②下列说法正确的是_________(填代号)。
a.A单质的熔点比B单质的熔点低
b.A的简单离子半径比B 的简单离子半径大
c.A、B元素的最高价氧化物对应的水化物都是强电解质
d.化合物X中既含有离子键又含有共价键
③400℃时,X能发生分解反应生成两种盐,其物质的量之比为1∶3,其中一种是无氧酸盐。该反应的化学方程式为_____________________________________________。
(2)若X能与稀硫酸反应,生成无色、无味的气体。
①该气体分子的电子式为______________________。
②X在水中持续加热,发生水解反应,生成一种更难溶的物质并逸出气体,反应的化学方程式为__________________________________________。
③X可用作防火涂层,其原因是:a.高温下X发生分解反应时,吸收大量的热;
b. __________________________________________(任写一种)。
(3)若X难溶于水,在空气中易氧化变质,B元素原子的最外层电子数是其电子层数的2倍。X能快速消除自来水中的C1O-,该反应的离子方程式为______________________________________。
(4)用一个化学方程式证明上述(1)、(3)两种情况下化合物X中B元素非金属性强弱________________________________________。
高三化学解答题困难题查看答案及解析
-
某含氧酸盐X的化学式为ABO3 ;已知在元素周期表中,A、B均为前四周期主族元素,且A位于B的下一周期。
(1)若常温下A、B的单质都能与水发生反应,且A的焰色反应为紫色。
①B在元素周期表中的位置是___________________。
②下列说法正确的是__________(填代号)。
a.A离子的半径大于B离子的半径
b.A、B元素的最高价氧化物对应的水化物都是强电解质
c.A单质与水反应后溶液的pH比B单质与水反应后溶液的pH大
③400℃时,X能发生分解反应生成两种盐,其物质的量之比为1:3,其中一种是无氧酸盐。该反应的化学方程式为_______________________________________________。
(2)若含氧酸盐X难溶于水,在空气中易氧化变质;且B元素原子的最外层电子数是其电子层数的2倍。已知X能快速消除自来水中的C1O—,则该反应的离子方程式为_____________
(3)若含氧酸盐X能与稀硫酸反应,生成无色、无味的气体。
①该气体的电子式为______________。
②X可用作防火涂层,其原因是:
a.高温下X发生分解反应时,吸收大量的热;b.________________________(任写一种)。
高三化学综合题中等难度题查看答案及解析
-
已知在元素周期表中,A、B均为前四周期主族元素,且A位于B的下一周期。某含氧酸盐X的化学式为ABO3。请回答:
(1)若常温下B的单质为黄绿色气体。
①A在元素周期表中的位置是_______________________。
②下列说法正确的是_________(填代号)。
a.A单质的熔点比B单质的熔点低
b.A的简单离子半径比B 的简单离子半径大
c.A、B元素的最高价氧化物对应的水化物都是强电解质
d.化合物X中既含有离子键又含有共价键
③400℃时,X能发生分解反应生成两种盐,其物质的量之比为1∶3,其中一种是无氧酸盐。该反应的化学方程式为_____________________________________________。
(2)若X能与稀硫酸反应,生成无色、无味的气体。
①该气体分子的电子式为______________________。
②X在水中持续加热,发生水解反应,生成一种更难溶的物质并逸出气体,反应的化学方程式为__________________________________________。
③X可用作防火涂层,其原因是:a.高温下X发生分解反应时,吸收大量的热;
b. __________________________________________(任写一种)。
(3)若X难溶于水,在空气中易氧化变质,B元素原子的最外层电子数是其电子层数的2倍。X能快速消除自来水中的ClO-,该反应的离子方程式为______________________________________。
(4)用一个化学方程式证明上述(1)、(3)两种情况下化合物X中B元素非金属性强弱________________________________________。
高三化学解答题困难题查看答案及解析
-
已知在元素周期表中,A、B均为前四周期主族元素,且A位于B的下一周期。某含氧酸盐X的化学式为ABO3。请回答:
(1)若常温下B的单质为黄绿色气体。
①A在元素周期表中的位置是_______________________。
②下列说法正确的是_________(填代号)。
a.A单质的熔点比B单质的熔点低
b.A的简单离子半径比B 的简单离子半径大
c.A、B元素的最高价氧化物对应的水化物都是强电解质
d.化合物X中既含有离子键又含有共价键
③400℃时,X能发生分解反应生成两种盐,其物质的量之比为1∶3,其中一种是无氧酸盐。该反应的化学方程式为_____________________________________________。
(2)若X能与稀硫酸反应,生成无色、无味的气体。
①该气体分子的电子式为______________________。
②X在水中持续加热,发生水解反应,生成一种更难溶的物质并逸出气体,反应的化学方程式为__________________________________________。
③X可用作防火涂层,其原因是:a.高温下X发生分解反应时,吸收大量的热;
b. __________________________________________(任写一种)。
(3)若X难溶于水,在空气中易氧化变质,B元素原子的最外层电子数是其电子层数的2倍。X能快速消除自来水中的ClO-,该反应的离子方程式为______________________________________。
(4)用一个化学方程式证明上述(1)、(3)两种情况下化合物X中B元素非金属性强弱________________________________________。
高三化学解答题困难题查看答案及解析
-
已知在元素周期表中,A、B均为前四周期主族元素,且A位于B的下一周期。某含氧酸盐X的化学式为ABO3。请回答:
(1)若常温下B的单质为黄绿色气体。
①A在元素周期表中的位置是_______________________。
②下列说法正确的是_________(填代号)。
a.A单质的熔点比B单质的熔点低
b.A的简单离子半径比B 的简单离子半径大
c.A、B元素的最高价氧化物对应的水化物都是强电解质
d.化合物X中既含有离子键又含有共价键
③400℃时,X能发生分解反应生成两种盐,其物质的量之比为1∶3,其中一种是无氧酸盐。该反应的化学方程式为_____________________________________________。
(2)若X能与稀硫酸反应,生成无色、无味的气体。
①该气体分子的电子式为______________________。
②X在水中持续加热,发生水解反应,生成一种更难溶的物质并逸出气体,反应的化学方程式为__________________________________________。
③X可用作防火涂层,其原因是:a.高温下X发生分解反应时,吸收大量的热;
b. __________________________________________(任写一种)。
(3)若X难溶于水,在空气中易氧化变质,B元素原子的最外层电子数是其电子层数的2倍。X能快速消除自来水中的ClO-,该反应的离子方程式为______________________________________。
(4)用一个化学方程式证明上述(1)、(3)两种情况下化合物X中B元素非金属性强弱________________________________________。
高三化学解答题困难题查看答案及解析
-
已知元素X位于Y的下一周期,X、Y的原子序数均不大于20。某含氧酸盐甲的化学式为XYO3。请回答:
(1)常温下Y的单质能与水发生反应,则X位于周期表_________,X、Y形成简单离子半径大小关系为X_____________Y(填“大于”、“小于”或“等于”)。395℃时,甲能发生分解反应生成两种盐,一种是含Y元素的无氧酸盐,该反应的化学方程式是_____________。
(2)若甲难溶于水,且甲与盐酸反应生成能使品红溶液褪色的气体。
①则甲为___________(填化学式)。该气体能使高锰酸钾溶液褪色,该反应的离子方程式为_______________。
②25℃时,甲在水中的沉淀溶解平衡曲线如下图所示,若要使溶液X2+离子沉淀完全,则加入
离子的最小浓度为___________mol•L﹣1。

(3)若甲能与盐酸反应,生成无色、无味的气体乙。则:
①乙中所含化学键类型____________。
②甲在水中持续加热生成一种更难溶的物质并逸出气体乙,该反应的化学方程式为________________。
高三化学推断题困难题查看答案及解析
-
已知元素 X 位于 Y 的下一周期,X、Y 的原子序数均不大于 20。某含氧酸盐甲的化学式为 XYO3。请回答:
(1)常温下 Y 的单质能与水发生反应,则 X 在周期表中的位置_________________,X、Y 形成简单离子半径大小关系为 X_____________Y(填“大于”、“小于”或“等于”)。395℃时,甲能发生分解反应生成两种盐,一种是含 Y 元素的无氧酸盐,该反应的化学方程式是_____________________。
(2)若甲能与盐酸反应,生成无色、无味的气体乙。则:
①乙的电子式为_______________________。
②甲在水中持续加热生成一种更难溶的物质并逸出气体乙,该反应的化学方程式为___________________。
(3)若甲难溶于水,且甲与盐酸反应生成能使品红溶液褪色的气体。
① 则甲为_______(填化学式)。该气体能使高锰酸钾溶液褪色,该反应的离子方程式为________。
② 25℃时,甲在水中的沉淀溶解平衡曲线如下图所示,若要使溶液 X2+离子沉淀完全,则加入 YO32-离子的最小浓度为___________mol•L﹣1。
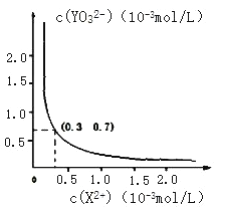
高三化学综合题中等难度题查看答案及解析
-
已知元素X位于Y的下一周期,X、Y的原子序数均不大于20.某含氧酸盐甲的化学式 为XYO3。请回答:
(1)常温下X的单质能与水发生反应,395℃时,甲能发生分解反应生成两种盐,一种是 含Y元素的无氧酸盐,则X位于周期表_____,甲发生分解反应的化学方程式是_____。
(2) 若甲难溶于水,且甲与盐酸反应生成能使品红溶液褪色的气体.
①则甲为_____(填化学式)该气体能使酸性高锰酸钾溶液褪色, 该反应的离子方程式为_____;
②X、Y形成简单离子半径大小关系为 > (用离子符号表示)._________
③25℃时,甲在水中的沉淀溶解平衡曲线如右图所示,若要使溶液 X2+离子沉淀完全,则 YO32-离子的最小浓度为_____mol·L-1。
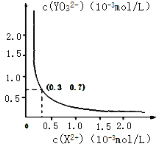
(当离子浓度小于 1×10-5mol·L-1 时,该离子沉淀完全)
(3)若甲能与盐酸反应,生成无色、无味的气体乙.则:
①乙的电子式为_____;
②甲在水中持续加热生成一种更难溶的物质并逸出气体乙,该反应的化学方程式为___。
高三化学综合题中等难度题查看答案及解析
-
(12分)下列框图中的A—J是中学化学中常见的八种物质,所有物质均由短周期元素组成,已知常温、常压下D为无色液体, C、E、G均为气体单质,B为金属,I是由3个原子组成的一元含氧弱酸分子, A—J可发生如下转化:
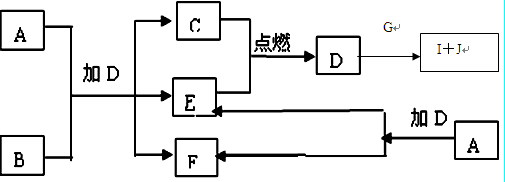
请填写下列空白:
⑴G的名称为________,F的电子式为________。
⑵15.6gA与D完全反应,转移的电子的物质的量为。
⑶常温下,A为一种________色的固体,它的一种重要用途是________。
⑷写出D、G反应转化为I和J的离子方程式________。
高三化学填空题中等难度题查看答案及解析
-
已知A、B、C、D、E、F是周期表前四周期的元素,原子序數依次增大。A的基态原子2p能级上有2个单电子;C是地壳中含量最多的元素;E的单质常温常压下为黄绿色气体,化学性质十分活泼,具有毒性;F位于ds区,最外能层有单电子,是热和电最佳导体之一;D与F不同周期,但最外能层电子数相等。
(1)写出基态C原子的电子排布式: ____________。
(2)A、B、C三种元素第一电离能最大的是____________。(用元素符号表示),其原因是____________。
(3)B、C两元素形成的化合物B2C的分子空间构型为____________。与B2C互为等电子体的粒子的化学式为____________。(填一种)。
(4)D、E形成的一种离子化合物,在晶胞结构图中黑球表示E的位置,白球表示D的位置,已知该晶胞的边长为ncm,阿伏加德罗常数为NA,求晶胞的密度ρ=_______g/cm3(用含n、NA的计算式表示)。
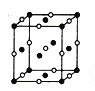
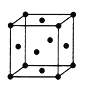
(5)由F原子形成的晶胞结构如图,F原子的半径为r,列式表示F原子在晶胞中的空间利用率:__________________(不要求计算结果)。
高三化学综合题困难题查看答案及解析