-
Ⅰ、甲同学欲配制0.55 mo1·L—1 的NaOH溶液200mL(存在200mL容量瓶)。称量操作如下:
①先用托盘天平称量烧杯的质量。称量前先调节天平零点。用“↓”表示在天平右盘上放置砝码,用“↑”表示从天平右盘上取下砝码。取用砝码情况和游码读数如下:
| 砝码质量 | 50 | 20 | 20 | 10 | 5 |
| 取用砝码情况 | 先↓后↑ | ↓ | 先↓后↑ | ↓ | 先↓后↑ |
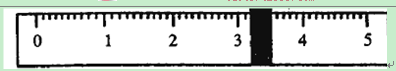
烧杯的质量为________g。
②称量烧杯和NaOH固体的质量。再在天平右盘上放置g砝码,将游码的位置移到________g的位置,往烧杯中逐渐加入NaOH固体,直到天平达到平衡。
Ⅱ、乙同学欲用用18mol/L 浓硫酸配制100 ml 3.0mol/L 稀硫酸的实验步骤如下:
① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 溶解 ④ 转移
⑤洗涤 ⑥定容 ⑦摇匀
回答下列问题
(1)所需浓硫酸的体积是________,量取浓硫酸所用的量筒的规格是________(请填编号)(从下列中选用 A.10ml B.25ml C.50ml D.100ml)
(2)定容时俯视溶液的凹液面对所配制的稀硫酸浓度有何影响________
(用偏大、偏小、无影响填写)
-
(12分)Ⅰ.甲同学欲配制0.55 mo1·L—1 的NaOH溶液200mL(存在200mL容量瓶)。称量操作如下:
①先用托盘天平称量烧杯的质量。称量前先调节天平零点。用“↓”表示在天平右盘上放置砝码,用“↑”表示从天平右盘上取下砝码。取用砝码情况和游码读数如下:
| 砝码质量 | 50 | 20 | 20 | 10 | 5 |
| 取用砝码情况 | 先↓后↑ | ↓ | 先↓后↑ | ↓ | 先↓后↑ |
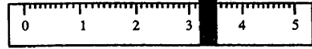
烧杯的质量为________g。
②称量烧杯和NaOH固体的质量。再在天平右盘上放置________g砝码,将游码的位置移到________g的位置,往烧杯中逐渐加入NaOH固体,直到天平达到平衡。
Ⅱ.乙同学欲用用18mol/L 浓硫酸配制100 ml 3.0mol/L 稀硫酸的实验步骤如下:
① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 溶解 ④ 转移 ⑤洗涤 ⑥定容 ⑦摇匀
回答下列问题
(1)所需浓硫酸的体积是________,量取浓硫酸所用的量筒的规格是________
(从下列中选用 A.10ml B.25ml C.50ml D.100ml)
(2)第③步实验的操作是________
________
(3)第⑥步实验的操作是________
________
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.所用的浓硫酸长时间放置在密封不好的容器中________
B.容量瓶用蒸馏水洗涤后残留有少量的水________
C.定容时俯视溶液的凹液面________
-
为了配制100 mL 1 mol·L-1 NaOH溶液,其中有下列几个操作:
①NaOH用纸盛载进行称量 ②选刚用蒸馏水洗净的100 mL容量瓶进行配制 ③NaOH在烧杯里刚好完全溶解,立即把溶液转移到容量瓶中 ④用蒸馏水洗涤烧杯内壁两次,洗涤液都移入容量瓶 ⑤使蒸馏水沿着玻璃棒注入容量瓶,直到溶液的凹液面恰好跟刻度线相切
其中操作错误的是( )
A. ①②③ B.  ③④⑤ C. ②③⑤ D. ①③⑤
③④⑤ C. ②③⑤ D. ①③⑤
-
为了配制100 mL 1 mol·L−1 NaOH溶液,其中有下列几个操作:
①NaOH用纸盛载进行称量;
②选刚用蒸馏水洗净的100 mL容量瓶进行配制;
③NaOH在烧瓶里刚好完全溶解,即把溶液转移到容量瓶;
④用蒸馏水洗涤烧杯内壁两次,洗涤液都移入容量瓶;
⑤使蒸馏水沿着玻璃棒注入容量瓶,直到溶液的凹面恰好跟刻度相切。
其中操作错误的是
A.①②③ B.③④⑤
C.②③⑤ D.①③⑤
-
为了配制100 mL 1 mol·L-1 NaOH溶液,其中有下列几个操作:
①NaOH用纸盛载进行称量
②选刚用蒸馏水洗净过的100 mL容量瓶进行配制
③NaOH固体在烧杯里刚好完全溶解,即把溶液转移到容量瓶中
④用蒸馏水洗涤烧杯内壁两次,洗涤液都移入容量瓶
⑤使蒸馏水沿着玻璃棒注入容量瓶,直到溶液的凹液面恰好跟刻度线相切
其中操作错误的是( )
A.①②③ B.③④⑤
C.②③⑤ D.①③⑤
-
(14分) 某同学帮助水质检测站配制960mL 1 mol·L-1NaOH溶液以备使用。
(1)该同学应选择________mL的容量瓶。
(2)其操作步骤如下图所示,则如图操作应在下图中的________(填选项字母)之间。
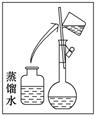

A.②与③ B.①与② C.④与⑤
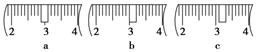
(3)该同学应称取NaOH固体________g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小________(填字母),并在下图中选出能正确表示游码位置的选项________(填字母)。
附表 砝码规格
| a | b | c | d | e |
| 砝码大小/g | 100 | 50 | 20 | 10 | 5 |
(4)下列操作对所配溶液的浓度大小有何影响?
①转移完溶液后未洗涤玻璃棒和烧杯,浓度会__________(填“偏大”“偏小”或“无影响”,下同)。
②容量瓶中原来有少量蒸馏水,浓度会____________。
-
下列实验操作或仪器选择正确的是
A. 配制200mL 0.1mol/LCuSO4溶液需要称量硫酸铜固体3.2g
B. 配制1mol/L H2SO4溶液,量取浓硫酸后,将浓硫酸直接注入容量瓶中
C. 配制1mol/L AlCl3溶液时,将氯化铝晶体溶于适量浓盐酸中,再加水稀释
D. 称量4.0g NaOH固体,溶解于1L水中,即可配制0.1mol/L的NaOH溶液
-
下列实验能达到目的或操作正确的是 ( )
A.称量NaOH固体时,应先在盘上各放一张干净滤纸,再进行称量
B.配制一定浓度溶液的过程中,容量瓶里有少量晶体未溶解,可在酒精灯上小心加热
C.配制450mL0.5mol/L稀硫酸溶液时,用量筒取22.5mL10mol/L的浓硫酸进行稀释
D.质量分数为w%的氨水与水等体积混合,所得溶液的质量分数小于0.5w%
-
下列实验操作中,错误的是( )
A.配制5%的食盐溶液时,将称量的食盐放在烧杯中加适量的蒸馏水搅拌溶解
B.用酸式滴定管准确量取10.00mLKMnO4溶液
C.用500mL容量瓶配制1mol/L的NaOH溶液
D.用pH试纸测得新制氯水的pH为2
-
下列实验操作中,错误的是( )
A.配制5%的食盐溶液时,将称量的食盐放在烧杯中加适量的蒸馏水搅拌溶解
B.用酸式滴定管准确量取10.00mLKMnO4溶液
C.用500mL容量瓶配制1mol/L的NaOH溶液
D.用pH试纸测得新制氯水的pH为2




