实验室用浓盐酸和二氧化锰制氯气。下列说法错误的是
A.浓盐酸在该反应中表现出酸性和还原性
B.该方法是瑞典化学家舍勒最先发现的
C.反应中电子转移4NA时,理论可以生成氯气22.4L
D.该反应的离子方程式为MnO2+4H++2Cl-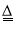 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
高一化学单选题中等难度题
实验室用浓盐酸和二氧化锰制氯气。下列说法错误的是
A.浓盐酸在该反应中表现出酸性和还原性
B.该方法是瑞典化学家舍勒最先发现的
C.反应中电子转移4NA时,理论可以生成氯气22.4L
D.该反应的离子方程式为MnO2+4H++2Cl-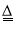 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
高一化学单选题中等难度题
实验室用浓盐酸和二氧化锰制氯气。下列说法错误的是
A.浓盐酸在该反应中表现出酸性和还原性
B.该方法是瑞典化学家舍勒最先发现的
C.反应中电子转移4NA时,理论可以生成氯气22.4L
D.该反应的离子方程式为MnO2+4H++2Cl-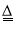 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
高一化学单选题中等难度题查看答案及解析
早在1774年,瑞典化学家舍勒在研究软锰矿(主要成分)的过程中,将它与浓盐酸混合加热,产生了黄绿色气体—氯气。某小组同学利用舍勒发现氯气的方法制取氯气并探究其性质。
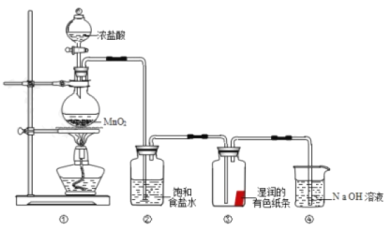
请回答:
(1)装置①中制取氯气,盛有浓盐酸的玻璃仪器名称为__________
(2)装置②的作用是________________________________________.
(3)装置③中的现象是________________________________________.
(4)装置④中反应的离子方程式是________________________________________.
高一化学实验题简单题查看答案及解析
(12分)舍勒发现氯气的的方法至今还是实验室制取氯气的主要方法之一.
(1)请写出实验室制氯气的反应化学方程________,
(2)反应方程式中氧化剂和还原剂物质的量之比为________;其中Cl2是________ 产物(填氧化或还原);
(3)如右图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是 ________,从而得出的结论是________.
(4)实验室中剩余的Cl2尾气通常用NaOH溶液吸收,发生反应的离子方程式________。
高一化学填空题中等难度题查看答案及解析
某小组同学利用舍勒发现氯气的方法制取氯气并探究其性质。
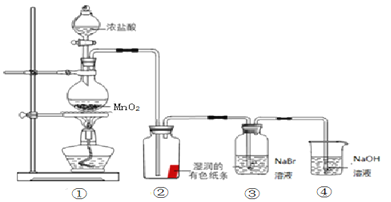
请回答:
(1)写出装置①中制取氯气化学反应方程式__________。在反应中,是利用了MnO2的_________ (填“氧化性”或“还原性”)。
(2)装置②中的现象是__________。
(3)③中溶液由无色变为橙黄色,发生反应的离子方程式是_________。
(4)用离子方程式解释④中NaOH溶液的作用____________。
(5)取一支试管,加入2 mL ③中橙黄色溶液,再滴入几滴KI-淀粉溶液,观察到溶液变为蓝色。通过以上实验,能否得出结论:Br2的氧化性强于I2 _________(能或否)。理由是_________。
高一化学实验题简单题查看答案及解析
瑞典化学家舍勒在研究软锰矿矿石时,把浓盐酸和软锰矿矿石混合加热,意外得到了氯气,MnO2 + 4HCl(浓)MnCl2 + Cl2 ↑+ 2H2O 关于该反应的叙述不正确的是
A.MnO2是氧化剂 B.HCl具有还原性
C.MnO2被HCl还原 D.氧化剂与还原剂的物质的量之比为1:4
高一化学单选题中等难度题查看答案及解析
1774年,瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合加热能制取氯气:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O。现将17.4gMnO2与200克36.5%的浓盐酸完全反应,回答下列问题(要有计算过程并要求取三位有效数字):
(1)反应中被还原的物质是什么?
(2)生成的Cl2的体积(标准状况)是多少?
(3)求反应中被氧化的HCl的物质的量。
高一化学计算题困难题查看答案及解析
(1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气,写出该反应的离子方程式 ;
(2)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。 漂白粉是常用的消毒剂。工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为 ;
(3)在下图的四条直线分别表示钠、铜、铝、铁与足量Cl2反应时,消耗金属的质量(纵轴)与反应掉的氯气质量(横轴)的关系,其中代表铁与Cl2反应的直线是 ,如果横轴表示消耗掉的硫的质量,则b表示的是四种金属中的 。

高一化学填空题中等难度题查看答案及解析
下列叙述中错误的是( )
A. 金刚石和石墨均为碳元素组成的单质
B. 瑞典的舍勒发现了氯气,英国的戴维确认了氯气是由一种元素组成的
C. 德国化学家维勒研究尿素的合成,揭开了人工合成有机物的序幕
D. 生铁的含碳量为0.03%~2%,将生铁进一步炼制,可以得到用途更广泛的钢(含碳量2%~4.5%)
高一化学单选题简单题查看答案及解析
1774年,瑞典化学家舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,意外地发现生成了一种黄绿色有刺激性气味的气体──氯气。某实验小组设计如下图所示的实验装置。
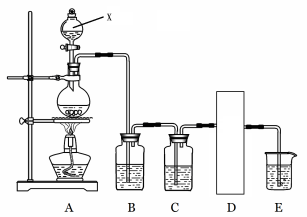
利用该装置制备纯净、干燥的氯气,并吸收多余氯气防止污染空气。圆底烧瓶内加入二氧化锰,x中加入浓盐酸。
(1)仪器x的名称是 ,D处可以选用下列装置中的 (填写编号)。
a b c d
(2)圆底烧瓶内发生反应的化学方程式为 。
(3)装置B中的试剂为 ,作用 。
(4)烧杯中发生反应的化学方程式为 。
高一化学实验题极难题查看答案及解析
重铬酸钾和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为
。
(1)浓盐酸在反应中表现出来的性质是_______(填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)是_______(“氧化”或“还原”)产物;产生
,则转移电子的物质的量为____mol。
(3)从铬元素的化合价态上判断,
三种物质中的铬元素既表现氧化性又表现还原性的是_____________(写化学式,下同)。
(4)已知氯气有毒,与水反应生成两种酸。实验室制备氯气可选用__________溶液进行尾气处理。
高一化学填空题中等难度题查看答案及解析