-
甲醇属于可再生能源,可作汽车的燃料,下列能正确表示甲醇燃烧热的热化学方程式为
A.CH3OH(l)+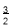 O2(g)=CO2(g)+2H2O(l) ΔH=+763.3 kJ·mol-1
O2(g)=CO2(g)+2H2O(l) ΔH=+763.3 kJ·mol-1
B.CH3OH(l)+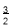 O2(g)=CO2(g)+2H2O(l) ΔH=-763.3 kJ·mol-1
O2(g)=CO2(g)+2H2O(l) ΔH=-763.3 kJ·mol-1
C.CH3OH(l)+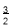 O2(g)=CO2(g)+2H2O(g) ΔH=-675.3 kJ·mol-1
O2(g)=CO2(g)+2H2O(g) ΔH=-675.3 kJ·mol-1
D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1 526.6 kJ·mol-1
-
能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)在25℃、101kPa时,2gC2H2(g)完全燃烧生成液态水时放出的热量是100kJ,则C2H2燃烧的热化学方程式是________。
(2)已知C(石墨,s)+O2(g)=CO2(g) △H=-393.5kJ·mol-1,C(金刚石,s)+O2(g)=CO2(g) △H=-395.0kJ·mol-1,则反应C(石墨,s)==C(金刚石,s) △H=__kJ·mol-1。
(3)已知H2(g)的燃烧热△H1=-285.0kJ·mol-1,CO(g)的燃烧热△H2=-283.0kJ·mol-1,CH3OH(l)的燃烧热△H3=-726.0kJ·mol-1。0.2mol由H2和CO组成的混合气体在完全燃烧时放出56.8kJ的能量,则混合气体中H2和CO的质量比为______。工业上在催化剂的作用下,可用H2(g)和CO(g)合成CH3OH(l)。请写出由H2(g)和CO(g)合成CH3OH(l)的热化学方程式:________。
(4)强酸和强碱的稀溶液的中和热可表示为H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1。已知:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) △H=-33.1kJ·mol-1。请写出醋酸溶液电离的热化学方程式:__________。
-
在25℃、101kPa的条件下,1g液态甲醇(CH3OH)燃烧生成CO2(g)和液态水时放热22.68kJ,下列热化学方程式正确的是
A. CH3OH(l)+  O2(g) =CO2(g)+2H2O(l);ΔH=725.76 kJ·mol-1
O2(g) =CO2(g)+2H2O(l);ΔH=725.76 kJ·mol-1
B. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l);ΔH=-1451.52 kJ·mol-1
C. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l);ΔH=-725.76kJ·mol-1
D. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l);ΔH=1451.52kJ·mol-1
-
在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是
A.CH3OH(l)+3/2 O2(g)== CO2(g)+2H2O(l) ΔH=+725.8 kJ/mol
B.2CH3OH(l)+3O2(g)== 2CO2(g)+4H2O(l) ΔH=-1452 kJ/mol
C.2CH3OH(l)+3O2(g)== 2CO2(g)+4H2O(l) ΔH=-725.8 kJ/mol
D.2CH3OH(l)+3O2(g)== 2CO2(g)+4H2O(l) ΔH=+1452 kJ/mol
-
依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g液态甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为: 。
(2)若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量。写出1mol N2和O2完全反应的热化学方程式为: 。
(3)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为: 。
-
直接甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
(1)101 kPa时,1 mol CH3OH完全燃烧生成稳定的氧化物放出热量726.51 kJ/mol,则甲醇燃烧的热化学方程式为 ________ 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H1=+49.0 kJ·mol-1
②CH3OH(g)+ O2(g)= CO2(g)+2H2(g) △H2
O2(g)= CO2(g)+2H2(g) △H2
已知H2(g)+ O2(g)=H2O(g) △H =-241.8 kJ·mol-1
O2(g)=H2O(g) △H =-241.8 kJ·mol-1
则反应②的△H2= kJ·mol-1。
(3)甲醇燃料电池的结构示意图如右。甲醇进入 极(填“正”或“负”),正极发生的电极反应式为 ________ 。负极发生的电极反应式为 ________ 。
-
依据叙述,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g液态甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为______________________________。
(2)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量。其热化学方程式为____________________________________________________________。
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量。其热化学方程式为____________________。
(4)已知拆开1mol H—H键、1mol N—H键、1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_____________________。
-
I. 依据事实写出下列反应的热化学方程式。
① 在25℃、101kPa下,1g甲醇CH3OH燃烧生成CO2和液态水时放热22.68kJ。
则表示甲醇燃烧热的热化学方程式为__________________。
② 若适量的N2和O2完全反应,每生成23克NO2需要吸收16.95kJ热量_____________。
II. 盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式
①Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g) △H= ―24.8 kJ.mol -1
②3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= ―47.2 kJ.mol -1
③Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5 kJ.mol -1
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式________________。
III.已知反应 2HI(g)=H2(g) + I2(g)的△H=+11kJ·mol-1,1molH2(g)、 1molI2(g)分子中化学键断裂时分别需要吸收 436KJ、151KJ 的能量,则 1molHI(g)分子中化学键断裂时需吸收的能量为______________kJ。
-
能源问题是人类社会面临的重大课题,甲醇是未来重要的绿色能源之一。
(1)利用工业废气CO2可制取甲醇,己知常温常压下下列反应的能量关系如图:
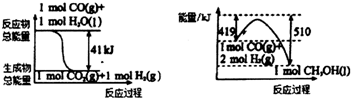
则CO2与H2反应生成液态CH3OH 的热化学方程式为_______________________。
(2)CH4 和H2O(g)通过下列转化也可以制得CH3OH:
I.CH4(g)+H2O(g) CO(g)+3H2(g); △H1>0
CO(g)+3H2(g); △H1>0
II.CO(g)+2H2(g) CH3OH(g); △H2<0
CH3OH(g); △H2<0
将1.0molCH4 和3.0molH2O (g)通入反应室(容积为100L)中,在一定条件下发生反应I,CH4的转化率与温度、压强的关系如下图所示。
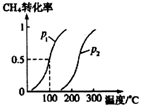
① 图中的P1___P2(填“<”、“>”或“=”) ,判断的理由是________________。
② 若反应II在恒容密闭容器进行,下列能判断反应II达到平衡状态的是______(填序号)。
A.生成CH3OH 的速率与消耗CO 的速率相等 B.混合气体的密度不变
C.混合气体的总物质的量不变 D.CH3OH、CO、H2的浓度都不再发生变化
③在某温度下,将一定量的CO和H2投入10L的密闭容器中发生反应II,5min时达到平衡,各物质的物质的浓度(mol· L-1)变化如下表所示:
| 2min | 5min | 10min |
| CO | 0.07 | 0.06 | 0.05 |
| H2 | 0.14 | 0.12 | 0.20 |
| CH3OH | 0.03 | 0.04 | 0.05 |
若5min时只改变了某一条件,则所改变的条件是_______________。
-
化学家认为石油、煤作为能源使用时,燃烧了“未来的原始材料”.下列观点正确的是
A. 大力提倡开发化石燃料作为能源
B. 研发新型催化剂,提高石油和煤中各组分的燃烧热
C. 化石燃料属于可再生能源,不影响可持续发展
D. 人类应尽可能开发新能源,取代化石能源
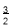 O2(g)=CO2(g)+2H2O(l) ΔH=+763.3 kJ·mol-1
O2(g)=CO2(g)+2H2O(l) ΔH=+763.3 kJ·mol-1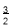 O2(g)=CO2(g)+2H2O(l) ΔH=-763.3 kJ·mol-1
O2(g)=CO2(g)+2H2O(l) ΔH=-763.3 kJ·mol-1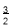 O2(g)=CO2(g)+2H2O(g) ΔH=-675.3 kJ·mol-1
O2(g)=CO2(g)+2H2O(g) ΔH=-675.3 kJ·mol-1
