-
已知:X、Y分别是地壳中含量最高的金属和非金属元素的单质,D、E、F为气体,X在酸性或碱性溶液中均可与NO3-发生氧化还原反应,气体D和G反应可生成盐,气体D和A溶液反应生成白色沉淀,气体E和F在NaOH溶液中按1:1反应钠盐M,各物质转化关系如下:
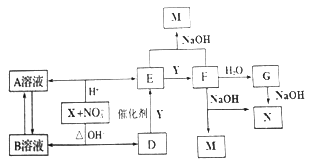
请回答下列问题:
(1)M的化学式__________。
(2)请写出D的溶液与A溶液反应的离子方程式:___________
(3)写出X在碱性条件下与NO3-反应的离子方程式:_____________
(4)标况下,若E,F的混合气体共48mL,恰好被10mL菜浓度的NaOH溶液吸收,则该NaOH溶液浓度为______mol,若反应后所得溶液中M和N的浓度之比为7:1,则原来气体中E与F的体积比为________。
-
(16分)下图中A~J均代表无机物或其水溶液,其中A是红棕色粉末,B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料。已知B可以在高温下与金属活性不如其强的其他金属的氧化物发生置换反应。
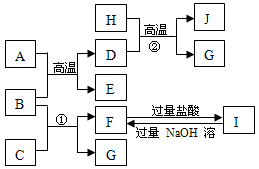
(1)写出下列物质的化学式:
A________ E________ I________
(2)反应①的离子方程式是________ E是________氧化物(填碱性或酸性或两性)
F与过量盐酸反应的离子方程式是________
(3)J与盐酸反应的化学方程式是________
反应后的溶液与氯气反应的离子方程式是________
-
阅读下表中短周期主族元素的相关信息并填空。
| 元素代号 | 相关信息 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是其内层电子数的三倍 |
| C | 是地壳中含量最高的金属元素 |
| D | A、B、D组成的化合物X是84消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
(1)E元素周期表中的位置 ;C的原子结构示意图 。
(2)X的化学式为 。
(3)A、B、D三种元素形成的简单离子半径由大到小的顺序为 (用离子符号表示)。
(4)A、B形成的一种原子个数比为1:1化合物的化学式为 。
(5)A在真空高压下能与由元素D、E组成化合物ED4反应生成两种固体物质,其中一种是自然界中硬度最大的物质,此反应在科学上有“稻草变黄金”的美称。写出该反应的化学方程式 。
-
A、B、C、D,E和F是六种短周期元素,它们的原子序数依次增大。 A和D,C与F为同主族元素;A的单质是最轻的气体; B元素最高价氧化物的水化物与其气态氢化物反应生成盐; E元素是地壳中含量最多的金属元素。F元素原子M层上电子数比L层少2个电子。 试完成下列填空
(1)E元素位于周期表的第________周期________族。
(2)F简单阴离子的结构示意图 ________。
(3)铜与B元素最高价氧化物的水化物的稀溶液反应的离子方程式为________。
(4)E的硫酸盐溶液中滴入B元素气态氢化物的水溶液,直至过量。离子方程式为________。
-
A、B、C、D,E和F是六种短周期元素,它们的原子序数依次增大. A和D,C与F为同主族元素;A的单质是最轻的气体; B元素最高价氧化物的水化物与其气态氢化物反应生成盐; E元素是地壳中含量最多的金属元素.F元素原子M层上电子数比L层少2个电子. 试完成下列填空
(1)E元素位于周期表的第______周期______族.
(2)F简单阴离子的结构示意图______.
(3)A、C、D 三种元素共同形成的化合物的电子式______,其微粒间存在的化学键有______.
(4)铜与B元素最高价氧化物的水化物的稀溶液反应的离子方程式为______.
(5)E的硫酸盐溶液中滴入B元素气态氢化物的水溶液,直至过量.离子方程式为______.
-
已知A、B、C、D是短周期元素的气态单质,其中A是黄绿色的气体单质,C在空气中含量最高,D是最轻的气体;E是一种最常用的金属;Y是一种常见的液态物质,Z是唯一显碱性的气体; M是一种红棕色的有毒气体;I为红褐色难溶于水的固体。有关的转化关系如下图所示(反应条件均已略去)。

回答下列问题:
(1)A的组成元素在元素周期表的位置为 ;
(2)F中化学键的类型是 、 ;(每空2分,共4分)
(3)Z和W在催化剂作用下反应生成C和Y,这是一个很有实际意义的反应,可以消除W对环境的污染,该反应的化学方程式为 ;
(4)I为红褐色难溶于水的固体,与“84消毒液”的有效成分(NaClO) ,在浓碱溶液中发生反应生成了高效环保的净水剂高铁酸钠,请写出此反应的离子方程式 。
(5)将过量的E加到N的稀溶液中,若过程中转移电子的数目为3.01×1023,则参加反应的E的质量为
g。
-
已知:A、C、J为日常生活中常见的金属单质,其中A、C均呈银白色,J呈紫红色。A是地壳中含量最高的金属元素,B是一种红棕色金属氧化物。它们之间的转化关系如下图。反应②在工业上可用于制作印刷电路板。请回答下列问题:
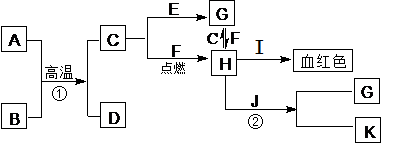
(1)写出C和I的化学式: , ;
(2)写出反应①的化学方程式: ,写出反应②的离子方程式: ;
(3)写出反应①在工业上的一种用途 。
-
如图A~J均代表不同物质或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料,常温下H为无色液体.
根据图示回答问题:
(1)写出下列物质的化学式:B______,E______,I______,J______;
(2)反应①的离子方程式是______;
E→F的化学方程式是______;
(3)F与过量盐酸反应的离子方程式是______.

-
下图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料。

根据图示回答问题:
(1)写出下列物质的化学式:A ______,E______;
(2)反应①的化学方程式是_________________________ ;
反应②的化学方程式是___________________________ ;
(3)J与盐酸反应的化学方程式是______________________ ;
反应后的溶液与足量的D反应的离子方程式是______________________,如何检验最后溶液中的阳离子:______________________________________。
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为________________________。
-
下图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料。
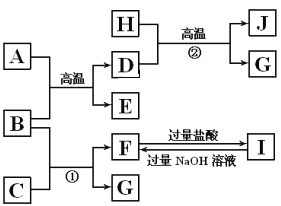
根据图示回答问题:
(1)写出下列物质的化学式:A ______,E______;
(2)反应①的化学方程式是_________________________;反应②的化学方程式是___________________________;
(3)J与盐酸反应的化学方程式是______________________;反应后的溶液与足量的D反应的离子方程式是______________________,如何检验最后溶液中的阳离子:______________________________________。
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为__________________。






