-
十九大报告指出,“建设生态文明是中华民族水续发展的千年大计”。控制和治理NOx、SO2、CO2是解决光化学烟算、减少酸雨和温室效应的有效途径,对构建生态文明有着极为重要的意义。回答下列问题:
(1)利用SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
①SCR(选择催化还原NOx)工作原理:
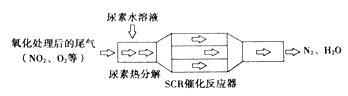
尿素水溶液热分解为NH3和CO2的化学方程式为________,SCR催化反应器中NH3还原NO2的化学方程式为__________。
②NSR(NOx储存还原)工作原理:
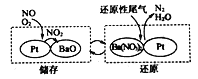
在储存过程中,NO发生的总化学反应方程式为__________
(2)双碱法除去SO2的工作原理:NaOH溶液 Na2SO3溶液
Na2SO3溶液
过程①的离子方程式为_____;CaO在水中存在如下转化:CaO(s)+H2O(1)=Ca(OH)2(s) Ca2+(aq)+2OH-(aq),从平衡移动的角度,简述过程②NaOH再生的原理____________.
Ca2+(aq)+2OH-(aq),从平衡移动的角度,简述过程②NaOH再生的原理____________.
(3)人工光合作用技术回收利用二氧化碳的工作原理:
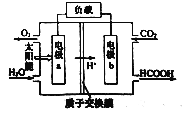
a极为_______极,b极的电极反应式为______________。
-
十九大报告指出:建设生态文明是中华民族永续发展的千年大计。必须树立和践行绿水青山就是金山银山的理念.....,实行最严格的生态环境保护制度,形成绿色发展方式和生活方式。下列有关节约资源和保护环境的说法不正确的是
A. 回收塑料及钢铁制品可以减少二氧化碳排放
B. 使用地热能、生物质能等非化石能源可减少PM2.5
C. 开采使用地下可燃冰,可以增加非化石能源消费比例
D. 创新生产工艺,实现电动机车替代燃油机车符合绿色发展方式
-
十九大报告指出:建设生态文明是中华民族永续发展的千年大计。必须树立和践行绿水青山就是金山银山的理念.....,实行最严格的生态环境保护制度,形成绿色发展方式和生活方式。则下列说法不正确的是
A. PM2.5是指粒径不大于2.5µm的可吸入悬浮颗粒物
B. 以液化石油气代替燃油可减少大气污染
C. 生活污水可灌溉庄稼,所以能排放到自然界水体中
D. 创新生产工艺,实现电动机车替代燃油机车符合绿色发展方式
-
CO2 、SO2 、NOx 是对环境影响较大的气体,控制和治理CO2、SO2、NOx 是解决温室效应、减少酸雨和光化学烟雾的有效途径。
(1)下列措施中,有利于降低大气中的CO2、SO2、NOx 浓度的有________(填字母)
a.减少化石燃料的使用,开发新能源
b.使用无氟冰箱,减少氟里昂排放
c.多步行或乘公交车,少用专车或私家车
d.将工业废气用碱液吸收后再排放
(2)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代作为公交车的燃料。写出用合成气(CO和H2)生产甲醇的化学方程式 ________,已知该反应合成1 mol液态甲醇吸收热量131.9 kJ, 2H2 (g) + CO(g) + 3/2O2g) =CO2 (g) +2H20 (g) △H =-594.1 kJ·mol-1,请写出液态甲醇燃烧生成二氧化碳和水蒸气的热化学方程式________ 。
(3)有人设想以下图所示装置用电化学原理将CO2、SO2 转化为重要化工原料。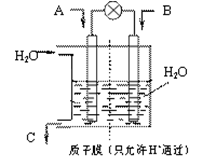
若A为CO2,B为H2,C为CH3OH,则通入CO2 的一极为 ________极;若A为SO2,B为O2,C为H2SO4。则负极的电极反应式为________ ;
(4)①在研究氮的氧化物的转化时,某小组查阅到以下数据:17℃、1.01×105 Pa时,
2NO2(g)  N2O4(g) △H <0的平衡常数 K=13.3,则该条件下密闭容器中N2O4 和NO2的混合气体达到平衡时,若 c (NO2) = 0.0300 mol·L-1,
N2O4(g) △H <0的平衡常数 K=13.3,则该条件下密闭容器中N2O4 和NO2的混合气体达到平衡时,若 c (NO2) = 0.0300 mol·L-1,
c (N2O4)= ________ (保留两位有效数字);
②改变上述体系的某个条件,达到新的平衡后,测得混合气体中 c (NO2) = 0.04 mol·L-1, c (N2O4) = 0.007 mol·L-1,则改变的条件为 ________;
-
CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径.
(1)下列措施中,有利于降低大气中的CO2、SO2、NOx浓度的有________(填字母).
a.减少化石燃料的使用,开发新能源
b.使用无氟冰箱,减少氟里昂排放
c.多步行或乘公交车,少用专车或私家车
d.将工业废气用碱液吸收后再排放
(2)新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应.该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为________(只要求写一种).
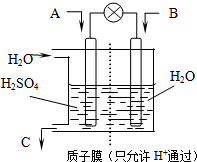
(3)有学者设想以如图所示装置用电化学原理将CO2、SO2转化为重要化工原料.
①若A为CO2,B为H2,C为CH3OH,则正极电极反应式为________.
②若A为SO2,B为O2,C为H2SO4.科研人员希望每分钟从C处获得100mL10mol/LH2SO4,则A处通入烟气(SO2的体积分数为1%)的速率为________L/min(标准状况).
-
CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径。
⑴下列措施中,有利于降低大气中的CO2、SO2、NOx浓度的有___ ___(填字母)。
a.减少化石燃料的使用,开发新能源
b.使用无氟冰箱,减少氟里昂排放
c.多步行或乘公交车,少用专车或私家车
d.将工业废气用碱液吸收后再排放
⑵新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的SO2,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用SO2外,还能得到一种复合肥料,该复合肥料可能的化学式为________________(只要求写一种)。
⑶有学者设想以下图所示装置用电化学原理将CO2、SO2转化为重要化工原料。
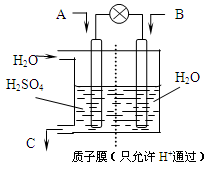
①若A为CO2,B为H2,C为CH3OH,则正极电极反应式为________。
②若A为SO2,B为O2,C为H2SO4。科研人员希望每分钟从C处获得100mL10mol/LH2SO4,则A处通入烟气(SO2的体积分数为1%)的速率为________L/min(标准状况)。
-
(16分)CO2、SO2、NOx是对环境影响较大的气体,控制和治理CO2、SO2、NOx是解决温室效应、减少酸雨和光化学烟雾的有效途径。
(1)下图是在101 kPa,298 K条件下1 mol NO2和1 mol CO反应生成1 mol CO2和1 mol NO过程中能量变化示意图。
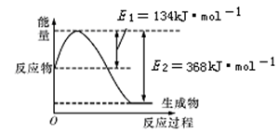
已知:①N2 (g) +O2 (g) =2 NO (g) ΔH=179.5 kJ·mol—1
②2NO (g) +O2 (g) =2 NO2 (g) ΔH=—112.3 kJ·mol—1
请写出NO与CO反应生成无污染气体的热化学方程式:_____________________。
(2)工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=—49.0 kJ·mol—1
CH3OH(g)+H2O(g) ΔH=—49.0 kJ·mol—1
某科学实验小组将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如下图中实线所示(图中字母后的数字表示对应的坐标)。
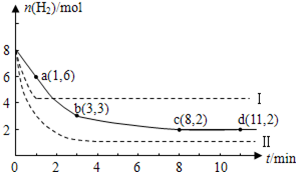
①该反应在0 ~8 min内CO2的平均反应速率是_____________________;
②该反应的平衡常数表达式为:K=_____________________;
③仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。与实线相比,曲线Ⅰ改变的条件可能是_____________________,曲线Ⅱ改变的条件可能是____________________。若实线对应条件下平衡常数为K,曲线Ⅰ对应条件下平衡常数为K1,曲线Ⅱ对应条件下平衡常数为K2,则K、K1和K2的大小关系是_____________________;
(3)有学者设想以如图所示装置用电化学原理将他们转化为重要化工原料。请回答:
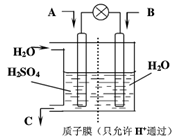
①若A为SO2,B为O2,C为H2SO4,则负极反应式___________________;
②若A为CO2,B为H2,C为CH3OH,则正极反应式__________________。
-
党的十九大报告中提出要建设美丽中国,推进绿色发展。燃煤烟气(污染气体包括NOx、CO、SO2等)的综合治理是解决大气污染的主要途径。
(1)用CH4催化还原氮氧化物可以消除其污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ·mol-1
③H2O(g)=H2O(1)△H=-44.0kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(1)的热化学方程式__________。
(2)选择合适的催化剂,在一定条件下可对部分燃煤烟气回收,其主要反应是:2CO(g)+SO2(g) 2CO2(g)+S(1)△H=-270kJ·mol-1
2CO2(g)+S(1)△H=-270kJ·mol-1
①其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图1,Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑催化剂价格因素,选择Fe2O3的主要优点是__________。
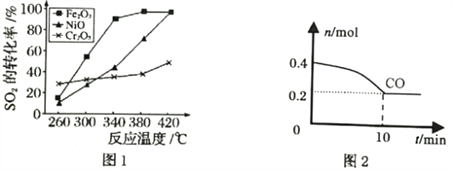
②T℃Fe2O3催化作用下,将等物质的量的CO和SO2充入容积为2L的密闭容器中,保持温度和体积不变,反应过程中CO的物质的量随时间变化如图2所示。10min内该反应的速率v(SO2)=________;T℃时该化学反应的平衡常数K=______;保持容积固定,若升高温度,反应的平衡常数_________(填“增大”“减小”或“不变”,下同),容器内混合气体的密度__________。
(3) 图3是用食盐水做电解液电解烟气脱氮的原理图,NO被阳极产生的氧化性物质氧化为NO3-,尾气经NaOH溶液吸收排入空气。
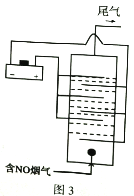
①NO被氧化的离子方程式是__________。
②若通入的烟气2240L(标准状况),烟气中NO含量为15%,(假设烟气中无其他含氮气体),测得溶液中含有NO3-的物质的量为1.47mol,则NO除去率为__________%。
-
党的十九大报告指出:“坚持人与自然和谐共生,坚定走生态良好的文明发展道路,建设美丽中国,为人民创造良好的生活环境”。下列行为与该主题不相吻合的是
A. 发展农村沼气,将废弃的农作物秸秆转化为清洁高效的能源
B. 实施矿物燃料的脱硫脱硝技术,可以减少SO2、NO2的排放
C. 在推广乙醇汽油的同时,研究开发太阳能电池和氢燃料电池汽车
D. 开着大排量的家用汽车开直播声讨雾霾天气
-
十九大报告指出:“坚持全民共治、源头防治,持续实施大气污染防治行动,打赢蓝天保卫战!”以NOx为主要成分的雾霾的综合治理是当前重要的研究课题。
I.汽车尾气中的NO(g)和CO(g)在一定条件下可发生如下反应:
反应①2NO(g)+2CO(g) N2(g)+2CO2(g) △H1
N2(g)+2CO2(g) △H1
(1)已知:反应②N2(g)+O2(g) 2NO(g) △H2=+180.5kJ·mol-1
2NO(g) △H2=+180.5kJ·mol-1
CO的燃烧热为283.0kJ·mol-l,则△H1=___。
(2)在密闭容器中充入5 mol CO和4 mol NO,发生上述反应①,图1为平衡时NO的体积分数与温度、压强的关系。
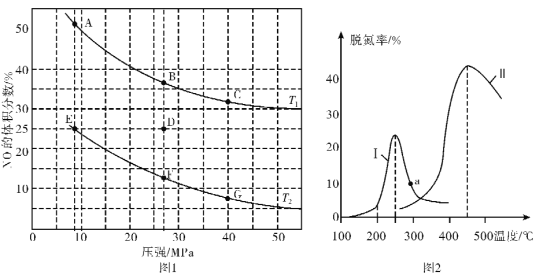
①温度:T1____T2(填“<”或“>”)。
②若在D点对反应容器升温的同时扩大体积使体系压强减小,重新达到的平衡状态可能是图中A~G点中的____点。
(3)某研究小组探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如上图2所示。若低于200℃,图2中曲线中脱氮率随温度升高而变化不大的主要原因为____;a点 ___(填“是”或“不是”)对应温度下的平衡脱氮率,说明理由____。
Ⅱ.N2O是一种强温室气体,且易形成颗粒性污染物,研究N2O的分解对环境保护有重要意义。
(4)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步I2(g) 2I(g)(快反应)
2I(g)(快反应)
第二步I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。
下列表述正确的是____。
A.N2O分解反应中:k值与是否含碘蒸气无关
B.第二步对总反应速率起决定作用
C.第二步活化能比第三步小
D.IO为反应的中间产物


Na2SO3溶液
Ca2+(aq)+2OH-(aq),从平衡移动的角度,简述过程②NaOH再生的原理____________.









