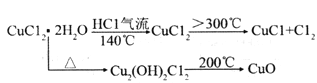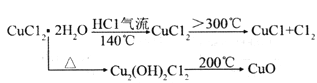-
铜及其化合物在工农业生产有着重要的用途,氯化铜、氯化业铜经常用作催化剂。其中CuCl广泛应用于化工和印染等行业。
【查阅资料】(i)氯化铜:从水溶液中结晶时,在15℃以下得到四水物,在15 -25.7℃得到三水物,在26~42℃得到二水物,在42℃以上得到一水物,在100得到无水物。
(ii)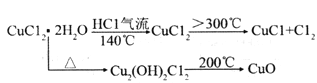
(1)实验室用如图所示的实验仪器及药品制备纯净、干燥的氧气并与铜反应(铁架台,铁夹略) 制备氯化铜。
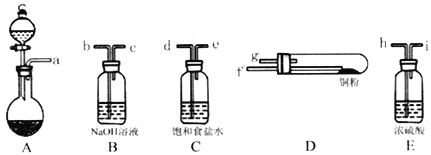
①按气流方向连接各仪器接口顺序是:
a→_____、_____→_____、_____→_____、_____→_____。
②本套装置有两个仪器需要加热,加热的顺序为先_____后_______
(2)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,写出该反应的化学方程式:_____________________。
(3)现欲从(2)所得溶液获得纯净的CuCl2•2H2O,进行如下操作:
①首先向溶液中加入H2O2溶液然后再加试剂X 用于调节pH,过滤,除去杂质,X可选用下列试剂中的(填序号)
a.NaOH b.NH3•H2O C.CuO d.CuSO4
②要获得纯净CuCl2•2H2O晶体的系列操作步骤为:向①所得滤液中加少量盐酸,蒸发浓缩、_____、_____、洗涤、干燥。
(4)用CuCl2•2H2O为原料制备CuCl 时,发现其中含有少量的CuCl 2或CuO杂质,若杂质是CuCl2,则产生的原因是______________。
(5)设计简单的实验验证0.1mol/L 的CuCl2溶液中的Cu2+ 对H2O2的分解具有催化作用:_____。
-
铜及其化合物在工农业生产有着重要的用途,氯化铜、氯化业铜经常用作催化剂。其中CuCl广泛应用于化工和印染等行业。
【查阅资料】(i)氯化铜:从水溶液中结晶时,在15℃以下得到四水物,在15 -25.7℃得到三水物,在26~42℃得到二水物,在42℃以上得到一水物,在100得到无水物。
(ii)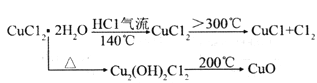
(1)实验室用如图所示的实验仪器及药品制备纯净、干燥的氧气并与铜反应(铁架台,铁夹略) 制备氯化铜。
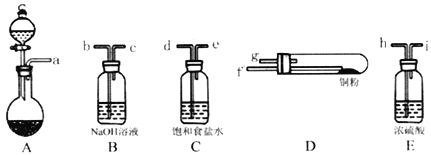
①按气流方向连接各仪器接口顺序是:
a→_____、_____→_____、_____→_____、_____→_____。
②本套装置有两个仪器需要加热,加热的顺序为先_____后_______
(2)印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,写出该反应的化学方程式:_____________________。
(3)现欲从(2)所得溶液获得纯净的CuCl2•2H2O,进行如下操作:
①首先向溶液中加入H2O2溶液然后再加试剂X 用于调节pH,过滤,除去杂质,X可选用下列试剂中的(填序号)
a.NaOH b.NH3•H2O C.CuO d.CuSO4
②要获得纯净CuCl2•2H2O晶体的系列操作步骤为:向①所得滤液中加少量盐酸,蒸发浓缩、_____、_____、洗涤、干燥。
(4)用CuCl2•2H2O为原料制备CuCl 时,发现其中含有少量的CuCl 2或CuO杂质,若杂质是CuCl2,则产生的原因是______________。
(5)设计简单的实验验证0.1mol/L 的CuCl2溶液中的Cu2+ 对H2O2的分解具有催化作用:_____。
-
硒(Se)和铜(Cu)在生产生活中有广泛的应用。硒可以用作光敏材料、电解锰行业的催化剂,也是动物体必需的营养元素和对植物有益的营养元素等。氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下所示:

请回答下列问题:
(1)若步骤①中得到的氧化产物只有一种,则它的化学式是____________。
(2)写出步骤③中主要反应的离子方程式:____________________________________。
(3)步骤⑤包括用pH=2的溶液酸洗、水洗两步操作,酸洗采用的酸是__________(写酸的名称)。
(4)上述工艺中,步骤⑥和⑦的作用是_____________。
(5)Se为ⅥA族元素,用乙二胺四乙酸铜阴离子水溶液和硒代硫酸钠(Na2SeSO3)溶液反应可获得纳米硒化铜,硒代硫酸钠还可用于Se的精制,写出硒代硫酸钠(Na2SeSO3)与H2SO4溶液反应得到精硒的化学方程式:_____。
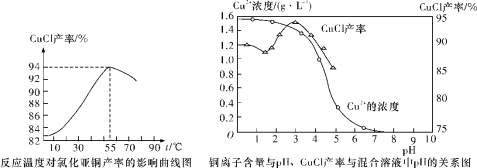
(6)氯化亚铜产率与温度、溶液pH关系如下图所示。据图分析,流程化生产氯化亚铜的过程中,温度过低影响CuCl产率的原因是____________________________________;温度过高、pH过大也会影响CuCl产率的原因是_______________________________。
(7)用NaHS作污水处理的沉淀剂,可以处理工业废水中的Cu2+。已知:25℃时,H2S的电离平衡常数Ka1=1.0×10-7,Ka2=7.0×10-15,CuS的溶度积为Ksp(CuS)=6.3×10-36。反应Cu2+(aq)+HS-(aq)  CuS(s)+H+(aq)的平衡常数K=__________(结果保留1位小数)。
CuS(s)+H+(aq)的平衡常数K=__________(结果保留1位小数)。
-
氯化亚铜是化工和印染等行业的重要原料,广泛用作有机合成的催化剂。
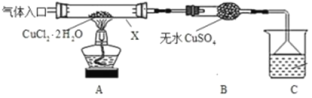
Ⅰ.甲采用CuCl2·2H2O热分解法制备CuCl,装置如图。
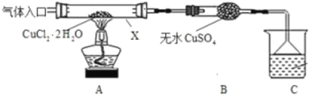
(1)仪器X的名称是_______________,C中烧杯的试剂可以是__________。
(2)“气体入口”通入的气体是_______。
(3)反应结束后,取所得产品分析,发现其中含有氧化铜,其可能原因是______________。
Ⅱ.乙另取纯净CuCl2固体用如下方法制备CuCl。

(4)操作②中反应的离子方程式为___________________。
(5)操作①中若用100 mL 10 mol/L盐酸代替0.2 mol/L盐酸,再通入SO2后,无白色沉淀产生。对此现象有如下两种猜想:
猜想一:c(H+)过大导致白色沉淀溶解。为验证此猜想,取75gCuCl2固体、100 mL0.2 mol/L盐酸及________mL10.0mol/LH2SO4配制成200 mL溶液,再进行操作②,观察是否有白色沉淀产生。
猜想二:_______________。请设计实验说明该猜想是否成立:_________________。
-
氯化亚铜是化工和印染等行业的重要原料,广泛用作有机合成的催化剂。
Ⅰ.甲采用CuCl2·2H2O热分解法制备CuCl,装置如图。
(1)仪器X的名称是_______________,C中烧杯的试剂可以是__________。
(2)“气体入口”通入的气体是_______。
(3)反应结束后,取所得产品分析,发现其中含有氧化铜,其可能原因是______________。
Ⅱ.乙另取纯净CuCl2固体用如下方法制备CuCl。

(4)操作②中反应的离子方程式为___________________。
(5)操作①中若用100 mL 10 mol/L盐酸代替0.2 mol/L盐酸,再通入SO2后,无白色沉淀产生。对此现象有如下两种猜想:
猜想一:c(H+)过大导致白色沉淀溶解。为验证此猜想,取75gCuCl2固体、100 mL0.2 mol/L盐酸及________mL10.0mol/LH2SO4配制成200 mL溶液,再进行操作②,观察是否有白色沉淀产生。
猜想二:_______________。请设计实验说明该猜想是否成立:_________________。
-
铜及其化合物应用广泛。
Ⅰ.氯化亚铜(CuCl)广泛用于化工、印染、有机合成等行业。以海绵铜(主要成分是Cu和少量CuO) 为原料,采用硝酸铵氧化分解技术生产氯化亚铜的工艺过程如下:
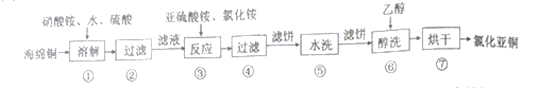
已知:CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易氧化。回答下列问题:
(1)步骤①中N 元素被还原为最低价,则Cu溶解的离子方程式为_______________。
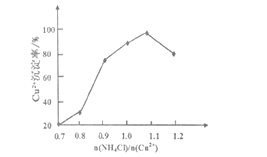
(2)步骤③中(NH4)SO3要适当过量,目的是使Cu2+充分还原,并保证Cu2+的还原速率和_____,其主要反应的离子方程式________________。已知NH4Cl、Cu2+的物质的量之比[n(NH4Cl]/n(Cu2+)] 与Cu2+沉淀率的关系如下图所示,当氯化铵用量增加到一定程度后Cu2+的沉淀率减少,原因是_____________________。
(3)步骤⑥中醇洗的目的是____________________________。
Ⅱ.以氧缺位铁酸铜(CuFe2O4-x)作催化剂,可利太阳能热化学循环法分解H2O制H2,其物质转化如图所示。
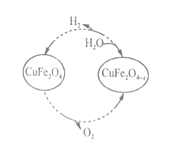
(4)氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为_______________。
(5)若x=0.15,则1mol CuFe2O4-x参与一次该循环,理论上能制得的H2体积为_______L(标准状况下)。
-
铜及其化合物应用广泛。
Ⅰ.氯化亚铜(CuCl)广泛用于化工、印染、有机合成等行业。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产氯化亚铜的工艺过程如下:
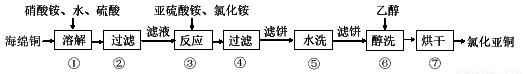
已知:CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易氧化。
回答下列问题:
(1)步骤①中N元素被还原为最低价,则Cu溶解的离子方程式为________。
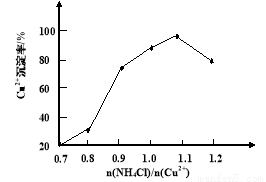
(2)步骤③中 (NH4)2SO3要适当过量,目的是使Cu2+充分还原速率和________,其主要反应的离子方程式为_________。已知NH4Cl、Cu2+的物质的量之比[n( NH4Cl )/n(Cu2+)]与Cu2+沉淀率的关系如右图所示,当氯化铵用量增加到一定程度后Cu2+的沉淀率减少,原因是________。
Ⅱ.以氧缺位铁酸铜(CuFe2O4-x)作催化剂,可利用太阳能热化学循环法分解H2O制H2,其物质转化如图甲所示。
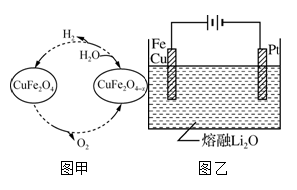
①氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为________。
②若x=0.15,则1 mol CuFe2O4参与该循环过程理论上一次能制得标准状况下的H2体积为________L。(标准状况下)
③CuFe2O4可用电化学方法得到,其原理如图乙所示,则阳极的电极反应式为__________。
-
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl是白色固体,难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以硫化铜精矿为原料生产CuCl的工艺过程如下:
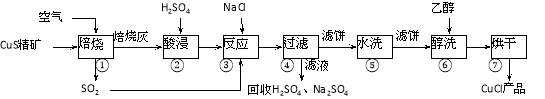
回答下列问题:
(1)CuS精矿经250 ℃低温焙烧后生成CuO,步骤②中主要反应的离子方程式是 。
(2)步骤③先加NaCl、通入SO2时无沉淀,加水稀释就产生大量白色沉淀,其原因是 。
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_______(写名称);步骤⑥醇洗的作用是 。
(4)已知25℃,101 kPa时:S(s)+O2(g)==SO2(g) ∆H=-296.8 kJ/mol
2Cu(s)+O2(g)==2CuO(s) ∆H=-314.6 kJ/mol
Cu(s)+S(s)==CuS(s) ∆H=-53.1 kJ/mol
步骤①中CuS与O2反应的热化学方程式是 。
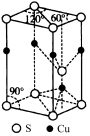
(5)CuS晶胞结构如图所示,其中含有硫原子的数目是 。
(6)假设上述①~③步反应完全转化,④~⑦步操作共损失产品3.5%,反应生成的硫酸全部被循环利用,则生产100 kg 96.5%的CuCl(Mr=99.0)产品,除循环利用之外,需要处理的尾气中含SO2 m3(标准状况)。
-
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
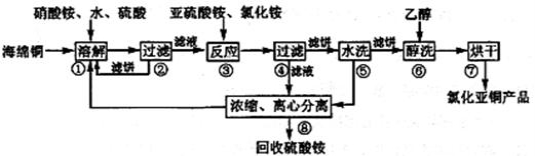
回答下列问题:
(1)写出“溶解”过程中发生的氧化还原反应的离子方程式(N元素被还原到最低价):_______,溶解温度应控制在60-70℃,原因是_______。
(2)写出步骤③中,氧化剂与还原剂的物质的量之比为________。已知NH4Cl、Cu2+的物质的量之比[n(NH4Cl)/n(Cu2+)]与Cu2+沉淀率的关系如图所示,当氯化铵用量增加到一定程度后的氯化亚铜的沉淀率减少,其可能的原因是__________。

(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_____(写名称),回收的主要物质是____(写化学式)
(4)上述工艺中,步骤⑥醇洗的作用是__________。
(5)称取2.000g CuCl样品(杂质不参与反应),溶于一定量的0.5000mol/L FeCl3溶液中,加水稀释至200mL得到溶于,取20.00mL用0.1000mol/L的Ce(SO4)2溶液滴定到终点,消耗20.00mL Ce(SO4)2
有关反应式:Fe3++CuCl═Fe2++Cu2++Cl﹣ Ce4++Fe2+═Fe3++Ce3+
则样品中CuCl的质量分数_________。
-
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:

回答下列问题:
(1)步骤①中氧化还原反应的离子方程式为__________,溶解温度应控制在60~70℃,原因是______。
(2)写出步骤③中主要反应的离子方程式__________。
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是__________(写名称)。
(4)上述工艺中,步骤⑥不能省略,理由是__________。
(5)准确称取所制备的氯化亚铜样品m g,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用amoI/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O72-被还原为Cr3+。样品中CuCl的质量分数为________。