-
298K 100kPa时,NH3(g)+HCl(g)═NH4Cl(s)△H1=-176kJ•mol-1
N2(g)+3H2(g)═2NH3(g)△H2=-92.2kJ•mol-1
H2(g)+Cl2(g)═2HCl(g)△H3=-184.6kJ•mol-1
298K时的N2(g)+4H2(g)+Cl2(g)═2NH4Cl(s)△H=______.高三化学解答题中等难度题查看答案及解析
-
按照盖斯定律,结合下列反应方程式,回答问题.已知:
(1)NH3(g)+HCl(g)=NH4Cl(s)△H=-176KJ•mol-1
(2)NH3(g)+H2O(l)=NH3•H2O(aq)△H=-35.1KJ•mol-1
(3)HCl(g)+H2O(l)=HCl(aq)△H=-72.3KJ•mol-1
(4)NH3•H2O(aq)+HCl(aq)=NH4Cl(aq)+H2O(l)△H=-52.3KJ•mol-1
(5)NH4Cl(S)+H2O(l)=NH4Cl(aq)△H=Q
则第(5)个方程式中的反应热是________ KJ•mol-1.高三化学填空题中等难度题查看答案及解析
-
已知: (1)NH3(g)+HCl(g)=NH4Cl(s); △H1=-76kJ·mol-1
(2)NH3(g)+H2O(l)=NH3·H2O(aq); △H2=-35.1kJ·mol-1
(3)HCl(g)+HCl (aq); △H3=-72.3kJ·mol-1
(4)HCl (aq) NH3·H2O(aq) =NH4Cl(aq)+H2O(l); △H4=-52.3kJ·mol-1
(5)NH4Cl(s)=NH2Cl(aq); △H5=?
根据盖斯定律,则(5)方程式中的反应热△H5为
A.-335.7 kJ·mol-1 B.-16.3 kJ·mol-1
C.+16.3 kJ·mol-1 D.-83.7 kJ·mol-1
高三化学选择题中等难度题查看答案及解析
-
已知下列四个热化学方程式:
NH4Cl(s)===NH3(g)+HCl(g) ΔH1=a kJ/mol ①
Ba(OH)2·8H2O(s)===BaO(s)+9H2O(l) ΔH2=b kJ/mol ②
2NH4Cl(s)+Ba(OH)2·8H2O(s)===BaCl2(aq)+2NH3(g)+10H2O(l) ΔH3=c kJ/mol ③ BaO(s)+2HCl(aq)===BaCl2(aq)+H2O(l) ΔH4=d kJ/mol ④
其中a、b、c均大于0,HCl气体溶解于水,溶液温度升高。由此可知下列判断一定正确的是( )
A. d<0 B. c<2a+b+d C. c=2a+b+d D. c>2a+b+d
高三化学选择题中等难度题查看答案及解析
-
已知在298K和101kPa条件下,有如下反应:
反应Ⅰ:C(s) + O2(g) = CO2(g) △ H1=-393.5 kJ·mol-1
反应Ⅱ:2C(s) + O2(g) = 2CO(g) △ H2=-221 kJ·mol-1
反应Ⅲ:N2(g) + O2(g) = 2NO(g) △ H3=+180.5 kJ·mol-1
试回答下列问题:
(1)汽车尾气净化原理为反应Ⅳ:2NO(g) + 2CO(g)
N2(g) + 2CO2(g) △ H=______,该反应能自发进行的条件是_______。(填“高温”、“低温”或“任意温度”)。
(2)如果在一定温度下,体积为 2 升的密闭容器中发生化学反应Ⅳ,0~4min各物质物质的量的变化如下表所示:
物质(mol)
时间
NO
CO
N2
CO2
起始
0.40
1.0
2 min 末
2.0
0.80
1.6
4 min 末
1.6
①求 0~2min 内用 CO 来表示的平均反应速率 v(CO)=________。
②试计算该温度下反应Ⅳ 的化学平衡常数 K=_________。
(3)若一定温度下,在容积可变的密闭容器中,上述反应Ⅳ达到平衡状态,此时容积为3L, c(N2)随时间 t 的变化曲线 x 如图所示。
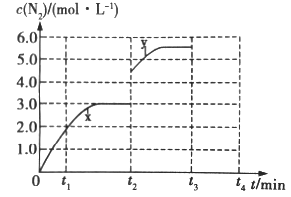
①若在 t2min时改变一个条件,c(N2)随反应时间 t 的变化如曲线 y 所示,则改变的条件是______。
②若在t2min时升高温度,t3min时重新达到平衡,请在图中画出在 t2~t4 内 c(N2)的变化曲线______。
高三化学简答题困难题查看答案及解析
-
德国人哈伯在1909年发明的合成氨反应原理为:N2(g)+3H2(g)⇌2NH3(g) 已知298K时:△H=-92.4kJ•mol-1试回答下列问题:
(1)在298K时,将10mol N2和30mol H2放入合成塔中,为何放出的热量小于924kJ?________.
(2)如图一在一定条件下,将1mol N2与3mol H2混合于一个10L密闭容器中,反应达到A平衡时,混合气体中氨占25%,试回答:
①N2的转化率αA为________.
②在状态A时,平衡常数KA=________(代入数值的表达式,不写出具体数值)当温度由T1变化到T2时,KA________KB(填“>”、“<”或“=”)
(3)图二是实验室模拟工业法合成氨的简易装置.简述检验有氨气生成的方法________.在1998年希腊亚里斯多德大学的Marmellos和Stoukides采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电化学合成氨.其实验装置如图.阴极的电极反应式________.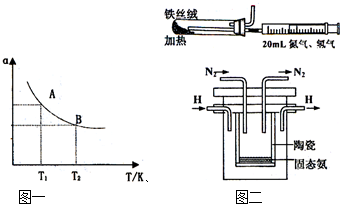
高三化学填空题中等难度题查看答案及解析
-
298K时,合成氨反应的热化学方程式为:
N2(g)+3H2(g)
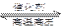 2NH3(g);△H=-92.4kJ·mol-1
2NH3(g);△H=-92.4kJ·mol-1在该温度下,取1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量总是小于92.4 kJ是______________________________________________。
高三化学填空题简单题查看答案及解析
-
(1)298K、100kPa时,C(s,石墨)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1 2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ•mol-1 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1,请写出298K时由C(s,石墨)和H2(g)生成1molC2H2(g)的热化学方程式______;
(2)水是生命之源,也是化学反应中的主角.试回答下列问题:A.B.C是中学化学常见的三种有色物质(其组成的元素均属短周期元素),它们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,请写出A.B.C与水反应的化学方程式:______;
(3)写出硫化钠在水溶液中水解的离子方程式______在配制硫化钠溶液时,为了防止发生水解,可以加入少量的______;
(4)明矾可做净水剂是因为______,有关的离子方程式为______;向明矾的水溶液中加入饱和的小苏打溶液,则观察到的现象是______,有关的离子方程式______;
(5)下列哪些事实能说明醋酸是弱酸______
①醋酸不易腐蚀衣服;
②0.1mol/L的CH3COONa溶液的PH约为9;
③进行中和滴定时,等体积等物质的量浓度的H2SO4溶液比等体积等物质的量浓度的CH3COOH溶液消耗的NaOH溶液多;
④0.1mol/L的CH3COOH溶液PH约为2.9;
⑤相同体积的PH均等于4的盐酸和CH3COOH溶液,被同一物质的量浓度的NaOH溶液中和,CH3COOH溶液消耗的NaOH溶液多;
⑥镁粉与一定量稀硫酸反应,如果向其中加入少量醋酸钠可以降低反应速率但不改变产生气体的总量.高三化学解答题中等难度题查看答案及解析
-
联氨(N2H4)是一种绿色环保的还原剂,其氧化产物为氮气。
(1)合成联氨的有关反应如下:
NH3(g)+NaClO(aq)=NH2C1(I)+NaOH(aq) △H1=-67.45 kJ ·mol-1
NH2Cl(1)+NaOH(aq)+NH3(g)=N2H4(I)+NaCl(aq)+ H2O(I) △H2 = - 195.32 kJ ·mol-1
反应2NH3(g)+NaClO(ap)=N2H4(I)+NaCl(aq)+H2O(I) △H=__________kJ ·mol-1
(2)联氨为二元弱碱,在水中的电离方式与氨相似.写出联氨与过量盐酸反应的离子方程式_____________。
(3)联氨-空气燃料电池是一种碱性燃料电池,电解质溶液是20%〜30%的KOH溶液。该电池放电时,负极的电极反应式是__________________。
(4)在高温下,N2H4可完全分解为NH3、N2及H2 ,实验测得分解产物中N2与H2的物质的量之比为3:2,,则该分解反应的化学方程式为_____________________。
(5)联氨常用于化学镀镍废料中回收金属镍,反应体系的pH对镍的回收率的影响如下图左所示,则利用联氨回收金属镍时溶液的pH应控制在__________,在确定合适的pH后,取100 mL化学镀镍废液,分别加入不同体积的联氨,镍的冋收率如下图右所示,则联氨的合理用量为_________mL,联氨的体积超过2.5 mL时,金属镍的冋收率降低,其可能的原因是________________。
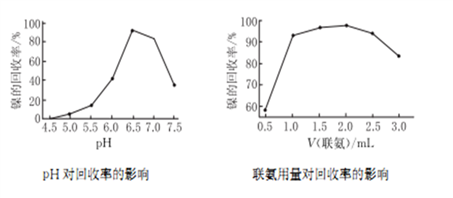
高三化学简答题困难题查看答案及解析
-
已知:
①N2(g)+O2(g)===2NO(g) ΔH1=+180 kJ·mol-1
②N2(g)+3H2(g)
2NH3(g) ΔH2=-92.4 kJ·mol-1
③2H2(g)+O2(g)===2H2O(g) ΔH3=-483.6 kJ·mol-1
下列说法正确的是

A.反应②中的能量变化如图所示,则ΔH2=E1-E3
B.H2的燃烧热为241.8 kJ·mol-1
C.氨的催化氧化反应为4NH3(g)+5O2(g)===4NO(g)+6H2O(g) ΔH=+906 kJ·mol-1
D.由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1
高三化学单选题困难题查看答案及解析