-
某工业废玻璃粉末含SiO2、Fe2O3、CeO2、FeO等。某课题小组设计如下工艺流程对资源进行回收,得到Ce(OH)4和硫酸铁铵矾。已知:CeO2不溶于稀硫酸;酸性条件下,Ce3+易水解,Ce4+有较强氧化性。

(1)硫酸铁铵矾可净水,其原理是(写离子方程式) 。
(2)滤液A的主要成分 (填写化学式)。
(3)反应①中H2O2是 (“氧化剂”或“还原剂”)。
(4)反应②的化学反应方程式是 。
(5)已知制硫酸铁铵矾晶体[Fe2(SO4) 3·(NH4) 2SO4·24H2O,式量964]的产率为80%,若加入13.2g (NH4) 2SO4(式量132),可制得晶体的质量是 g。
(6)化合物HT可作为萃取剂能将铈离子从水溶液中萃取出来,过程表示为:
Ce2(SO4)3 (水层)+ 6HT(有机层) 2CeT3 (有机层)+3H2SO4(水层
2CeT3 (有机层)+3H2SO4(水层 )
)
分液得到CeT3(有机层),再加入H2SO4 获得较纯的含Ce3+的水溶液。可选择硫酸作反萃取剂的原因是 (从平衡移动角度回答)。
-
二氧化铈(CeO2)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。
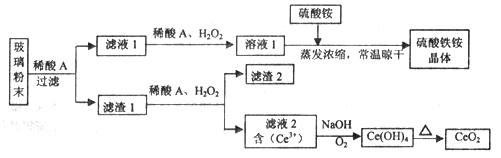
已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
(1)稀酸A的分子式是_____________________。
(2)滤液1中加入H2O2溶液的目的是__________________。
(3)设计实验证明滤液1中含有Fe2+_____________________。
(4)已知Fe2+溶液可以和难溶于水的FeO(OH)反应生成Fe3O4,书写该反应的离子方程式____________。
(5)由滤液2生成Ce(OH)4的离子方程式__________________。
(6)硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是___________________。
(7)取上述流程中得到的Ce(OH)4产品0.531 g,加硫酸溶解后,用浓度为0.l000mol·L-1FeSO 4标准溶液滴定至终点时(铈被还原为Ce3+ ),消耗25.00 mL标准溶液。该产品中Ce(OH)4的质置分数为_______(结果保留两位有效数字)。
-
二氧化铈(CeO2)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。
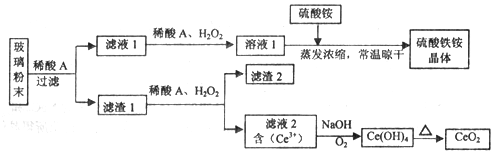
已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
(1)稀酸A的分子式是_____________________。
(2)滤液1中加入H2O2溶液的目的是__________________。
(3)设计实验证明滤液1中含有Fe2+_____________________。
(4)已知Fe2+溶液可以和难溶于水的FeO(OH)反应生成Fe3O4,书写该反应的离子方程式____________。
(5)由滤液2生成Ce(OH)4的离子方程式__________________。
(6)硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是___________________。
(7)取上述流程中得到的Ce(OH)4产品0.531 g,加硫酸溶解后,用浓度为0.l000mol·L-1FeSO 4标准溶液滴定至终点时(铈被还原为Ce3+ ),消耗25.00 mL标准溶液。该产品中Ce(OH)4的质置分数为_______(结果保留两位有效数字)。
-
二氧化铈(CeO2)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含 等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
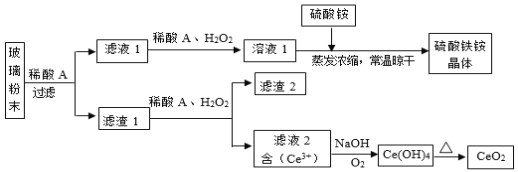
(1)稀酸A的分子式是___________。
(2)滤液1中加入H2O2溶液的目的是___________。
(3)设计实验证明滤液1中含有Fe2+____________。
(4)在酸性溶液中,已知Fe2+溶液可以和难溶于水的FeO(OH)反应生成Fe3O4,书写该反应的离子方程式________________。
(5)由滤液2生成 的离子方程式______________。
的离子方程式______________。
(6)硫酸铁铵晶体 广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是_________。
广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是_________。
(7)取上述流程中得到的 产品0.832g,加硫酸溶解后,用浓度为0.1000
产品0.832g,加硫酸溶解后,用浓度为0.1000 的
的 标准溶液滴定至终点时(铈被还原为
标准溶液滴定至终点时(铈被还原为 ),消耗20.00mL标准溶液。该产品中
),消耗20.00mL标准溶液。该产品中 的质量分数为___________。
的质量分数为___________。
-
铝鞣剂在皮革工业有广泛应用。某学习小组以铝灰(主要成分是Al、A12O3、FeO、SiO2等)为原料制备铝鞣剂[Al(OH)2Cl],设计工艺流程如下图所示:
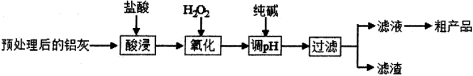
已知:
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 2.8 |
| A13+ | 3.4 | 4.7 |
| Fe2+ | 5.8 | 8.8 |
请回答下列问题:
(1)酸浸时温度控制在30℃-35℃,不宜太低,也不宜太高,其原因是_________。
(2)氧化时的离子方程式为_________。
(3)调节溶液的pH范围为_________。
(4)滤渣中主要含有物质的化学式是_________。
-
(孔雀石主要成分Cu2(OH)2CO3 (含少量FeO、SiO2)。某兴趣小组用孔雀石制备CuSO4·5H2O,所设计的工艺流程如下所示:
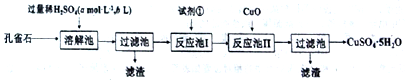
回答下列问题:
(1)从CuSO4溶液中获取CuSO4·5H2O所进行的操作是加热、蒸发浓缩、________、过滤。
(2)溶解池中所发生的化学反应方程式为_________________,_________________。
(3)选择的试剂①为_________。
A.KMnO4 B.NaClO C.Cl2 D.H2O2
反应池Ⅰ中发生反应的离子方程式为________________________________。
(4)含Cu2(OH)2CO3质量分数为c%的孔雀石dg,理论上能获取CuSO4·5H2O的质量为___________。
-
某地煤矸石经预处理后主要含SiO2(61%)、Al2O3(30%)和少量的Fe2O3、FeO及MgO。实验小组设计如下流程用其制备碱式硫酸铝[Al2(OH)4SO4]:
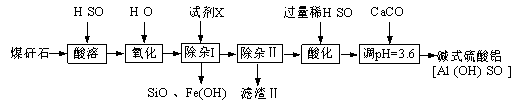
(1)为提高“酸浸”时铝浸出率,可采取的措施之一是 。
(2)氧化时应控制反应温度在10℃~20℃,其原因是 ,“氧化”时可用MnO2替代,发生的离子方程式 。
(3)试剂X为 ,设计一个简单的实验,证明铁元素已被沉淀完全: 。
(4)加入CaCO3制备碱式硫酸铝的化学方程式 。
-
工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:
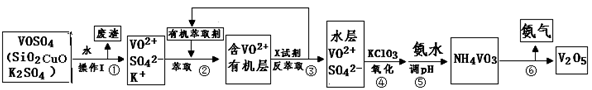
请回答下列问题:
(1)步骤①所得废渣的成分是 (写化学式),操作I的名称 。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):R2(SO4)n (水层)+ 2nHA(有机层) 2RAn(有机层)+ nH2SO4(水层)
2RAn(有机层)+ nH2SO4(水层)
②中萃取时必须加入适量碱,其原因是 。
③中X试剂为 。
(3)⑤的离子方程式为 。
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 0 | 1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为 ;若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)< 。〖已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39〗
(5)该工艺流程中,可以循环利用的物质有 和 。
-
工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:
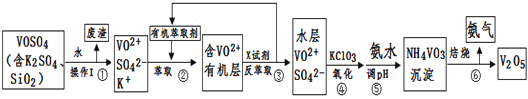
请回答下列问题:
(1)步骤①所得废渣的成分是____________写化学式),操作I的名称______。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n(水层)+ 2nHA(有机层) 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是____________________________。
③中X试剂为___________________。
(3)⑤的离子方程式为________________________。
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为__________;
若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)<_____________。
(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
(5)该工艺流程中,可以循环利用的物质有______________和_______。
-
工业上利用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2等)为原料制备高档颜料铁红(Fe2O3 ),具体生产流程如下:

试回答下列问题:
(1)滤液X中含有的金属阳离子是________(填离子符号)。
(2)步骤Ⅲ中可选用________试剂调节溶液的pH(填字母)。
A.稀硝酸 B.氨水 C.氢氧化钠溶液 D.高锰酸钾溶液
(3)过滤操作中除了玻璃棒、烧杯还需要的玻璃仪器是________。
(4)步骤Ⅳ的反应温度一般需控制在35℃以下,其目的是________。
(5)在空气中煅烧FeCO3生成产品氧化铁的化学方程式为________。

2CeT3 (有机层)+3H2SO4(水层
)








