-
实现“低碳经济”的一项重要课题就是研究如何将CO2转化为可利用的资源。因此,研究CO2 的综合利用对“低碳社会”的构述构建具有重要意义。
(1)一定条件下CO2可以和铁反应:Fe(s)+CO2(g) FeO(s)+CO(g),该反应的平衡常数(K)与温度(T)的关系如图甲所示:
FeO(s)+CO(g),该反应的平衡常数(K)与温度(T)的关系如图甲所示:
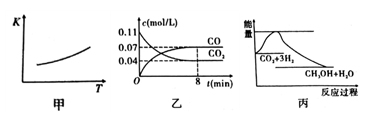
①该反应的△H______0(填“<”、“=”或“>”)。
②下列措施,能使平衡时 增大的是______(填序号)。
增大的是______(填序号)。
A.充入一定量的CO B.升高温度 C.使用催化剂
③一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2,反应过程中CO2和CO的物质的量浓度与时间的关系如图乙所示。该反应的平衡常数K=_____________。
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),图丙表示该反应过程中能量的变化。
CH3OH(g)+H2O(g),图丙表示该反应过程中能量的变化。
①下列关于该反应的说法,正确的是______(填序号)。
A.△H<0,△S<0 B.△H>0,△S<0 C.△H>0,△S>0 D.△H<0,△S>0
②已知:CO2(g)+3H2(g) CH3OH(l)+H2O(l) △H=-143.0kJ•mol-1;
CH3OH(l)+H2O(l) △H=-143.0kJ•mol-1;
H2(g)+  O2(g)=H2O(l) △H=-285.8kJ•mol-1。
O2(g)=H2O(l) △H=-285.8kJ•mol-1。
写出表示CH3OH燃烧热的热化学方程式:________________________________。
③一种以甲醇为原料的燃料电池,使用合适的合金为电极,以氢氧化钠溶液、甲醇、氧气为原料,该电池负极的电极反应式为_______________________________。
(3)以CO2为原料还可以合成多种氮肥。
①工业上由CO2和NH3在一定条件下合成尿素的化学方程式为CO2(g)+2NH3(g) CO(NH2)2(l)+H2O(g)。起始以
CO(NH2)2(l)+H2O(g)。起始以 =5投料进行反应,达到化学平衡时CO2的转化率为60%,则NH3的平衡转化率为______________。
=5投料进行反应,达到化学平衡时CO2的转化率为60%,则NH3的平衡转化率为______________。
②将足量CO2通入饱和氨水中可制得碳铵(NH4HCO3)。已知室温下Kb(NH3·H2O)=1.8×10-5,Kal(H2CO3)=4.3×10-7,则 0.lmol/LNH4HCO3 溶液呈_________(填“酸性”“中性”或“碱性”)。
-
实现节能减排和低碳经济的一项重要课题就是研究如何将CO2转化为可利用的资源,目前工业上有一种方法是用CO2来生产燃料甲醇,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ/mol ) 的变化,据此回答下列有关问题:
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ/mol ) 的变化,据此回答下列有关问题:
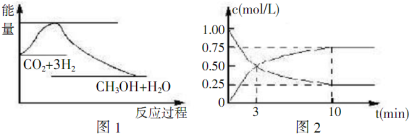
(1)25℃时,1.01×105Pa,16g液态甲醇完全燃烧,当恢复到原状态时放出363.3kJ的热量,写出该反应的热化学方程式______________。
(2)为探究反应原理,现进行如下实验:某温度下,在体积为lL的密闭容器中充入lmolCO2和4molH2,一定条件下发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2的浓度随时间变化如上图2所示.
CH3OH(g)+H2O(g),测得CO2的浓度随时间变化如上图2所示.
①从反应开始到平衡,CH3OH的平均反应速率v(CH3OH)=______________;H2的转化率为______________.
②若向该容器中加入 amolCO2、bmolH2、cmolCH3OH(g)和dmolH2O(g),且a、b、c、d均大于0,在相同条件下达到平衡时,混合物中各组分的物质的量与上述平衡相同,试比较反应放出的能量:①______________②(填“大于”“小于” 或“等于”)
③下列措施中能使H2的转化率提高的是______________(填字母)。
A.升高温度 B.将CH3OH(g)及时液化抽出
C.选择高效催化剂 D.相同条件下 再充入lmolCO2和4molH2
(3)甲醇是一种可再生能源具有广泛的开发和应用前景。某实验小组用一种以甲醇为原料的燃料电池作为电源,设计了一种电解法制取Fe(OH)2的实验装置如(下图所示),通电后溶液中产生大量白色沉淀且较长时间不变色。
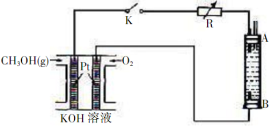
①该燃料电池的负极反应为______________。
②下列说法中正确的是______________(填序号)
A.电源中的负极附近 pH升高
B.电极B的发生氧化反应
C.A、B两端都必须用铁作电极
D.阴极发生的反应是2H++2e-=H2↑
E.电解的电解质溶液可以是CuSO4溶液
③若电池中甲醇的通入量为8g,且反应完全,则理论上最多能产生沉淀______________g。
-
(14分)实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
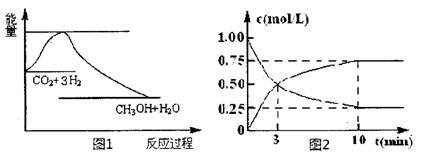
(1)关于该反应的下列说法中,正确的是____________(填字母)。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1mol CO2和 4molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,CH3OH的平均反应速率v(CH3OH)=___________;H2的转化率w(H2)=_________________。
②该反应的平衡常数表达式K=____________。
③下列措施中能使化学平衡向正反应方向移动的是___________(填字母)。
A.升高温度 B.将CH3OH(g)及时液化抽出
C.选择高效催化剂 D.再充入1molCO2和4 molH2
(3)25℃,1.01×10 5Pa时,16g液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式:__________________________。
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此电池的负极应加入和通入的物质有_____________;其正极的电极反应式是:_____________________。
-
实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业上有一种方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),图1表示该反应过程中能量变化:
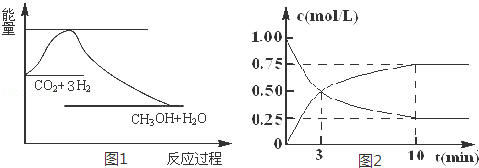
(1)关于该反应的下列说法中,正确的是 (填字母).
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),测得CO2和CH3O(g)的浓度随时间变化如图2所示.
①从反应开始到平衡,CO2的平均反应速率v(CO2)= mol/(L.min)
②该反应的平衡常数表达式K=
③下列措施中能使化学平衡向正反应方向移动的是 (填字母)
A.升高温度 B.将CH3OH(g)及时液化抽出 C.选择高效催化剂
(3)25℃,1.01105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式: .
-
实现 “节能减排” 和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
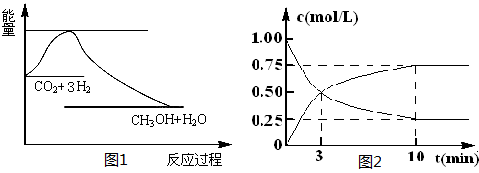
(1)关于该反应的下列说法中,正确的是________(填字母)。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,CH3OH的平均反应速率v(CH3OH) =________ ;H2的转化率w(H2) =。
②该反应的平衡常数表达式K=________。
③下列措施中能使化学平衡向正反应方向移动的是 (填字母)。
A.升高温度
B.将CH3OH(g)及时液化抽出
C.选择高效催化剂
D.再充入l molCO2和4 molH2
(3)25℃,1.01×105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式:________。
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此电池的负极应加入和通入的物质有________;其正极的电极反应式是:________。
-
实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化如图,关于该反应的下列说法中,正确的是
CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化如图,关于该反应的下列说法中,正确的是
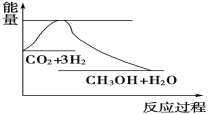
A. ΔH>0,ΔS>0 B. ΔH>0,ΔS<0 C. ΔH<0,ΔS>0 D. ΔH<0,ΔS<0
-
实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化如图,关于该反应的下列说法中,正确的是
CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化如图,关于该反应的下列说法中,正确的是
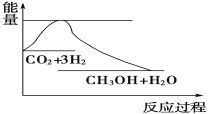
A. ΔH>0,ΔS>0 B. ΔH>0,ΔS<0 C. ΔH<0,ΔS>0 D. ΔH<0,ΔS<0
-
CO2的资源化利用一直是化学家们关注的重要课题,中科院大连化学物理研究所设计了一种新型多功能复合催化剂,成功地实现了CO2直接加氢制取高辛烷值汽油: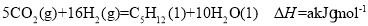 (反应①),该研究成果被评价为“CO2催化转化领域的突破性进展”。
(反应①),该研究成果被评价为“CO2催化转化领域的突破性进展”。
(1)已知氢气的燃烧热为 ,若要利用
,若要利用 的燃烧热求a的值,则还需要知道一个反应的
的燃烧热求a的值,则还需要知道一个反应的 ,该反应是________________________________。反应①在一定条件下具有自发性,则a_______________0(填“>”或“<”)。
,该反应是________________________________。反应①在一定条件下具有自发性,则a_______________0(填“>”或“<”)。
(2)向某密闭容器中按一定投料比充入 、
、 ,控制条件使其发生反应:
,控制条件使其发生反应: 。测得
。测得 的平衡转化率与温度、压强之间的关系如图1所示:
的平衡转化率与温度、压强之间的关系如图1所示:
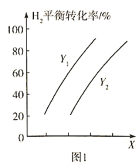
则X表示______________, ___________
___________ (填“>”或“<”)。欲提高
(填“>”或“<”)。欲提高 的平衡转化率并提高单位时间内
的平衡转化率并提高单位时间内 的产量,可采取的措施是______________________(填两种)。
的产量,可采取的措施是______________________(填两种)。
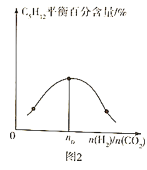
(3)控制一定温度、催化剂,按不同投料比 将反应物通入到某密闭容器中,测得平衡时
将反应物通入到某密闭容器中,测得平衡时 的百分含量与投料比之间的关系如图2所示,则
的百分含量与投料比之间的关系如图2所示,则 ____________。
____________。
(4)在钌-铑双金属催化剂的作用下,CH3OH、CO2、H2可高效地转化为乙酸,反应方程式为 。一定温度下,向某刚性容器中通入等物质的量的三种原料气,测得体系中的总压强与时间的关系如下表所示:
。一定温度下,向某刚性容器中通入等物质的量的三种原料气,测得体系中的总压强与时间的关系如下表所示:
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| p/kPa | 3 | 2.7 | 2.5 | 2.35 | 2.26 | 2.2 | 2.2 |
则反应开始到达到平衡的过程中, ______________
______________ ______________
______________ 。
。
(5)碳捕捉技术的发展也有利于CO2在资源应用方面得到充分利用。常温下,若某次用NaOH溶液捕捉空气中的CO2所得溶液的pH=10,并测得溶液中 ,则
,则 _____________
_____________ 。
。
-
CO2是地球上取之不尽用之不竭的碳源,将CO2应用于生产中实现其综合利用是目前的研究热点。
(1)由CO2转化为羧酸是CO2资源化利用的重要方法。
I.在催化作用下由CO2和CH4转化为CH3COOH的反应历程示意图如图。
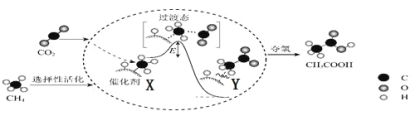
①在合成CH3COOH的反应历程中,下列有关说法正确的是_____。(填字母)
a.该催化剂使反应的平衡常数增大
b.CH4→CH3COOH过程中,有C—H键发生断裂
c.由X→Y过程中放出能量并形成了C—C键
②该条件下由CO2和CH4合成CH3COOH的化学方程式为_____。
II.电解法转化CO2制HCOOH的原理如图。
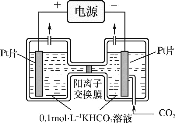
①写出阴极CO2还原为HCOO-的电极反应式:_____。
②电解一段时间后,阳极区的KHCO3溶液浓度降低,其原因是_____。
(2)由CO2合成甲醇是CO2资源化利用的重要方法。研究表明在催化剂作用下CO2和H2可发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH
CH3OH(g)+H2O(g) ΔH
①有利于提高合成CH3OH反应中CO2的平衡转化率的措施有_____。(填字母)
a.使用催化剂 b.加压 c.增大初始投料比
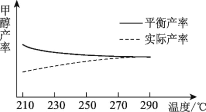
②研究温度对于甲醇产率的影响。在210℃~290℃保持原料气中CO2和H2的投料比不变,得到甲醇的实际产率、平衡产率与温度的关系如图所示。ΔH____0(填“>”或“<”),其依据是____。
-
中共十九大报告指出,加快水污染防治、实施流域环境和近岸海域综合治理、环境污染的治理是化学工作者研究的重要课题,也是践行“绿水青山就是金山银山”的重要举措。在适当的条件下,将CO2转化为甲醇、甲醚等有机物,既可降低CO2造成的温室效应对环境的影响,还可得到重要的有机产物。
(1)已知:①2H2(g)+O2(g)=2H2O(g) ΔH1=−484 kJ/mol
②CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH2=−50 kJ/mol
CH3OH(g)+H2O(g) ΔH2=−50 kJ/mol
则2CH3OH(g)+3O2(g)= 2CO2(g)+4H2O(g) ΔH,ΔH=_____________。
(2)已知T K时,某恒容密闭容器中存在如下反应:2CO2(g)+6H2(g)  CH3OCH3(g)+3H2O(g) ΔH<0,测得容器中不同时刻时各物质的浓度(mol/L)如下表所示:
CH3OCH3(g)+3H2O(g) ΔH<0,测得容器中不同时刻时各物质的浓度(mol/L)如下表所示:
| c(CO2) | c(H2) | c(CH3OCH3) | c(H2O) |
| 开始时 | a | b | 0 | 0 |
| 10 s时 | 3 | 0.5 | c | 1.5 |
①若反应开始到10s时间段内,v(H2)=_____________,既能提高反应速率,又能提高H2转化率的方法是________________________。
②若T K时,化学平衡常数K=15,则10 s 时v(正)_______v(逆)(填“>”“<”或“=”),此时CO2的转化率为________。
(3)一定条件下,向某恒容密闭容器中充入x mol CO2和y mol H2,发生的反应为CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH=−50 kJ·mol−1。
CH3OH(g)+H2O(g) ΔH=−50 kJ·mol−1。
①下图1中能表示该反应的平衡常数K与温度T之间的变化关系曲线为______(填“a”或“b”),其判断依据是__________________________________。
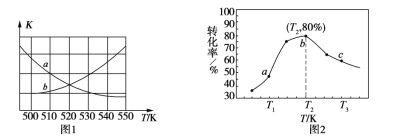
②若x=2、y=3,测得在相同时间内不同温度下H2的转化率如图2所示,则在该时间段内,恰好达到化学平衡时,容器内的压强与反应开始时的压强之比为____________。
FeO(s)+CO(g),该反应的平衡常数(K)与温度(T)的关系如图甲所示:

增大的是______(填序号)。
CH3OH(g)+H2O(g),图丙表示该反应过程中能量的变化。
CH3OH(l)+H2O(l) △H=-143.0kJ•mol-1;
O2(g)=H2O(l) △H=-285.8kJ•mol-1。
CO(NH2)2(l)+H2O(g)。起始以
=5投料进行反应,达到化学平衡时CO2的转化率为60%,则NH3的平衡转化率为______________。







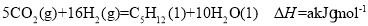 (反应①),该研究成果被评价为“CO2催化转化领域的突破性进展”。
(反应①),该研究成果被评价为“CO2催化转化领域的突破性进展”。




