-
沉淀碳酸钙主要用于食品、医药等行业。以精选石灰石 含有少量
含有少量 、
、 杂质
杂质 为原料制备沉淀碳酸钙的工艺流程如下:
为原料制备沉淀碳酸钙的工艺流程如下:

 流程中可以循环利用的物质有气体 Ⅰ、气体Ⅱ和____
流程中可以循环利用的物质有气体 Ⅰ、气体Ⅱ和____ 填化学式
填化学式 。
。
 “碳化”时发生反应的离子方程式为 ______________,该过程中通入气体Ⅰ和气体Ⅱ的顺序是________。
“碳化”时发生反应的离子方程式为 ______________,该过程中通入气体Ⅰ和气体Ⅱ的顺序是________。
 工业上常用电解氯化钠和氯化钙熔融物来制备金属钠,原理如下图所示:
工业上常用电解氯化钠和氯化钙熔融物来制备金属钠,原理如下图所示:

 电解过程中,加入氯化钙的目的是________。
电解过程中,加入氯化钙的目的是________。
 石墨电极发生的电极反应为________。
石墨电极发生的电极反应为________。
-
沉淀碳酸钙主要用于食品、医药等行业。以精选石灰石(含有少量MgCO3、FeCO3杂质)为原料制备沉淀碳酸钙的工艺流程如下:
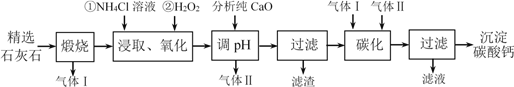
(1)流程中可以循环利用的物质有气体Ⅰ、气体Ⅱ和__________(填化学式)。
(2)“碳化”时发生反应的离子方程式为________________,该过程中通入气体Ⅰ和气体Ⅱ的顺序是________________。
(3)工业上常用电解氯化钠和氯化钙熔融物来制备金属钠,原理如下图所示:

①电解过程中,加入氯化钙的目的是________________。
②石墨电极发生的电极反应方程式为________________。
③电解得到的Na中约含1%的Ca,除去其中少量Ca的方法为________________。
已知部分物质的熔沸点如下表:

-
沉淀碳酸钙主要用于食品、医药等行业。以精选石灰石(含有少量MgCO3、FeCO3杂质)为原料制备沉淀碳酸钙的工艺流程如下:
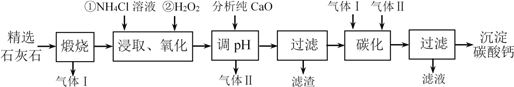
(1)流程中可以循环利用的物质有气体Ⅰ、气体Ⅱ和__________(填化学式)。
(2)“碳化”时发生反应的离子方程式为________________,该过程中通入气体Ⅰ和气体Ⅱ的顺序是________________。
(3)工业上常用电解氯化钠和氯化钙熔融物来制备金属钠,原理如下图所示:
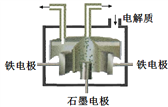
①电解过程中,加入氯化钙的目的是________________。
②石墨电极发生的电极反应方程式为________________。
③电解得到的Na中约含1%的Ca,除去其中少量Ca的方法为________________。
已知部分物质的熔沸点如下表:
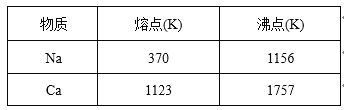
-
硫酸镍广泛应用于电镀、催化、医药等行业中,具有很高的经济价值。一种用含镍废催化剂(主要含 、C,还含有铝、铁的单质及氧化物,和少量有机物)为原料制备
、C,还含有铝、铁的单质及氧化物,和少量有机物)为原料制备 的工艺流程如下:
的工艺流程如下:

部分阳离子以氢氧化物形式沉淀时的 如下:
如下:
| 沉淀物 | 开始沉淀时的 | 完全沉淀时的 |
| 
| 2.7 | 3.2 |
| 
| 7.6 | 9.7 |
| 
| 7.1 | 9.2 |
回答下列问题:
(1)滤液a中溶质的主要成分除 外,还含有_________________(填化学式)。
外,还含有_________________(填化学式)。
(2)酸溶前需进行“热处理”的主要目的是____________;滤渣b主要成分是________(填化学式)。
(3)加入 溶液时发生反应的离子方程式为_______;简述加入
溶液时发生反应的离子方程式为_______;简述加入 除杂的原理_______。
除杂的原理_______。
(4)操作d为________、过滤、洗涤、干燥;产品晶体中有时会混有少量 ,其原因可能是__________。(写出一点即可)
,其原因可能是__________。(写出一点即可)
(5)取ag上述流程制得的硫酸镍晶体样品溶于蒸馏水中,在不断搅拌下缓慢加入足量丁二酮肟溶液 ,再加入
,再加入 溶液调节溶液的
溶液调节溶液的 在8~9,充分反应后,过滤、洗涤、烘干、称量得到红色固体质量为bg。发生反应的方程式为
在8~9,充分反应后,过滤、洗涤、烘干、称量得到红色固体质量为bg。发生反应的方程式为 (红色)
(红色) ,已知
,已知 相对分子质量为M,列式计算样品纯度为_________。
相对分子质量为M,列式计算样品纯度为_________。
-
(16分)医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙为原料(含量为97.5%A,含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙的主要流程如下:
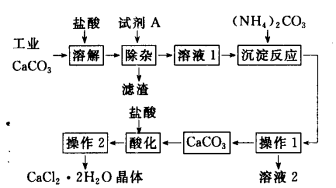
(1)除杂操作时加入试剂A,调节溶液的pH为8.0~8.5,以除去溶液中少量的Al3+、Fe3+。试剂A可以选择 ________________________________。
a.Ca(OH)2 b.NaOH c.NH3 d.Na2CO3
(2)检验溶液1中是否含Fe3+的方法是____________________________
(3)请指出下列操作的名称:操作1_______;操作2___________;请指出操作1中所用的玻璃仪器的名称_____________________。
(4)写出加入碳酸铵所发生的反应的离子方程式_____________;写出溶液2的一种用途_________。
(5)准确称取100 g工业碳酸钙粉末,通过上述方法理论上可以制得质量分数为99%的医药级二水合氯化钙的质量为____________。
-
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下:

生成氢氧化物沉淀的pH
| Mg(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 9.4 | 6.3 | 1.5 |
| 完全沉淀时 | 12.4 | 8.3 | 2.8 |
(1)MgCO3与稀硫酸反应的离子方程式为________。
(2)加氨水调节溶液的PH范围为________。
(3)滤渣2 的成分是________(填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C MgO+S↓+3CO↑
MgO+S↓+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集。
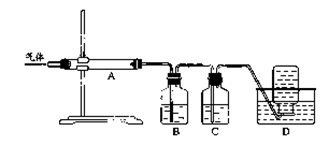
①D中收集的气体是________(填化学式)。
②B中盛放的溶液是________(填字母)。
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硫酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:________。
-
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下:

生成氢氧化物沉淀的pH:
| Mg(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 9.4 | 6.3 | 1.5 |
| 完全沉淀时 | 12.4 | 8.3 | 2.8 |
(1)MgCO3 与稀硫酸反应的离子方程式为_______________________。
(2)加双氧水的目的______________________;相关的离子方程式_________________________;加氨水调节溶液的PH范围为______________。
(3)滤渣2 的成分是_____________(填化学式)。
(4)煅烧过程存在以下反应:2MgSO4+C 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用下图装置对煅烧产生的气体进行分步吸收或收集。
①D中收集的气体可以是________________(填化学式)。
②B中盛放的溶液可以是________________(填字母)。
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式:__________________________。
-
工业以软锰矿(主要成分是 MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如下:
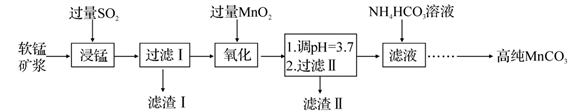
已知:25℃时,部分金属阳离子以氢氧化物形式沉淀时溶液的pH 如下表所示。
| 金属阳离子 | Fe3+ | Fe2+ | Mn2+ |
| 开始沉淀的pH | 2.7 | 7.6 | 8.3 |
| 完全沉淀的pH | 3.7 | 9.7 | 9.8 |
(1)“浸锰”过程中 Fe2O3与SO2反应的离子方程式为 Fe2O3+SO2+2H+ =2Fe2++SO42-+H2O,该反应是经历以下两步反应实现的。
写出ⅱ的离子方程式:_______________________。
ⅰ:Fe2O3+6H+ =2Fe3++3H2O ⅱ:……
(2)过滤Ⅰ所得滤液中主要存在的两种金属阳离子为_________ (填离子符号)。
(3)写出“氧化”过程中MnO2 与Fe 2+反应的离子方程式:___________。
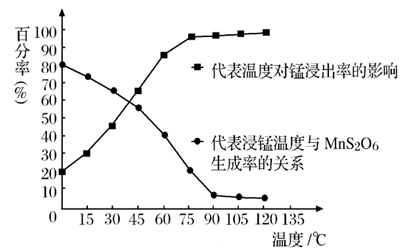
(4)“浸锰”反应中往往有副产物 MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是;_____滤渣Ⅱ的成分是______ (写化学式);向过滤Ⅱ所得的滤液中加入NH4HCO3 溶液时温度不宜太高的原因是______________。
(5)加入NH4HCO3溶液后,生成 MnCO3沉淀,同时还有气体生成,写出反应的离子方程式:__________________ 。
(6)生成的 MnCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是_______________。
-
过碳酸钠 是过氧化物类的消毒剂,可以利用候氏制碱法得到的
是过氧化物类的消毒剂,可以利用候氏制碱法得到的 ,进行制备,流程图如下:
,进行制备,流程图如下:
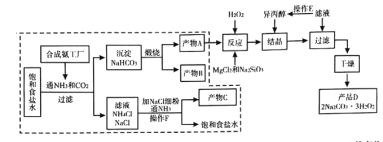
已知:①产物 中可能含有少量的
中可能含有少量的 、
、 金属离子杂质。②硅酸钠可与
金属离子杂质。②硅酸钠可与 、
、 等高价金属离子形成沉淀。
等高价金属离子形成沉淀。
请回答下列问题:
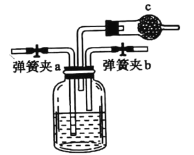
(1)虚线框中是侯氏制碱法的原理,某同学用右图装置在实验室模拟侯氏制碱法,实验中应先打开弹簧夹________(填 或
或 ),通入________气体。
),通入________气体。
(2)索尔维制碱法是利用石灰石分解制备 ,并用生成的
,并用生成的 和
和 反应制备氨气,将
反应制备氨气,将 和
和 通人饱和食盐水制备
通人饱和食盐水制备 晶体,分离提纯后分解制备纯碱。与索尔维制碱法相比,侯氏制碱法的优点是(至少写两点)________。
晶体,分离提纯后分解制备纯碱。与索尔维制碱法相比,侯氏制碱法的优点是(至少写两点)________。
(3)“反应”需控制温度在 左右,写出“反应”中生成产品
左右,写出“反应”中生成产品 的化学方程式________,加
的化学方程式________,加 的作用是________。
的作用是________。
(4)流程图中可循环使用的物质有________。
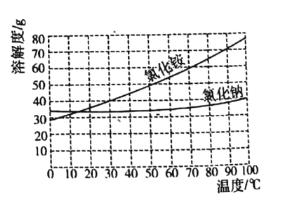
(5)操作 的主要步骤有________(已知
的主要步骤有________(已知 和
和 的溶解度曲线如图所示)
的溶解度曲线如图所示)
(6)为了测定产品 的纯度,某小组的方法是:取
的纯度,某小组的方法是:取 产品配成
产品配成 的溶液,取出
的溶液,取出 用
用 用硫酸酸化的
用硫酸酸化的 溶液滴定至终点,该滴定过程中消耗高锰酸钾标准溶液的体积为
溶液滴定至终点,该滴定过程中消耗高锰酸钾标准溶液的体积为 。产品的纯度为________%(用含有
。产品的纯度为________%(用含有 和
和 的式子表示)。
的式子表示)。
-
医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙(CaCl2·2H2O的质量分数为97.0%~103.0%)的主要流程如下:

(1)除杂操作时加入氢氧化钙固体,调节溶液的pH为8.0~8.5,以除去溶液中的少量Al3+、Fe3+,检验Fe(OH)3是否沉淀完全的实验操作是_____________________________;
(2)酸化操作是加入盐酸,调节溶液的pH约为4.0,其目的有:
①___________________________;②___________________________;
(3)测定样品中Cl-含量的方法是:
A.称取0.7500 g样品,溶解,在250 mL容量瓶中定容;B.量取25.00 mL待测溶液于锥形瓶中;C.用0.0500 mol·L-1 AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.00 mL。
①上述测定过程中不需要用盛装溶液润洗的仪器有 ,若润洗后会导致结果
②计算上述样品中CaCl2·2H2O的质量分数为________________;
③若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有: ; 。
(4)工业上冶炼金属钙的方法是 ;请写出此冶炼的化学反应方程式________________;


















