-
我国电池的年市场消费量约为80亿只,其中70%是锌锰干电池,利用废旧锌锰干电池制备硫酸锌晶体(ZnSO4·7H2O)和纯MnO2的工艺如下图所示:
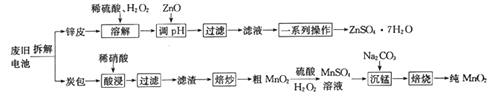
已知:
①锌皮的主要成分为Zn,含有少量Fe;炭包的主要成分为ZnCl2、NH4Cl、MnO2、碳粉等,还含有少量的 Cu、Ag、Fe 等。
②Ksp[Zn(OH)2]=2.0×10-16;Ksp[Fe(OH)2]=8.0×10-16;Ksp[Fe(OH)3]=4.0×10-38。
(1)除去炭包中碳粉的操作为_____________。
A.酸浸 B.过滤 C.焙炒 D.焙烧
(2)粗MnO2转化为MnSO4时,主要反应的离子方程式为_____________________。
(3)焙烧时发生反应的化学方程式为_____________。
(4)制备硫酸锌晶体流程中,用ZnO调节溶液pH的目的是______________________________,若溶解时不加H2O2带来的后果是____________________。
(5)“草酸钠-高锰酸钾返滴法”可测定MnO2的纯度:取agMnO2样品于锥形瓶中,加入适量稀硫酸,再加入V1mLc1mol·L-1Na2C2O4溶液(足量),最后用c2mol·L-1的KMnO4溶液滴定剩余的Na2C2O4,达终点时消耗V2 mL标准KMnO4溶液。
①MnO2参与反应的离子方程式为_____________。
②该样品中MnO2的质量分数为__________________(假定杂质不参与反应,列出表达式即可)。
-
我国电池的年市场消费量约为80亿只,其中70%是锌锰干电池,利用废旧锌锰干电池制备硫酸锌晶体(ZnSO4·7H2O)和纯MnO2的工艺如下图所示:
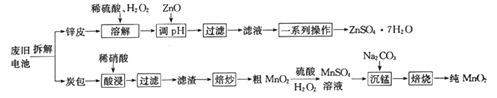
已知:
①锌皮的主要成分为Zn,含有少量Fe;炭包的主要成分为ZnCl2、NH4Cl、MnO2、碳粉等,还含有少量的 Cu、Ag、Fe 等。
②Ksp[Zn(OH)2]=2.0×10-16;Ksp[Fe(OH)2]=8.0×10-16;Ksp[Fe(OH)3]=4.0×10-38。
(1)除去炭包中碳粉的操作为_____________。
A.酸浸 B.过滤 C.焙炒 D.焙烧
(2)粗MnO2转化为MnSO4时,主要反应的离子方程式为_____________________。
(3)焙烧时发生反应的化学方程式为_____________。
(4)制备硫酸锌晶体流程中,用ZnO调节溶液pH的目的是______________________________,若溶解时不加H2O2带来的后果是____________________。
(5)“草酸钠-高锰酸钾返滴法”可测定MnO2的纯度:取agMnO2样品于锥形瓶中,加入适量稀硫酸,再加入V1mLc1mol·L-1Na2C2O4溶液(足量),最后用c2mol·L-1的KMnO4溶液滴定剩余的Na2C2O4,达终点时消耗V2 mL标准KMnO4溶液。
①MnO2参与反应的离子方程式为_____________。
②该样品中MnO2的质量分数为__________________(假定杂质不参与反应,列出表达式即可)。
-
我国电池的年市场消费量约为80亿只,其中70%是锌锰干电池,利用废旧锌锰干电池制备硫酸锌晶体(ZnSO4·7H2O)和纯MnO2的工艺如下图所示:
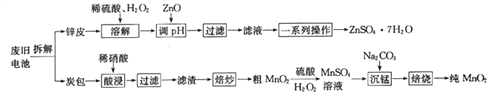
已知:
①锌皮的主要成分为Zn,含有少量Fe;炭包的主要成分为ZnCl2、NH4Cl、MnO2、碳粉等,还含有少量的 Cu、Ag、Fe 等。
②Ksp[Zn(OH)2]=2.0×10-16;Ksp[Fe(OH)2]=8.0×10-16;Ksp[Fe(OH)3]=4.0×10-38。
(1)除去炭包中碳粉的操作为_____________。
A.酸浸 B.过滤 C.焙炒 D.焙烧
(2)粗MnO2转化为MnSO4时,主要反应的离子方程式为_____________________。
(3)焙烧时发生反应的化学方程式为_____________。
(4)制备硫酸锌晶体流程中,用ZnO调节溶液pH的目的是______________________________,若溶解时不加H2O2带来的后果是____________________。
(5)“草酸钠-高锰酸钾返滴法”可测定MnO2的纯度:取agMnO2样品于锥形瓶中,加入适量稀硫酸,再加入V1mLc1mol·L-1Na2C2O4溶液(足量),最后用c2mol·L-1的KMnO4溶液滴定剩余的Na2C2O4,达终点时消耗V2 mL标准KMnO4溶液。
①MnO2参与反应的离子方程式为_____________。
②该样品中MnO2的质量分数为__________________(假定杂质不参与反应,列出表达式即可)。
-
我国电池的年市场消费量约为80亿只,其中 是锌锰干电池,利用废旧锌锰干电池制备硫酸锌晶体
是锌锰干电池,利用废旧锌锰干电池制备硫酸锌晶体 和纯
和纯 的工艺如下图所示:
的工艺如下图所示:

已知:
①锌皮的主要成分为Zn,含有少量Fe;炭包的主要成分为 、
、 、
、 、碳粉等,还含有少量的Cu、Ag、Fe等。
、碳粉等,还含有少量的Cu、Ag、Fe等。
② ;
; ;
; 。
。
(1)除去炭包中碳粉的操作为________。
A.酸浸  过滤
过滤  焙炒
焙炒  焙烧
焙烧
(2)粗 转化为
转化为 时,主要反应的离子方程式为____________________________。
时,主要反应的离子方程式为____________________________。
(3)焙烧时发生反应的化学方程式为__________________________________________。
(4)制备硫酸锌晶体流程中,在溶解时加 的作用是____________________________,用ZnO调节溶液pH的目的是_____________________________。滤液制备硫酸锌晶体
的作用是____________________________,用ZnO调节溶液pH的目的是_____________________________。滤液制备硫酸锌晶体 的一系列操作为:____________、____________、________、洗涤、干燥。
的一系列操作为:____________、____________、________、洗涤、干燥。
(5)“草酸钠 高锰酸钾返滴法”可测定
高锰酸钾返滴法”可测定 的纯度,取
的纯度,取 样品于锥形瓶中,加入适量稀硫酸,再加入足量的
样品于锥形瓶中,加入适量稀硫酸,再加入足量的 溶液,最后用
溶液,最后用 溶液滴定剩余的
溶液滴定剩余的 。其中
。其中 与
与 溶液反应的离子方程式为__________________________________________。
溶液反应的离子方程式为__________________________________________。
-
用Zn(主要含有Fe、Al、Pb杂质)和硫酸来制取H2,利用制氢废液制备硫酸锌晶体(ZnSO4·7H2O)、Al2O3和Fe2O3,流程如下:
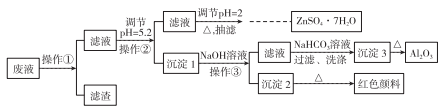
已知Al3+、Fe3+、Zn2+的氢氧化物完全沉淀的pH分别为5.2、4.1和8.5,ZnSO4·7H2O晶体易溶于水,易风化。回答下列问题:
(1)调节pH=2的目的是______________,调节pH=2,可加入_________(填化学式)。
(2)写出生成沉淀3的化学方程式:______________________。
(3)加热浓缩ZnSO4溶液出现极薄品膜时,要停止加热的主要原因是_____________。
(4)某同学用如图所示的装置抽滤。

①有关抽滤的说法正确的是__________。
A.抽滤的目的主要是得到较干燥的沉淀
B.滤纸的直径应略小于漏斗内径,又能盖住全部小孔
C.图中有一处出错
D.抽滤结束,从吸滤瓶的支管口倒出滤液
②抽滤,洗涤沉淀的具体操作是___________________________。
(5)为得到干燥的ZnSO4·7H2O产品,选择干燥方法是________。
A.加热烘干 B.用浓H2SO4干燥
C.用酒精洗干 D.在空气中白然干燥
-
用Zn(主要含有Fe、Al、Pb杂质)和硫酸来制取H2,利用制氢废液制备硫酸锌晶体(ZnSO4·7H2O)、Al2O3和Fe2O3,流程如下:
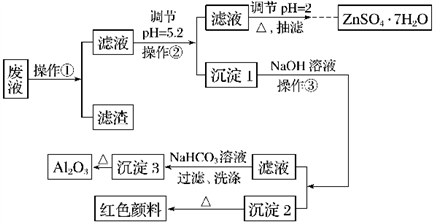
已知Al3+、Fe3+、Zn2+的氢氧化物完全沉淀的pH分别为5.2、4.1和8.5,ZnSO4·7H2O晶体易溶于水,易风化。回答下列问题:
(1)调节pH=2的目的是______________________,调节pH=2,可加入________________(填化学式)。
(2)写出生成沉淀3的化学方程式:_____________________________________。
(3)加热浓缩ZnSO4溶液出现极薄晶膜时,要停止加热的主要原因是_______________________________。
(4)
某同学用如图所示的装置抽滤。

①有关抽滤的说法正确的是________(填字母)。
A.抽滤的目的主要是得到较干燥的沉淀
B.滤纸的直径应略小于漏斗内径,又能盖住全部小孔
C.图中有一处出错
D.抽滤结束,从吸滤瓶的支管口倒出滤液
②抽滤,洗涤沉淀的具体操作是____________________________________________________。
(5)为得到干燥的ZnSO4·7H2O产品,选择干燥方法是________(填字母)。
A.加热烘干
B.用浓H2SO4干燥
C.用酒精洗干
D.在空气中自然干燥
-
某兴趣小组用废旧镀锌铁皮按下列流程制备七水硫酸锌(ZnSO4·7H2O)
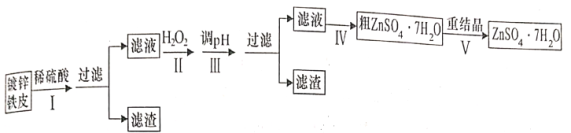
相关信息如下:
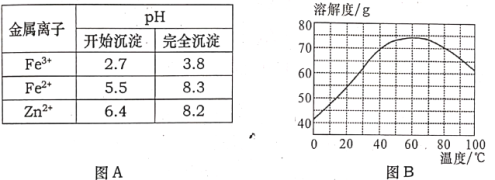
①金属离子形成氢氧化物沉淀的pH,如图A所示。
②ZnSO4的溶解度(物质在100g水中溶解的质量)随温度变化曲线如图B所示。
请回答:
(1)为提高镀锌铁皮中金属离子的浸出率,除了可适当增加硫酸的浓度,还可以采取的措施有:_______(任写一条)。
(2)步骤Ⅱ中需加入过量H2O2,请用离子方程式表示H2O2的作用________。
(3)步骤Ⅲ中调节pH范围为_______,调节pH宜选用的试剂为_______。
A.稀硫酸 B.氢氧化锌 C.氢氧化钠 D.氧化锌
(4)检验步骤Ⅲ所得滤液中是否含有Fe3+可采用的实验方法是_______。
(5)步骤Ⅳ需要用到下列所有操作:a.蒸发至溶液出现晶膜 b.在60℃蒸发溶剂 c.冷却至室温 d.在100℃蒸发溶剂 e.过滤
请给出上述操作的正确顺序______(操作可敢复使用)。
(6)步骤V中,某同学采用不同降温方式进行冷却结都,测得ZnSO4·7H2O颗粒大小分布如图所示。根据该实验结果,为了得到颗粒大小相对均的较大晶粒,宜选择______方式进行冷却结晶。
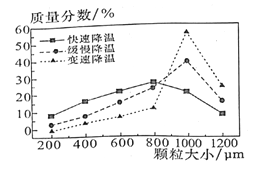
A.快速降温 B.级慢降温 C.变速降温
(7)ZnSO4可用于制备金属锌。用锌和高铁酸钾制成的高铁碱性电池,能储存比普通碱性电池多50%的电能,已知该电池的总反应是2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2。该电池正极反应式是________。
-
某兴趣小组用废旧镀锌铁皮按下列流程制备七水硫酸锌(ZnSO4·7H2O)

相关信息如下:
①金属离子形成氢氧化物沉淀的pH,如图A所示。
②ZnSO4的溶解度(物质在100g水中溶解的质量)随温度变化曲线如图B所示。

请回答:
(1)为提高镀锌铁皮中金属离子的浸出率,除了可适当增加硫酸的浓度,还可以采取的措施有:_______(任写一条)。
(2)步骤Ⅱ中需加入过量H2O2,请用离子方程式表示H2O2的作用________。
(3)步骤Ⅲ中调节pH范围为_______,调节pH宜选用的试剂为_______。
A.稀硫酸 B.氢氧化锌 C.氢氧化钠 D.氧化锌
(4)检验步骤Ⅲ所得滤液中是否含有Fe3+可采用的实验方法是_______。
(5)步骤Ⅳ需要用到下列所有操作:a.蒸发至溶液出现晶膜 b.在60℃蒸发溶剂 c.冷却至室温 d.在100℃蒸发溶剂 e.过滤
请给出上述操作的正确顺序______(操作可敢复使用)。
(6)步骤V中,某同学采用不同降温方式进行冷却结都,测得ZnSO4·7H2O颗粒大小分布如图所示。根据该实验结果,为了得到颗粒大小相对均的较大晶粒,宜选择______方式进行冷却结晶。

A.快速降温 B.级慢降温 C.变速降温
(7)ZnSO4可用于制备金属锌。用锌和高铁酸钾制成的高铁碱性电池,能储存比普通碱性电池多50%的电能,已知该电池的总反应是2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2。该电池正极反应式是________。
-
(16分)2006年世界锂离子电池总产量超过25亿只,锂电池消耗量巨大,对不可再生的金属资源的消耗是相当大的,回收利用锂资源成为重要课题。某研究小组对某废旧锂离子电池正极材料(图中简称废料,成份为LiMn2O4、石墨粉和铝箔)进行回收研究,工艺流程如下:
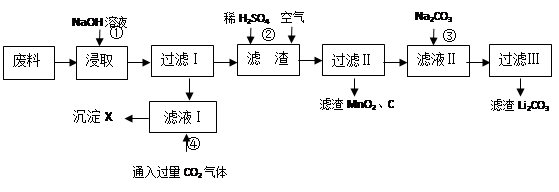
已知:Li2SO4、LiOH和Li2CO3在303K下的溶解度分别为34.2g、12.7g和1.3g。
(1)废料在用NaOH溶液浸取之前需要进行粉碎操作,其目的是________。
(2)废旧电池可能由于放电不完全而残留有锂单质,为了安全对拆解环境的要求________________________。
(3)写出反应④生成沉淀X的离子方程式:
________。
(4)己知LiMn2O4中Mn的化合价为+3和+4价,写出反应②的离子反应方程式:
________。
(5)生成Li2CO3的化学反应方程式为__ ______________。已知Li2CO3在水中的溶解度随着温度升高而减小,最后一步过滤时应__________。
-
2006年世界锂离子电池总产量超过25亿只,锂电池消耗量巨大,对不可再生的金属资源的消耗是相当大的,回收利用锂资源成为重要课题.某研究小组对某废旧锂离子电池正极材料(图中简称废料,成份为LiMn2O4、石墨粉和铝箔)进行回收研究,工艺流程如下:
已知:Li2SO4、LiOH和Li2CO3在303K下的溶解度分别为34.2g、12.7g和1.3g.
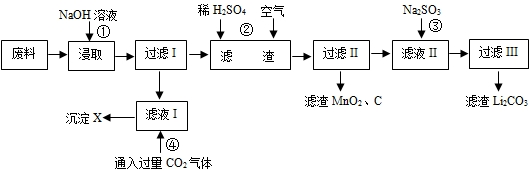
(1)废料在用NaOH溶液浸取之前需要进行粉碎操作,其目的是________.
(2)废旧电池可能由于放电不完全而残留有锂单质,为了安全对拆解环境的要求________.
(3)写出反应④生成沉淀X的离子方程式:________.
(4)己知LiMn2O4中Mn的化合价为+3和+4价,写出反应②的化学反应方程式:________.
(5)生成Li2CO3的化学反应方程式为________.已知Li2CO3在水中的溶解度随着温度升高而减小,最后一步过滤时应________.















