-
为测定已变质的过氧化钠的纯度,设计如下图所示的实验;Q为一具有良好的弹性气球,称取一定量的样品放于其中,按图安装的实验装置打开分液漏斗的活塞,将稀H2SO4滴入气球中.请填空:
(1)Q内发生反应生成______种气体,其中的反应有______个氧化还原反应.
(2)为测定反应生成气体的总体积,滴稀H2SO4前必须关闭(填K1、K2或K3,下同)______,打开______.
(3)当上述反应停止,将K1、K2、K3处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是______.
(4)导管a的作用是______.
(5)b中装的固体试剂是______,为何要缓缓打开K1______.
(6)实验结束时量筒I中有x mL水,量筒II中收集到y mL气体,则过氧化钠的纯度是______(体积折算到标准状况).

-
实验室测定已部分变质的过氧化钠样品纯度的装置如图所示(Q为弹性良好的气球不与药品反应,取定量的样品放入其中)。按图示安装好仪器,打开分液漏斗的活塞,将稀硫酸滴入气球中。下列说法中不正确的是
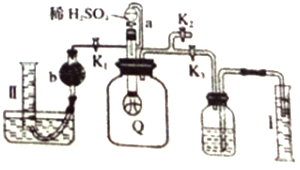
A. 稀硫酸滴入气球中,Q 中能生成两种气体
B. 准确读取量筒I读数后,先关闭K3然后打开K2,再缓缓打开K1,准确读取量筒II读数
C. I、II中测量的气体体积的差值即为CO2的体积(相同状况下)
D. b中的固体试剂可以是碱石灰,也可以是无水氯化钙。
-
通过测定混合气中 含量可计算已变质的
含量可计算已变质的 含
含 纯度,实验装置如图
纯度,实验装置如图 为弹性良好的气囊
为弹性良好的气囊 ,下列分析错误的是
,下列分析错误的是

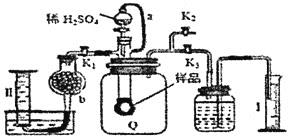
A.干燥管b中装入碱石灰
B.测定气体总体积必须关闭 、
、 ,打开
,打开
C.测定总体积后,关闭 ,打开
,打开 ,可观察到Q气球慢慢缩小,并测出氧气体积
,可观察到Q气球慢慢缩小,并测出氧气体积
D.Q气球中产生的气体主要成份 、
、
-
通过测定混合气中 含量可计算已变质的
含量可计算已变质的 含
含 纯度,实验装置如图
纯度,实验装置如图 为弹性良好的气囊
为弹性良好的气囊 ,下列分析错误的是
,下列分析错误的是

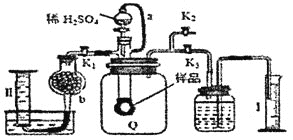
A.干燥管b中装入碱石灰
B.测定气体总体积必须关闭 、
、 ,打开
,打开
C.测定总体积后,关闭 ,打开
,打开 ,可观察到Q气球慢慢缩小,并测出氧气体积
,可观察到Q气球慢慢缩小,并测出氧气体积
D.Q气球中产生的气体主要成份 、
、
-
通过测定混合气中 含量可计算已变质的
含量可计算已变质的
 含
含 纯度,实验装置如图
纯度,实验装置如图 为弹性良好的气囊
为弹性良好的气囊 。下列分析错误的是
。下列分析错误的是

A.干燥管b中装入碱石灰
B.Q气球中产生的气体主要成份 、
、
C.测定气体总体积必须关闭 、
、 ,打开
,打开
D.读完气体总体积后,关闭 ,缓缓打开
,缓缓打开 ;可观察到Q气球慢慢缩小
;可观察到Q气球慢慢缩小
-
通过测定混合气中O2含量可计算已变质的Na2O2 (含Na2CO3) 纯度,实验装置如图(Q为弹性良好的气囊)。下列分析错误的是
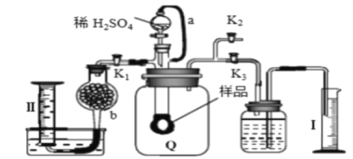
A. 干燥管b中装入碱石灰
B. Q气球中产生的气体主要成份O2、CO2
C. 测定气体总体积必须关闭K1、K2,打开K3
D. 读完气体总体积后,关闭K3,缓缓打开K1;可观察到Q气球慢慢缩小
-
实验室有一瓶久置的Na2SO3固体试剂,已部分变质,为测定其纯度,实验设计与操作如下,请回答问題:
(1)Na2SO3变质的原因(用化学方程式表示)___________。
(2)取一定量的样品溶于水,加入过量的BaCl2溶液,然后过滤(如图)、洗涤、干燥、称量,其中洗涤沉淀的具体操作为___________。
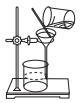
(3)实验时用BaCl2比用CaCl2好,写出两点理由:___________。
-
有一Na2SO3固体因部分被氧化而变质。为测定样品纯度,甲、乙两位同学分别设计了如下实验方案:
(甲同学)称取m g样品溶于水,加入过量的BaCl2溶液。过滤,向沉淀中加入过量盐酸,再过滤,将残留固体洗涤后进行烘干,冷却后称得质量为m1 g。
(1)BaCl2溶液必须过量的原因是___________________________________________。在滤液中滴加____________溶液,若没有白色沉淀生成,则证明BaCl2溶液不足,还需继续在滤液中加入BaCl2溶液后进行过滤。洗涤残留固体的方法是__________________________________________________;在洗出液中滴加_______________溶液,可以判断残留固体是否洗涤干净。
(2)判断残留固体质量m1 g能够作为实验测定值代入计算式,推算样品纯度,必须补充的实验操作是_________________________________________________________。
(乙同学)称取m g样品溶于水,配成溶液,用滴定管取V mL于锥形瓶中,用浓度为c mol/L的标准酸性高锰酸钾溶液滴定至终点。反应关系为:SO32- + MnO4- SO42- + Mn2+ (未配平)
(3)配制样品溶液时,不一定需要的实验仪器是__________(选填答案编号)。
a.容量瓶 b.玻璃棒 c.滴定管 d.烧杯
(4)滴定终点的判断依据是___________________________________________________。
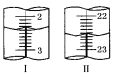
(5)上述滴定中,滴定管在注入酸性高锰酸钾溶液之前,先用蒸馏水洗净,再用__________________________________________。滴定管液面变化如图所示,从图Ⅰ图Ⅱ显示消耗的高锰酸钾溶液体积为__________________。
-
(10分)某学生为了测定部分变质的Na2SO3样品的纯度,设计了如下实验,回答下列问题:

(1)写出A装置中玻璃仪器的名称:酒精灯、______、 。
(2)实验开始后,写出B中反应的离子方程式_______________________。
(3)C中的现象是______________,E装置的作用是_____________________。
(4)某学生按下图所示称取一定量的Na2SO3样品放入A装置的烧瓶中,滴入足量的H2SO4完全反应。然后将B中完全反应后的溶液与足量的BaCl2溶液反应,过滤、洗涤、干燥,得白色沉淀23.3g。请你计算原样品中Na2SO3的纯度为________(精确到0.1%)。

(5)在过滤沉淀时若滤液出现浑浊,则必须要重复操作,若该学生没有重复过滤,则测定的结果将______(填“偏高”、“偏低”或“无影响”)。
(6)要使测定结果准确,第一:装置气密性必须良好;第二:应先点燃___处酒精灯(填装置字母)。
-
(10分)为测定某碳酸氢钠样品纯度(含有少量氯化钠),学生设计了如下几个实验方案(每个方案均称取m1g样品),请回答每个方案中的问题。
[方案Ⅰ] 选用重量法进行测定:可用下图中的装置进行实验。
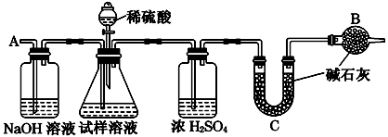
(1)A装置中NaOH溶液的作用是__________________若直接向试样溶液中鼓入空气会导致实验测定结果________(填“偏高”、“偏低”或“无影响”)。
(2)该方案需直接测定的物理量是______________________________________。
[方案Ⅱ] 选用气体体积法进行测定:可用如图中的装置进行实验,为了减小实验误差,量气管中加入饱和NaHCO3溶液。
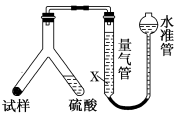
(3)通过实验,测得该试样中碳酸氢钠质量分数偏低,产生这种现象
的原因可能是________。
a.测定气体体积时未冷却至室温
b.测定气体体积时水准管的液面高于量气管的液面
c.Y型管中留有反应生成的气体
d.气体进入量气管前未用浓硫酸干燥
[方案Ⅲ] 选用滴定法进行测定:
(4)称取m1g样品,配成100 mL溶液,取出20 mL,用c mol·L-1的标准HCl溶液滴定,消耗体积为VmL,则该试样中碳酸氢钠质量分数的计算表达式为:_________________。











