-
侯德榜先生是我国化学工业的奠基人,他发明的“侯氏制碱法”结束了我国长期依赖外国进口纯碱的历史,在人类化学工业发展史上写下了光辉的一页。“侯氏制碱法”的基础原料是二氧化碳、氨气和饱和食盐水,反应的原理如下:Ⅰ. NaCl + H2O +NH3+ CO2=NaHCO3↓+X(由于该反应中生成的NaHCO3过多,而水又溶解不完,所以NaHCO3会首先以固体沉淀物的形式从水中结晶析出);Ⅱ. 2NaHCO3△Na2CO3+H2O+CO2↑
(1)实验室制CO2的化学方程式是_________________________。
(2)反应Ⅰ中的X是一种氮肥,X与熟石灰混合、研磨,能闻到有刺激性气味的气体产生,则X的化学式是___________。
(3)反应Ⅱ的基本反应类型是___________________________。
(4)“侯氏制碱法”的反应原理中可以循环利用的物质是_________________。
九年级化学填空题中等难度题查看答案及解析
-
侯德榜是我国化学工业的奠基人,纯碱工业的创始人。他发明的“侯氏制碱法”,缩短了生产流程,减少了对环境的污染,在人类化学工业史上写下了光辉的一页。侯氏制碱法的主要反应为:
NH3 + CO2 + H2O + NaCl = NaHCO3 + NH4Cl ,

他利用生成物中的NaHCO3溶解度较小,一经生成便会大量析出,能够很容易的分离出NaHCO3。
化学小组同学模拟“侯氏制碱法”完成以下实验:10℃时,向92.6g饱和NaCl溶液中先通入足量NH3共3.4g,再通入一定量CO2至恰好完全反应。请计算:(不考虑溶解在溶液中的NH3和CO2的质量)。
(1) NH4Cl可作为氮肥使用,其中氮元素的质量分数(只写出计算过程)___________。
(2) 以上反应中消耗CO2的质量是多少?
(3) 反应后称量溶液中析出NaHCO3晶体的质量为14.4g,则剩余溶液的质量是多少?
九年级化学计算题极难题查看答案及解析
-
(2011•崇安区二模)侯德榜先生是我国制碱工业的先驱和奠基人.他发明的“侯氏制碱法”提高了原料的利用率,在制得了纯碱的同时还获得了大量化肥.其主要过程如图所示:
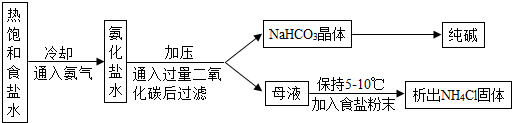
整个过程中涉及的主要反应有:
NH3+H2O+CO2═NH4HCO3
NH4HCO3+NaCl═NaHCO3+NH4Cl(晶体)
2NaHCO3Na2CO3+H2O+CO2↑
(1)“侯氏制碱法”生产的最终产品中可做化肥的是______.该化肥能否与熟石灰混合使用?______(填:“能”或“不能”);若不能,为什么?(用化学方程式表示)______(若能则此问不做).
(2)实验室中,纯碱也可以和熟石灰用来制取少量的烧碱,用化学方程式表示其过程:______.
(3)根据题目提供的信息,有的原材料可以循环使用,它们是______.
(4)碳酸钠和碳酸氢钠都是白色固体,从题目信息中可以找到一种鉴别它们的方法:_______.
(5)工业上制作印制板是利用氯化铁腐蚀Cu的原理:化学反应方程式为2FeCl3+Cu═2FeCl2+CuCl2.工业生产过程中产生的废液对环境有污染,为了节约金属资源并减少对环境的污染,请你设计一个实验流程处理废液回收Cu和FeCl2.
要求:参照上图的流程方式,将设计的实验流程在方框内完成.
查阅资料:Fe+2FeCl3═3FeCl2.九年级化学解答题中等难度题查看答案及解析
-
(6分)侯德榜先生是我国制碱工业的先驱和奠基人。他发明的“侯氏制碱法”提高了原料的利用率,在制得了纯碱的同时还获得了大量化肥。其主要过程如图所示:
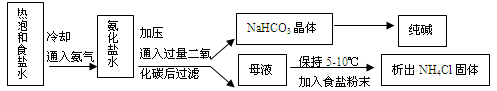
整个过程中涉及的主要反应有:
NH3+H2O+CO2=== NH4HCO3
NH4HCO3+NaCl===NaHCO3+NH4Cl(晶体)
2NaHCO3 △ Na2CO3+H2O+CO2↑
(1)“侯氏制碱法”生产的最终产品中可做化肥的是____________。该化肥能否与熟石灰混合使用?________(填:“能”或“不能”);若不能,为什么?(用化学方程式表示)
________(若能则此问不做)。
(2)根据题目提供的信息,有的原材料可以循环使用,它们是_____________________。
(3) 工业上制作印制板是利用氯化铁腐蚀Cu的原理:反应方程式为2FeCl3+Cu==2FeCl2+CuCl2。工业生产过程中产生的废液对环境有污染,为了节约金属资源并减少对环境的污染,请你设计一个实验流程处理废液回收Cu和FeCl2 。
要求:参照上图的流程方式,将设计的实验流程在方框内完成。
查阅资料:Fe+2FeCl3 ===3FeCl2
九年级化学填空题中等难度题查看答案及解析
-
侯德榜先生是我国制碱工业的先驱和奠基人.他发明的“侯氏制碱法”提高了原料的利用率,在制得了纯碱的同时还获得了大量化肥.其主要过程如图所示:
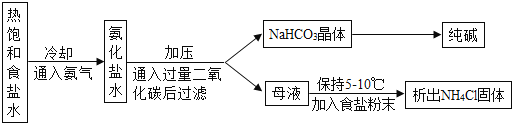
整个过程中涉及的主要反应有:
NH3+H2O+CO2=NH4HCO3
NH4HCO3+NaCl=NaHCO3+NH4Cl(晶体)
2NaHCO3
Na2CO3+H2O+CO2↑
(1)“侯氏制碱法”生产的最终产品中可做化肥的是____.该化肥能否与熟石灰混合使用?_____(填:“能”或“不能”);若不能,为什么?(用化学方程式表示)____(若能则此问不做).
(2)实验室中,纯碱也可以和熟石灰用来制取少量的烧碱,用化学方程式表示其过程:_____.
(3)根据题目提供的信息,有的原材料可以循环使用,它们是_____.
(4)碳酸钠和碳酸氢钠都是白色固体,从题目信息中可以找到一种鉴别它们的方法:_____.
(5)工业上制作印制板是利用氯化铁腐蚀
的原理:化学反应方程式为2FeCl3+Cu=2FeCl2+CuCl2.工业生产过程中产生的废液对环境有污染,为了节约金属资源并减少对环境的污染,请你设计一个实验流程处理废液回收Cu和FeCl2._________.
要求:参照如图的流程方式,将设计的实验流程在方框内完成.
查阅资料:Fe+2FeCl3=3FeCl2.
九年级化学流程题简单题查看答案及解析
-
侯德榜先生是我国制碱工业的先驱和奠基人.他发明的“侯氏制碱法”提高了原料的利用率,在制得了纯碱的同时还获得了大量化肥.其主要过程如图所示:

整个过程中涉及的主要反应有:
NH3+H2O+CO2═NH4HCO3
NH4HCO3+NaCl═NaHCO3+NH4Cl(晶体)
2NaHCO3Na2CO3+H2O+CO2↑
(1)“侯氏制碱法”生产的最终产品中可做化肥的是______.该化肥能否与熟石灰混合使用?______(填:“能”或“不能”);若不能,为什么?(用化学方程式表示)______(若能则此问不做).
(2)实验室中,纯碱也可以和熟石灰用来制取少量的烧碱,用化学方程式表示其过程:______.
(3)根据题目提供的信息,有的原材料可以循环使用,它们是______.
(4)碳酸钠和碳酸氢钠都是白色固体,从题目信息中可以找到一种鉴别它们的方法:_______.
(5)工业上制作印制板是利用氯化铁腐蚀Cu的原理:化学反应方程式为2FeCl3+Cu═2FeCl2+CuCl2.工业生产过程中产生的废液对环境有污染,为了节约金属资源并减少对环境的污染,请你设计一个实验流程处理废液回收Cu和FeCl2.
要求:参照上图的流程方式,将设计的实验流程在方框内完成.
查阅资料:Fe+2FeCl3═3FeCl2.九年级化学解答题中等难度题查看答案及解析
-
侯德榜先生是我国制碱工业的先驱和奠基人,其生产的产品纯碱和副产品氯化铵工艺流程如图所示:
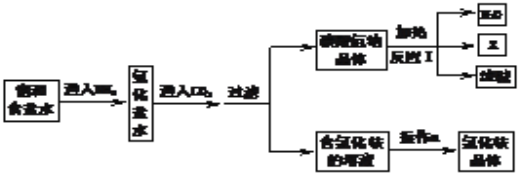
(1)NH3溶于水得到氨水。将无色酚酞溶液滴入氨水中,溶液呈______色。
(2)写出反应Ⅰ的化学方程式____________________________。
(3)上述工艺流程中可循环利用的物质是__________(水除外)。
(4)氯化氨在农业上可作氮肥,但不能与熟石灰混合施用。原因是_________(用化学方程式表示)。
(5)写出氨碱法生产碳酸氢钠的反应原理:_____________________________________。
九年级化学流程题中等难度题查看答案及解析
-
我国著名化学家侯德榜先生发明的侯氏制碱法,因原料利用率高,并能进行连续生产,从而享誉中外。某课外兴趣小组同学,按照“侯氏制碱法”原理,设计了如下图所示一套实验装置。
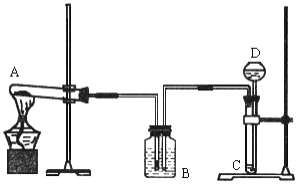
实验室可供选用的药品有:浓氨水、纯碱、大理石、稀盐酸、稀硫酸、熟石灰、氯化
铵、氯化钠。
(1)A、D 中最合适的试剂为:A_______,D_______(填名称)。
(2)本实验在具体操作过程中,应先通______气体,再通______气体,原因是_______。
(3)小红同学认为实验装置中存在某些不足,请指出其中的一处错误_________。
(4)在改进装置后,小丽同学进行了实验,实验所用的饱和氯化钠溶液中含溶质 58.5g,实验最后得到无水碳酸钠 26.0g,针对实验结果,该同学认真分析了造成损失的原因,发现其操作步骤并没有错误,则主要原因是___________。
九年级化学实验题中等难度题查看答案及解析
-
(2011•乐山)利用井盐和合成氨生产的氨气及二氧化碳生产纯碱的“联合制碱法”是由我国著名化学家侯德傍先生发明的,其氯化钠的利用率高达96%.其原理流程如右图所示:
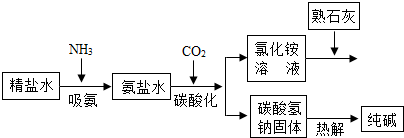
(1)氨极易溶于水,向饱和食盐水通入氨气可得到饱和食盐水和氨水的混合盐水(称为氨盐水).氨盐水比食盐水更容易吸收二氧化碳,其原因是;
(2)写出氯化铵溶液与熟石灰反应的化学方程式.九年级化学填空题中等难度题查看答案及解析
-
(2分)利用井盐和合成氨生产的氨气及二氧化碳生产纯碱的“联合制碱法”是由我国著名化学家侯德傍先生发明的,其氯化钠的利用率高达96%。其原理流程如下图所示:
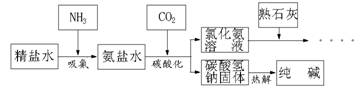
(1)氨极易溶于水,向饱和食盐水通入氨气可得到饱和食盐水和氨水的混合盐水(称为氨盐水)。氨盐水比食盐水更容易吸收二氧化碳,其原因是;
(2)写出氯化铵溶液与熟石灰反应的化学方程式 ________。
九年级化学信息分析题中等难度题查看答案及解析