-
NaNO2是一种食品添加剂,它与酸性KMnO4溶液可发生反应:MnO4-+NO2-+X→Mn2++NO3-+H2O(未配平)。下列叙述中正确的是
A. 生成1mo1NaNO3需消耗0.4mo1KMnO4
B. 反应过程中溶液的pH减小
C. 该反应中NO2﹣被还原
D. X可以是盐酸
高二化学单选题困难题查看答案及解析
-
NaNO2是一种食品添加剂,它能致癌.酸性KMnO4溶液与NaNO2的反应方程式是:MnO4-+NO2-+H+→Mn2++NO3-+H2O(未配平)。下列叙述中正确的是( )
A.该反应中NO2-是还原剂
B.反应过程中溶液的pH减小
C.生成1mol NaNO3时消耗0.4mol KMnO4
D该反应可说明氧化性MnO4-<NO3-
高二化学选择题困难题查看答案及解析
-
NaNO2是一种食品添加剂,它能致癌。酸性高锰酸钾溶液与亚硝酸钠的反应方程式是:MnO4- + NO2- +( )→Mn2+ + NO3- + H2O。下列叙述中正确的是
A. 该反应中NO2-被还原
B. 反应过程中溶液的pH变小
C. 生成1molNaNO3需要消耗0.4molKMnO4
D. ( )中的粒子是OH-
高二化学单选题中等难度题查看答案及解析
-
亚硝酸钠(NaNO2)是重要的防腐剂。某化学兴趣小组尝试制备亚硝酸钠,查阅资料:①HNO2为弱酸,在酸性溶液中,NO2-可将MnO4-还原为Mn2+且无气体生成。
②NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸
探究一 亚硝酸钠固体的制备
以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠。(反应方程式为2NO+Na2O2=2NaNO2,部分夹持装置和A中加热装置已略)
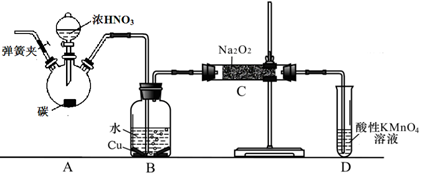
(1)写出装置A烧瓶中发生反应的化学方程式________。
(2)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为排除干扰应在B、C装置间增加装置E,E中盛放的试剂应是________(填字母)。
A.浓H2SO4 B.碱石灰 C.无水CaCl2
探究二 亚硝酸钠固体含量的测定及性质验证
称取装置C中反应后的固体4.000g溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000
mol/L酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
滴定次数
1
2
3
4
KMnO4溶液体积/mL
20.60
20.02
20.00
19.98
(3)第一组实验数据出现异常,造成这种异常的原因可能是________(填字母)。
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定终了仰视读数
(4)根据表中数据,计算所得固体中亚硝酸钠的质量分数。
(5)亚硝酸钠易溶于水,将0.2mol·L-1的亚硝酸钠溶液和0.1mol·L-1的盐酸等体积混合,混合后溶液呈酸性,则混合后溶液中离子浓度由大到小的顺序为________。
探究三 反应废液的处理
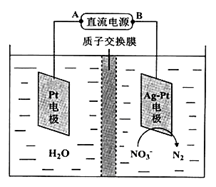
反应后烧瓶A中仍然存在一定量的硝酸,不能直接排放,用NaOH溶液调成中性,再用电化学降解法进行处理。25℃时,反应进行10min,溶液的pH由7变为12。电化学降解NO3-的原理如右图所示。
(6)电源正极为________(填A或B),阴极反应式为________。
高二化学实验题极难题查看答案及解析
-
(10分)草酸与高锰酸钾在酸性条件下能够发生如下反应:
MnO4- + H2C2O4 + H+ — Mn2+ + CO2↑+ H2O(未配平)
现用4 mL 0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
组别
10%硫酸体积/mL
温度/℃
其他物质
I
2 mL
20
II
2 mL
20
10滴饱和MnSO4溶液
III
2 mL
30
IV
1 mL
20
1 mL蒸馏水
(1)该反应中氧化剂和还原剂的物质的量之比为 。
(2)如果研究催化剂对化学反应速率的影响,使用实验 和 (用I~IV表示,下同);如果研究温度对化学反应速率的影响,使用实验 和 。
(3)对比实验I和IV,可以研究________对化学反应速率的影响,实验IV中加入1 mL蒸馏水的目的是 。
高二化学实验题中等难度题查看答案及解析
-
草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4-+H 2C2O4+H+--Mn2++CO2↑+H2O(未配平) 用4mL 0.001mol/L KMnO4溶液与2mL 0.01mol/L H 2C2O4溶液,研究不同条件对化学反应速率的影响.改变的条件如下:
(1)如果研究催化剂对化学反应速率的影响,使用实验________ 和________(用Ⅰ~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,使用实验________和________.组别 10%硫酸体积/mL 温度/℃ 其他物质 Ⅰ 2mL 20 Ⅱ 2mL 20 10滴饱和MnSO4溶液 Ⅲ 2mL 30 Ⅳ 1mL 20 1mL蒸馏水
(2)对比实验Ⅰ和Ⅳ,可以研究________对化学反应速率的影响,实验Ⅳ中加入1mL蒸馏水的目的是________.高二化学填空题中等难度题查看答案及解析
-
草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4—+H2C2O4+H+→Mn2++CO2↑+H2O(未配平)。用4 mL 0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
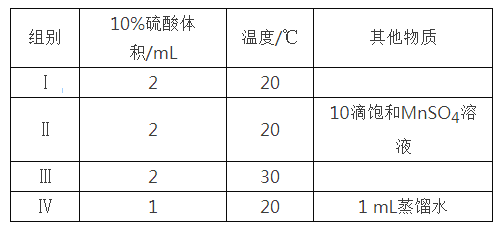
(1)写出该反应的离子方程式______________________,该反应中每生成1molCO2 转移电子数为________ 。
(2)如果研究催化剂对化学反应速率的影响,使用实验_______和________(用I~IV表示,下同);如果研究温度对化学反应速率的影响,使用实验________和_________。
(3)对比实验I和IV,可以研究________对化学反应速率的影响,实验IV中加入1 mL蒸馏水的目的是______________________。高二化学实验题中等难度题查看答案及解析
-
配平下列反应方程式:
(1)酸性KMnO4溶液能合H2C2O4(草酸)溶液褪色,反应离子方程式为:
____MnO4-+___H2C2O4+___H+=___Mn2++___CO2↑+___H2O
(2)淀粉碘化钾溶液在酸性环境中过一段时间后会褪色,反应离子方程式为:
___I-+___O2+___H+═___I2+___H2O
高二化学填空题中等难度题查看答案及解析
-
亚硝酸钠(NaNO2)是肉制品生产中最常使用的一种食品添加剂,某化学兴趣小组利用一氧化氮与过氧化钠反应制备亚硝酸钠并进行一系列实验探究。
查阅资料:
①NO2能与Na2O2反应;
②在酸性溶液中,NO2-可将MnO4-还原为Mn2+且无气体生成。
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸。
Ⅰ.制备亚硝酸钠
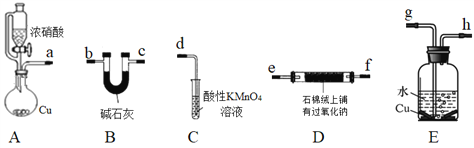
(1)装置A用恒压滴液漏斗,相比普通分液漏斗,显著的优点是____________________________。
(2)上述装置按气流方向连接的顺序为:a→____________________(填仪器接口的字母编号)。
(3)D中反应的方程式为_____________________________。如果没有B装置,D中生成的亚硝酸钠中含有的杂质有______________(填化学式)。
(4)C装置的作用是_________________(用离子方程式表示)。
Ⅱ.测定产品纯度,实验步骤:
①准确称量4.000 g产品配成250 mL溶液。
②从步骤①配制的溶液中移取25.00 mL加入锥形瓶中。
③用0.1000 mol/L酸性KMnO4溶液滴定至终点。
④重复以上操作3次,消耗酸性KMnO4溶液的平均体积为20.00 mL。
(5)达到滴定终点的现象是____________。产品中NaNO2的纯度为______________%。
(6)设计实验证明HNO2的酸性比CH3COOH强_________。
高二化学实验题中等难度题查看答案及解析
-
在稀硫酸中,KMnO4和H2O2能发生氧化还原反应。
氧化反应:H2O2-2e-===2H++O2↑
还原反应:MnO4-+5e-+8H+===Mn2++4H2O
(1)写出该氧化还原反应的离子方程式:_______________________。
(2)反应中氧化剂是________;被氧化元素是__________;若有0.5 mol H2O2参加此反应,电子转移个数为____________。
(3)若KMnO4的量不足,在Mn2+的催化作用下,H2O2仍能分解,分解反应的化学方程式为________________________;这时若有0.5 mol H2O2发生分解,电子转移个数为__________________。
高二化学填空题简单题查看答案及解析