-
在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)(已知:2SO2+O2 2SO3),反应过程中的能量关系可用如图简单表示(图中的△H 表示生成1mol产物的数据). 下列说法正确的是( )
2SO3),反应过程中的能量关系可用如图简单表示(图中的△H 表示生成1mol产物的数据). 下列说法正确的是( )
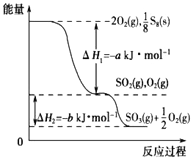
A. S8的燃烧热△H=﹣a kJ·mol﹣1
B. 1 mol SO2和过量 O2反应可释放出 b kJ 的热量
C. 已知1个S8分子中有8个S﹣S,S=O的键能为d kJ·mol﹣1,O=O的键能为e kJ·mol﹣1,则S8分子中S﹣S的键能为(2d﹣a﹣e) kJ·mol﹣1
D. 若使用V2O5作催化剂,当SO2(g)转化生成1mol SO3(g)时,释放的热量小于b kJ
-
在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)(已知:2SO2+O2 2SO3),反应过程中的能量关系可用右图简单表示(图中的ΔH 表示生成1 mol产物的数据)。 下列说法正确的是( )
2SO3),反应过程中的能量关系可用右图简单表示(图中的ΔH 表示生成1 mol产物的数据)。 下列说法正确的是( )

A.S8的燃烧热 ΔH=-a kJ·mol-1
B.1 mol SO2和过量 O2反应可释放出 b kJ 的热量
C.已知1个S8分子中有8个S-S,S=O的键能为d kJ·mol-1,O=O的键能为e kJ·mol-1,则S8分子中S-S的键能为(2d-a-e) kJ·mol-1
D.若使用V2O5作催化剂,当SO2(g)转化生成1mol SO3(g)时,释放的热量小于b kJ
-
有关2SO2+O2 2SO3的说法中,不正确的是
2SO3的说法中,不正确的是
A.该反应为可逆反应,故在一定条件下SO2和O2不可能全部转化为SO3
B.达到平衡后,反应就停止了,故正、逆反应速率相等且均为零
C.一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻之后,正、逆反应速率相等
D.平衡时SO2、O2、SO3的分子数之比不再改变
-
一定条件下的可逆反应2SO2+O2 2SO3,下列判断能说明达到化学反应的限度的是
2SO3,下列判断能说明达到化学反应的限度的是
A.SO2完全转化为SO3
B.SO2、O2与SO3的物质的量之比为2∶1∶2
C.反应混合物中,SO3的质量分数不再改变
D.消耗2 mol SO2的同时生成2 mol SO3
-
在密闭容器中发生反应2SO2+O2 2SO3(g),起始时SO2和O2分别为20mol和10mol,达到平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的条件下,欲使平衡时各成分的体积分数与前者相同,则起始时SO3的物质的量及SO3的转化率分别为( )
2SO3(g),起始时SO2和O2分别为20mol和10mol,达到平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的条件下,欲使平衡时各成分的体积分数与前者相同,则起始时SO3的物质的量及SO3的转化率分别为( )
A.10mol和10% B.20mol和20%
C.20mol和40% D.30mol和80%
-
已知单质硫在通常条件下以S8(斜方硫)的形式存在,其结构如图所示。
S8: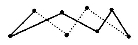 (冠状)
(冠状)
在一定条件下,S8(s)和O2(g)发生反应依次转化为SO2(g)和SO3(g)。能量和反应过程的关系可用下图简单表示(图中的ΔH表示生成1 mol产物的数据)。
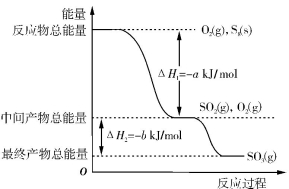
试根据上图回答下列问题:
(1)写出表示S8(s)的燃烧热的热化学方程式____________。
(2)写出SO3分解生成SO2和O2的热化学方程式____________。
(3)若已知S—O的键能为d kJ/mol,O O的键能为e kJ/mol,则S8分子中S—S键的键能为__________。
O的键能为e kJ/mol,则S8分子中S—S键的键能为__________。
-
某密闭容器中充入一定量SO2、O2,发生反应2SO2+O2 2SO3,测得SO3浓度与反应
2SO3,测得SO3浓度与反应 温度的关系如图所示。下列说法正确的是 ( )
温度的关系如图所示。下列说法正确的是 ( )
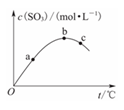
A.该反应ΔH>0 B.SO2转化率:a>b>c
C.化学反应速率:c>b>a D.平衡常数K:b>c>a
-
工业制备硫酸过程中存在如下反应:2SO2+O2 2SO3,该反应为放热反应。下列关于该反应的说法正确的是( )
2SO3,该反应为放热反应。下列关于该反应的说法正确的是( )
A.一定条件下SO2能完全转化为SO3
B.反应物的总能量小于生成物的总能量
C.使用催化剂不能加快反应速率
D.增大O2的浓度能加快反应速率
-
对于在一定条件下进行的可逆反应:2SO2+O2 2SO3,改变下列条件,可以提高反应物中活化分子百分数,但不改变SO2的转化率的是( )
2SO3,改变下列条件,可以提高反应物中活化分子百分数,但不改变SO2的转化率的是( )
A.升高温度 B.增大压强
C.使用催化剂 D.增大反应物浓度
-
在一定温度下,将4.0 mol SO2与2.0 mol O2的混合气体充入容积为2.0 L的密闭容器中发生反应:2SO2 + O2 2SO3,经过2.0 min达到平衡状态,SO2的平衡转化率为90.0%。
2SO3,经过2.0 min达到平衡状态,SO2的平衡转化率为90.0%。
(1)0~2 min内O2的平均反应速率v(O2)=_______________。
(2)该温度下此反应的化学平衡常数K=________________。
(3)在相同的温度下,某容器内c(SO2)=c(O2)=c(SO3)=1.0 mol•L-1,则此时反应速率v正________v逆(填“>”、“<”或“=”)。
2SO3),反应过程中的能量关系可用如图简单表示(图中的△H 表示生成1mol产物的数据). 下列说法正确的是( )


 (冠状)
(冠状)
