-
在元素周期表的前四周期元素A、B、C、D、E五种元素,其原子序数依次增大,B的p轨道上有两个未成对电子,A原子的第一电离能比B大,C原子的核外电子总数是最外层电子数的3倍D 、E原子的最外层电子数均为1,D的单质是常见的活泼金属, E的次外层电子为全充满结构。
(1)A、B、C三种元素的电负性由大到小的顺序是_________________(填元素符号),E原子的核外电子排布式是________________,第一电离能A>B,原因是________________________________。
(2) A与氢原子形成的18e-分子M的电子式是__________________________,M中A原子的杂化形式是________________________________。
(3)C可形成多种含氧酸,其最高价含氧酸Q的酸根的空间构型是_____________________,另一种含氧酸R的相对分子量比Q小32,且0.01molR可消耗1mol/LNaOH溶液10mL,则含氧酸R的结构式是_______________________ 。(已知:含氧酸中只有羟基上的氢原子可电离与碱反应)
(4)E与O2、NH3可在水溶液中发生反应生成[E(NH3)2]+,该离子在水溶液中呈无色,该离子中E的
化合价为___________,若向该离子中继续通入O2,可生成[E( NH3)4]2+,溶液变为深蓝色,请写出该反应的离子方程式____________________________。
(5)碳原子可形成多种同素异形体,C60便是其中之一,D单质可与C60分子在一定条件下发生化合反应生成一种离子化合物,其阴离子是C60-,该化合物的晶胞结构为NaC1型,则每个晶胞中含有的D+的数目是________个,已知:晶胞中最近的D+之间的距离为a pm,则该物质的密度ρ=___________g/cm3
(只需写出表达式即可)
高三化学简答题中等难度题查看答案及解析
-
有A、E、R、X、Y、Z六种前四周期元素,原子序数依次增大,基态A原子的2p轨道处半充满状态,原子的第一电离能E﹤A, R是地壳中含量最高的金属元素,X原子核外的M层中有三对成对电子,Y为周期表前四周期中电负性最小的元素, Z原子核外电子数为24。
请回答下列问题:
(1)基态Z原子的核外电子排布式是________。AE2+与二氧化碳分子互为等电子体,AE2+的电子式是____。AX3 分子的VSEPR模型是________。
(2)某化合物由E、Y两种元素组成,其晶胞如图,该化合物的化学式为______。
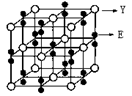
(3)在化合物Y2ZE4的水溶液入适量硫酸,能观察到的现象是________。
(4)A的简单氢化物极易溶于E的简单氢化物,其原因是________ 。
(5)A的最高价氧化物对应水化物的稀溶液与R的单质反应时,A被还原到最低价,该反应的化学方程式是________。
高三化学选择题困难题查看答案及解析
-
A、B、C、D、E为前四周期元素,原子序数依次增大。基态A原子的核外电子占据4个原子轨道;B与C同主族,大气平流层中单质B3浓度减少会致人患皮肤癌增加;D是前四周期元素中第一电离能最小的元素;E的合金是当今用量最大的合金。
(1)E2+的核外电子排布式为________。
(2)CB32-的立体构型是(用文字描述) ;其中心原子的杂化轨道类型为________。
(3)根据等电子原理,AB分子的电子式为________;其中σ键与π键之比为________。
(4)[E(H2O)6]3+内E3+与H2O间的作用力为________。
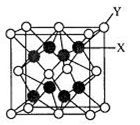
(5)D2C的晶胞结构与CaF2晶胞(如图)相似,则Y应为________(填离子符号);D2C的熔点比CaF2熔点________(填“高”、“低”或“无法比较”)。
高三化学推断题中等难度题查看答案及解析
-
A、B、C、D、E为前四周期元素,原子序数依次增大。基态A原子的核外电子占据4个原子轨道;B与C同主族,大气平流层中单质B3浓度减少会致人患皮肤癌增加;D是前四周期元素中第一电离能最小的元素;E的合金是当今用量最大的合金。
(1)E2+的核外电子排布式为 。
(2)CB32-型是(用文字描述) ;其中心原子的杂化轨道类型为 。
(3)根据等电子原理,AB分子的电子式为 ;其中σ键与π键之比为 。
(4)[E(H2O)6]3+内E3+与H2O间的作用力为 。
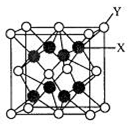
(5)D2C的晶胞结构与CaF2晶胞(如图)相似,则Y应为 (填离子符号);D2C的熔点比CaF2熔点 (填“高”、“低”或“无法比较”)。
高三化学填空题困难题查看答案及解析
-
A、B、C、D、E五种元素都是36号以前元素,原子序数依次增大,其相关信息如下表
(1)写出下列元素的符号:A______B______C______D______,E______;元素 相关信息 A A的第一电离能低于同周期相邻元素 B B原子中成对电子数等于未成对电子数的2倍 C C原子p轨道和s轨道中的电子数相等,与非金属的原子结合时形成共价键 D D与A、B、C均不同周期,其单质分子中只有一条共价键 E E在所处周期中电负性最大,且与D是同一主族元素
(2)A与D形成的化合物的化学式为______,其分子的立体构型是______,是______(填“极性”或“非极性”)分子;
(3)请比较化合物ED与Cl2、Br2、I2三者沸点由高到低的顺序:______>______>______>______,
其理由是______.
(4)A的最高价氧化物的水化物(H2AO3)晶体是一种白色片层状结构,层内的H3AO3分子这间有序排列如图.
①在H3AO3分子中,A原子的杂化方式是______;
②在晶体中,H3AO3分子能形成这种排列方式的原因是______;
③在H3AO3晶体中层与层之间的作用力是______,该晶体属于______晶体.
高三化学解答题中等难度题查看答案及解析
-
(12 分) X、Y、Z、W、Q五种元素其核电荷数依次增大。X原子只有1个s电子,Y、Z、W属于同周期,Y原子L层中s电子和p电子数目相同,Z原子p轨道为半充满,W原子第一电离能比Z原子的小,Q原子内层均饱和,N层上只有两个电子。
(1)Q2+离子的核外电子排布式为 。
(2)XYZ分子中Y原子轨道的杂化类型为 ,
1molXYZ分子中含有σ键的数目为 。
(3)写出YZW-离子的两种等电子体的化学式: 。
(4)QW的熔点比Q的硫化物的熔点高,其原因是
。
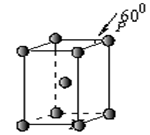
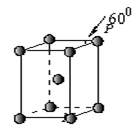
(5)Q晶体属于六方堆积,其晶胞结构见下图,则P点原子
被 个晶胞所共用。
高三化学填空题中等难度题查看答案及解析
-
(12 分)X、Y、Z、W、Q五种元素其核电荷数依次增大。X原子只有1个s电子,Y、Z、W属于同周期,Y原子L层中s电子和p电子数目相同,Z原子p轨道为半充满,W原子第一电离能比Z原子的小,Q原子内层均饱和,N层上只有两个电子。
(1)Q2+离子的核外电子排布式为 。
(2)XYZ分子中Y原子轨道的杂化类型为 ,1molXYZ分子中含有σ键的数目为 。
(3)写出YZW-离子的两种等电子体的化学式: 。
(4)QW的熔点比Q的硫化物的熔点高,其原因是 。
(5)Q晶体属于六方堆积,其晶胞结构见图14,则P点原子被 个晶胞所共用。
高三化学填空题中等难度题查看答案及解析
-
已知
、
、
、
、
都是元素周期表中前四周期的元素,它们的核电荷数依次增大。其中
与
、
与
在周期表中相邻,
原子核外有两个未成对电子,
的第一电离能比同周期相邻两种元素的都大,
原子在同周期元素原子中半径最大(稀有气体原子除外);
与
位于不同周期,
原子核外最外层电子数与
相同,其余各电子层均充满电子。请根据以上信息,回答下列问题。
(1)
、
、
、
四种元素的电负性由大到小的排列顺序为_________。
(2)
的氢化物的结构式为_________,其分子的空间构型为________。
(3)
的某种化合物的结构如图所示,已知微粒间的相互作用包括化学键和分子间作用力,则此化合物中各种粒子间的相互作用力有___________。

(4)
与
的气态氢化物相比,_________(填化学式,下同)的沸点更高;
与
的气态氢化物相比,________的沸点更高。
(5)
的稳定氧化物中,中心原子采取________杂化,该氧化物分子的空间构型为______。
高三化学综合题困难题查看答案及解析
-
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A与B同周期、A与D同族,A原子核外有两个未成对电子,B元素的第一电离能比同周期相邻两种元素都大,C原子在同周期原子中半径最大(稀有气体除外);E与C位于不同周期,E原子核外最外层电子数与C相同,其余各层电子均充满。请根据以上信息回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
(1)E原子核外电子排布式是 。
(2)B的最高价含氧酸根的空间构型为 。
(3)A、B、D三种元素电负性由大到小排列顺序为 。
(4)D单质比化合物DA的熔点 (填“高”或“低”),理由是 。
(5)已知A、C和地壳中含量最多的元素按1∶1∶2的原子个数比可形成某离子化合物,该化合物能使酸性高锰酸钾溶液褪色,写出发生反应的离子方程式 。
高三化学填空题困难题查看答案及解析
-
周期表中前四周期的元素A、Z、Q、R、T的原子序数依次增大,且A、Z、Q同周期。A共有两个原子轨道上有电子,且电子数目相同。Z、Q相邻,且Z中的未成对电子数为3个,R元素在地壳中含量位于金属元素的第二位。T是人类最早使用的元素,并以这种元素命名了我国的一个时代。请回答下面的问题:
(1)A、Z、Q第一电离能从小到大的顺序为:_______________(填元素符号),T的价层电子排布图为:__________________________。
(2)Q的基态原子中能量最高的电子,其电子云在空间有___________个方向,原子轨道呈_______形。
(3)Z3-的立体构型为____________,写出与Z3-互为等电子体的一种非极性分子化学式____________。
(4)在不同的温度下,A以ACl2和二聚体A2Cl4两种形式存在,二聚体的结构式如图所示:
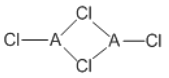
①ACl2中A的杂化方式为______________________。
②1mol A2Cl4中含配位键的数目为____________。
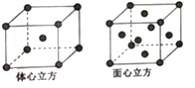
(5)R单质的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。体心立方晶胞和面心立方晶胞的棱边长分别为acm、bcm,则R单质的体心立方晶胞和面心立方晶胞的密度之比为_________,R原子配位数之比为_____________。
高三化学综合题中等难度题查看答案及解析