在密闭容器中,对于反应:2SO2(g)+O2(g) 2SO3(g),SO2和O2起始时分别为20 mol和10 mol;达平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为( )
A.10 mol和10% B.20 mol和20% C.20 mol和40% D.20 mol和80%
高一化学选择题简单题
在密闭容器中,对于反应:2SO2(g)+O2(g) 2SO3(g),SO2和O2起始时分别为20 mol和10 mol;达平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为( )
A.10 mol和10% B.20 mol和20% C.20 mol和40% D.20 mol和80%
高一化学选择题简单题
在密闭容器中,对于反应:2SO2(g)+O2(g) 2SO3(g),SO2和O2起始时分别为20 mol和10 mol;达平衡时,SO2的转化率为80%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为( )
A.10 mol和10% B.20 mol和20% C.20 mol和40% D.20 mol和80%
高一化学选择题简单题查看答案及解析
在密闭容器中进行反应2SO2 + O2 2SO3 ,SO2、O2、SO3的起始浓度分别为0.2 mol·L-1,0.1 mol·L-1,0.2 mol·L-1,当平衡时,下列数据正确的是
A.SO2的浓度为0.25 mol·L-1 ,SO3的浓度为0.25mol·L-1
B.SO3的浓度为0.3mol·L-1
C.SO2的浓度为0.4 mol·L-1 ,O2的浓度为0.2 mol·L-1
D.SO3的浓度为0.4 mol·L-1
高一化学选择题中等难度题查看答案及解析
已知SO2和O2反应生成2molSO3时,放出的热量为QKJ,在1L的密闭容器中进行反应 2SO2(g)+O2(g)2SO3(g),SO2、O2、SO3的起始物质的量分别为0.2mol、0.1mol、0.2mol,下列叙述正确的是
A. 反应达到平衡时放出的热量为0.1QKJ
B. 某时刻,SO3的物质的量为0.28 mol,则SO2的转化率为40%
C. 某时刻,SO2、O2、SO3的物质的量分别为0.3mol、0.15mol、0.15mol
D. 某时刻,SO3的浓度可能为0.4mol-1·L-1
高一化学单选题中等难度题查看答案及解析
向体积为2 L的密闭容器中充入2 mol SO2和1 mol O2,测得起始容器压强为p,一定条件下发生反应:2SO2(g)+O2(g)2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入2 mol SO3,则下列说法正确的是
A. 充入2 mol SO3后,SO2的物质的量增大
B. 第一次反应达到平衡时共放出热量176.4 kJ
C. 充入2 mol SO3达到新平衡时,容器内的压强为1.4p
D. 降低容器的温度可使新平衡时各物质的体积分数与第一次平衡时相同
高一化学选择题简单题查看答案及解析
一定条件下2L的密闭容器中,有反应2SO2(g)+O2(g) 2SO3(g)+Q。
(1)若起始时SO2为2mol,反应2min后SO2剩余1.6mol,则在0~2min内SO2的平均反应速率为_____mol/(L·min);若继续反应使SO2剩余1.2mol,则需要再反应的时间_____2min(不考虑温度变化);(选填“>”、“<”或“=”)
(2)反应达到平衡后,在其他条件不变的情况下,升高温度,下列说法正确的是_____;(选填字母)
A.正反应速率增大,逆反应速率减小,平衡向正反应方向移动
B.正反应速率减小,逆反应速率增大,平衡向逆反应方向移动
C.正、逆反应速率都增大,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
(3)若反应速率(v)与时间(t)的关系如图所示,则导致t1时刻速率发生变化的原因可能是_____;(选填字母)
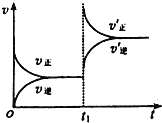
A.增大A的浓度 B.缩小容器体积
C.加入催化剂 D.降低温度
(4)在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器的接触室(见图)。下列说法错误的是_____。(选填字母)
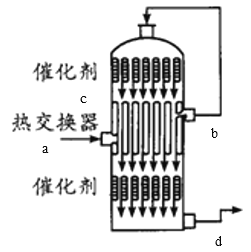
A.a、b两处的混合气体成分相同,b处气体温度高
B.c、d两处的混合气体成分不同
C.热交换器的作用是预热待反应的气体,冷却反应后的气体
D.反应气体进行两次催化氧化的目的是提高SO2的转化率
(5)硫酸工业制法中硫铁矿是制取SO2的主要原料。硫铁矿氧化焙烧的化学反应如下:3FeS2+8O2→Fe3O4+6SO2 4FeS2+11O2→2Fe2O3+8SO2,若48molFeS2完全反应耗用氧气131 mol,则反应产物中Fe3O4与Fe2O3物质的量之比为________。
高一化学综合题中等难度题查看答案及解析
相同温度下,容积均恒为2L的甲、乙、丙3个密闭容器中发生反应:2SO2(g)+O2(g) 2SO3(g) △H=-197kJ·mol-l。实验测得起始、平衡时的有关数据如下表:

下列叙述正确的是
A.Q1>Q3>Q2 =78.8kJ
B.三个容器中反应的平衡常数均为K=2
C.甲中反应达到平衡时,若升高温度,则SO2的转化率将大于50%
D.若乙容器中的反应经tmin达到平衡,则0~tmin内,v(O2)= mol/(L·min)
高一化学选择题困难题查看答案及解析
一定条件下,在容积为2L的密闭容器内发生反应:2SO2(g)+O2(g)2SO3(g)已知起始充入4molSO2(g)和2molO2(g),经2s后测得SO3的浓度为0.6mol/L。下列说法正确的是
A.降低体系温度能加快该反应的速率
B.0~2S内用O2表示该反应的平均费用速率为0.15mol/(L·s)
C.增大SO3的浓度能减慢该反应速率
D.反应一段时间后可生成4molSO3
高一化学选择题中等难度题查看答案及解析
已知2SO2 (g)+O2 (g) 2SO3 (g);△H =﹣197kJ•mol﹣1,向同温、同体积的三个密闭容器中分别充入气体,起始投料量如下表:
| SO2 (mol) | O2 (mol) | SO3 (mol) | |
| 甲 | 2 | 1 | 0 |
| 乙 | 4 | 2 | 0 |
| 丙 | 0 | 0 | 2 |
恒温、恒容下反应达平衡时,下列关系一定正确的是
A.SO3的质量m:2m甲 = m乙
B.容器内压强P:2P丙 > P乙
C.反应放出或吸收热量的数值Q:Q甲 > Q丙
D.c(SO2)与c(O2)之比a:a丙 > a乙
高一化学选择题中等难度题查看答案及解析
在一密闭容器中进行如下反应:2SO2(气)+O2(气)2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
A. SO2为0.4mol/L、O2为0.2mol/L B. SO3为0.4mol/L
C. SO2、SO3均为0.15mol/L D. SO2为0.25mol/L
高一化学单选题中等难度题查看答案及解析
在一密闭容器中进行如下反应:2SO2(气)+O2(气)2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是 ( )
A、SO2为0.4mol/L、O2为0.2mol/L B、SO2、SO3均为0.15mol/L
C、SO2为0.25mol/L D、SO3为0.4mol/L
高一化学选择题中等难度题查看答案及解析