-
请回答下列问题:
(1)纯水在T℃时,pH=6,该温度下0.1 mol•L-1 的NaOH 溶液中,由水电离出的c(OH-)=__________ mol•L-1。
(2)在25℃下;将amol·L-1的NaX溶液与0.01mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,则a__________0.01(填“>”、“<”或“=”);用含a的代数式表示HX 的电离常数 Ka=________。
(3)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
①CO(g)+NO2(g)=NO(g)+CO2(g) △H=-aKJ·mol-1 (a>0)
②2CO(g)+2NO(g)=N2(g)+2CO2(g) △H=-bKJ·mol-1 (b>0)
若用标准状况下5. 6LCO将NO2还原至N2(CO完全反应),则整个过程中转移电子的物质的量为_____ mol,放出的热量为_________ kJ(用含有a和b的代数式表示)。
(4)已知AgCl、Ag2CrO4 (砖红色) 的Ksp分别为2×10-10和2.0×10-12。分析化学中,测定含氯的中性溶液中Cl- 的含量,以K2CrO4作指示剂,用AgNO3溶液滴定。滴定过程中首先析出沉淀_________,当溶液中Cl- 恰好完全沉淀(浓度等于1.0×10-5 mol·L-1) 时,此时溶液中c(CrO42-)等于__________ mol•L-1。
高二化学填空题中等难度题查看答案及解析
-
水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在 100℃时,pH=6,该温度下 0.1mol•L﹣1 的 NaOH 溶液中,溶液的 pH=_____。
(2)25℃时,向水中加入少量碳酸钠固体,得到 pH 为 11 的溶液,其水解的离子方程式为_____, 由水电离出的 c(OH﹣)=_____mol•L﹣1。
(3)体积均为 100mL、pH 均为 2 的盐酸与一元酸 HX,加水稀释过程中 pH 与溶液体积的关系如图所示,则 HX 是_____(填“强酸”或“弱酸”),理由是_____。
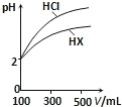
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。
化学式
电离常数(25℃)
HCN
K=4.9×10﹣10
CH3COOH
K=1.8×10﹣5
H2CO3
K1=4.3×10﹣7、K2=5.6×10﹣11
①25℃时,等浓度的 NaCN 溶液、Na2CO3 溶液和 CH3COONa 溶液,pH 由大到小的顺序为________(填化学式)。
②25℃时,在 0.5mol/L 的醋酸溶液中由醋酸电离出的 c(H+)约是由水电离出的 c(H+)的_________倍。
高二化学填空题困难题查看答案及解析
-
水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在 100℃时,pH=6,该温度下 0.1mol•L﹣1 的 NaOH 溶液中,溶液的 pH=_____。
(2)25℃时,向水中加入少量碳酸钠固体,得到 pH 为 11 的溶液,其水解的离子方程式为_____, 由水电离出的 c(OH﹣)=_____mol•L﹣1。
(3)体积均为 100mL、pH 均为 2 的盐酸与一元酸 HX,加水稀释过程中 pH 与溶液体积的关系如图所示,则 HX 是_____(填“强酸”或“弱酸”),理由是_____。
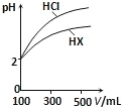
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。
化学式
电离常数(25℃)
HCN
K=4.9×10﹣10
CH3COOH
K=1.8×10﹣5
H2CO3
K1=4.3×10﹣7、K2=5.6×10﹣11
①25℃时,等浓度的 NaCN 溶液、Na2CO3 溶液和 CH3COONa 溶液,pH 由大到小的顺序为________(填化学式)。
②25℃时,在 0.5mol/L 的醋酸溶液中由醋酸电离出的 c(H+)约是由水电离出的 c(H+)的_________倍。
高二化学填空题困难题查看答案及解析
-
水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在100℃时,pH=6,该温度下0.1mol•L-1的NaOH溶液中,溶液的pH= .
(2)25℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为 , 由水电离出的c(OH-)= mol·L-1.
(3)体积均为100mL、pH均为2的盐酸与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX是 (填“强酸”或“弱酸”),理由是 .
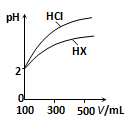
高二化学填空题困难题查看答案及解析
-
请回答下列问题:
(1)纯水在T ℃时pH=6,该温度下1 mol/L的NaOH溶液中,由水电离出的c(OH-)= mol/L。
(2)某一元弱酸溶液(A)与二元强酸(B)的pH相等。若将两溶液稀释相同的倍数后,pH(A) pH(B) (填“>”、“=”或“<”);现用上述稀释溶液中和等浓度等体积的NaOH溶液,则需稀释溶液的体积V(A) V(B)(填“>”、“=”或“<”)。
(3)已知:二元酸H2R 的电离方程式是:H2R=H++HR﹣,HR﹣
R2﹣+H+,若0.1mol•L﹣1NaHR溶液的c(H+)=a mol•L﹣1,则0.1mol•L﹣1H2R溶液中c(H+) (0.1
+a) mol•L﹣1(填“<”、“>”或“=”),理由是 。
(4)电离平衡常数是衡量弱电解质电离程度的物理量。已知:
化学式
电离常数(25 ℃)
HCN
K=4.9×10-10
CH3COOH[]
K=1.8×10-5
H2CO3
K1=4.3×10-7、K2=5.6×10-11
①25 ℃时,有等浓度的HCN溶液、H2CO3溶液和CH3COOH溶液,三溶液的pH由大到小的顺序为________(用化学式表示)。
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为__________________。
高二化学填空题极难题查看答案及解析
-
水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在100 ℃时,pH=6,该温度下0.1 mol·L-1的NaOH溶液的pH=_____________。
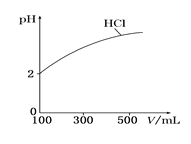
(2)体积均为100 mL、pH均为2的盐酸与一元弱酸HX,加水稀释过程中盐酸的pH与溶液体积的关系如图所示,则在图上画出HX加水至500mL稀释过程中pH值的变化曲线_____,并说明理由___________。
(3)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
化学式
电离平衡常数(25 ℃)
HCN
K=4.9×10-10
CH3COOH
K=1.8×10-5
H2CO3
K1=4.3×10-7,K2=5.6×10-11
25 ℃时,在0.5 mol·L-1的醋酸溶液中由醋酸电离出的c(H+)约是由水电离出的c(H+)的_____倍。
(4)写出在NaCN溶液中通入少量CO2反应的离子方程式________________________。
(5)某兴趣小组为研究碳酸钠水解平衡与温度的关系,用数字实验系统测定一定浓度碳酸钠溶液的pH与温度的关系,得到曲线如图,下列分析合理的是___________。
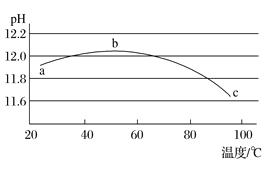
A 碳酸钠水解是吸热反应 B ab段说明水解平衡向右移动
C bc段说明水解平衡向左移动 D 水的电离平衡也对pH产生影响
高二化学综合题中等难度题查看答案及解析
-
请回答下列问题:
(1)纯水在T ℃时,pH=6,该温度下1 mol·L-1的NaOH溶液中,由水电离出的c(OH-)=_______mol·L-1。
(2)某一元弱酸溶液(A)与二元强酸(B)的pH相等。若将两溶液稀释相同的倍数后,pH(A)___pH(B) (填“>”、“=”或“<”);
现用上述稀释溶液中和等浓度等体积的NaOH溶液,则需稀释溶液的体积V(A) _____V(B)(填“>”、“=”或“<”)。
(3)25℃时,0.05mol/LH2SO4溶液的pH=_________;0.05mol/LBa(OH)2溶液中的c(H+)=_______。
(4)某温度下纯水中的c(H+)=2×10-7mol/L,则此时水中的c(OH-)=____________;若温度不变,滴入稀盐酸,使c(H+)=5×10-4mol/L,则溶液中c(OH-)=_________,此时溶液中由水电离产生的c(H+)=_________。
高二化学简答题中等难度题查看答案及解析
-
请按要求回答下列问题:
(1)纯水在100℃时pH=6,该温度下1mol·L-1的NaOH溶液中,由水电离出的c(OH-)=__mol·L-1。
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为__,由水电离出的c(OH-)=___mol·L-1。
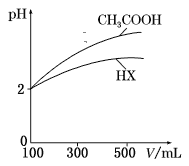
(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离常数___(填“大于”“小于”或“等于”)CH3COOH的电离常数。理由是___。
(4)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
化学式
电离常数(25℃)
HCN
K=4.9×10-10
CH3COOH
K=1.8×10-5
H2CO3
K1=4.3×10-7、K2=5.6×10-11
①25℃时,有等pH的a.NaCN溶液、b.Na2CO3溶液和c.CH3COONa溶液,三溶液的浓度由大到小的顺序为___。(用a、b、c表示)
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为___。
③25℃时,等浓度的HCN和NaCN混合溶液显___性。(酸、碱、中)
(5)室温时,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
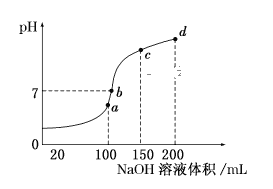
试分析图中a、b、c、d四个点,水的电离程度最大的是__;在b点,溶液中各离子浓度由大到小的排列顺序是__。
高二化学综合题中等难度题查看答案及解析
-
水是生命的源泉、工业的血液、城市的命脉。请回答下列问题:
(1)纯水在25 ℃时,pH=7,该温度下1 mol·L-1的NaOH溶液中,由水电离出的c(OH-)=________mol·L-1。
(2)25 ℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为__________,由水电离出的c(OH-)=________mol·L-1。
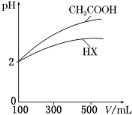
(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如右图所示,则HX的电离常数________(填“大于”“小于”或“等于”)CH3COOH的电离常数。理由是_______。
(4)电离常数是衡量弱电解质电离程度强弱的物理量。已知:
化学式
电离常数(25 ℃)
HCN
K=4.9×10-10
CH3COOH
K=1.8×10-5
H2CO3
K1=4.3×10-7、K2=5.6×10-11
25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为____________________。
高二化学填空题困难题查看答案及解析
-
请回答下列问題:
(1)纯水在T ℃时,pH=6,该温度下1 mol·L-1的NaOH溶液中,由水电离出的c(OH-)=________ mol·L-1。
(2)某一元弱酸溶液(A)与二元强酸(B)的pH相等。若将两溶液稀释相同的倍数后,pH(A)___pH(B) (填“>”、“=”或“<”);现用上述稀释溶液中和等浓度等体积的NaOH溶液,则需稀释溶液的体积V(A)_____V(B)(填“>”、“=”或“<”)。
(3)已知:二元酸H2R 的电离方程式是:H2R=H++HR﹣,HR﹣
R2﹣+H+,
①若0.1mol•L-1NaHR溶液的c(H+)=a mol•L﹣1,则0.1mol•L﹣1H2R溶液中c(H+)_____(0.1+a) mol•L﹣1(填“<”、“>”或“=”),理由是___________________。
② NaHR溶液呈_____性,理由是___________________。
③某温度下,向10 mL、0.1 mol/L NaHA溶液中加入0.1 mol/L KOH溶液V mL至中性,此时溶液中以下关系一定正确的是______(填写字母)。
A.溶液 pH=7 B.水的离子积KW=c2(OH-) C.V=10 D.c(K+)<c(Na+)
高二化学简答题简单题查看答案及解析