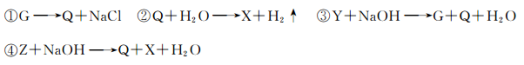-
G、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的化学式,但知道它们在一定条件下具有如下的转化关系(未配平):
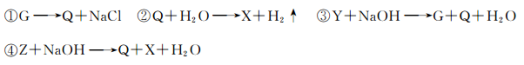
则G、Q、X、Y、Z这五种化合物中氯元素的化合价由低到高的顺序为( )
A.QGZYX B.GYQZX C.GYZQX D.ZXGYQ
-
(10分)G、Q、X、Y、Z均为氯的含氧化合物。我们不了解它们的化学式,但知道它们在一定条件下具有如下转化关系(未配平)
①G Q+NaCl
Q+NaCl
②Q +H2O X+H2
X+H2
③Y+NaOH G+Q+H2O
G+Q+H2O
④Z+NaOH  Q+X+H2O
Q+X+H2O
(1)这五种化合物中氯的化合价由高到低的顺序是 ;
(2)臭氧与二氧化氯作用,可以得到红色油状的六氧化二氯Cl2O6 ,遇有机物会爆炸。它与氢氧化钠溶液反应可得到氯的两种含氧酸盐,其离子方程式是: 。
(3)亚氯酸钠NaClO2 ,可以作漂白剂,在常温下不见光可以保存约1年。但在酸性条件下因为生成亚氯酸而发生分解反应:HClO2  ClO2+H++Cl―+H2O,分解时,刚加入硫酸时的反应很慢,随后突然迅速放出气态的二氧化氯。写出配平的化学方程式 。
ClO2+H++Cl―+H2O,分解时,刚加入硫酸时的反应很慢,随后突然迅速放出气态的二氧化氯。写出配平的化学方程式 。
如果有2molHClO2发生反应,则转移电子的个数是 ,后期反应速率迅速加快的原因是 。
A、酸使亚氯酸的氧化性增强 B、溶液中的氢离子还起了催化作用
C、溶液中的氯离子还起了催化作用 D、逸出的气体使反应生成物的浓度降低
-
G、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的化学式,但知道它们在一定条件下具有如下的转化关系(未配平):
①G→Q+NaCl ②Q+H2O→X+H2
③Y+NaOH→G+Q+H2O ④Z+NaOH→Q+X+H2O
则G、Q、X、Y、Z这五种化合物中氯元素的化合价由低到高的顺序为
A.QGZYX B.GYQZX C.GYZQX D.ZXGYQ
-
G、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的化学式,但知道它们在一定条件下具有如下的转化关系(未配平):
①G→Q+NaCl ②Q+H2O→X+H2 ③Y+NaOH→G+Q+H2O ④Z+NaOH→Q+X+H2O
则G、Q、X、Y、Z这五种化合物中氯元素的化合价由低到高的顺序为( )
A.QGZYX B.GYQZX C.GYZQX D.ZXGYQ
-
G、W、X、Y、Z均为含氯的化合物,我们不了解它们的化学式,但知道它们在一定条件下具有如下的转化关系(未配平):
①G→W+NaCl ②W+H2O X+H2 ③Y+NaOH→G+W+H2O
X+H2 ③Y+NaOH→G+W+H2O
④Z+NaOH→W+X+H2O这五种化合物中的氯的化合价由低到高的顺序是
A.W、G、Z、Y、X B.G、Y、W、Z、X
C.G、Y、Z、W、X D.Z、X、G、Y、W
-
G、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的分子式(或化学式),但知道它们在一定条件下具有如下的转换关系(未配平):(1)G→Q+NaCl (2)Q+H2O X+H2 (3)Y+NaOH→G+Q+H2O (4)Z+NaOH→Q+X+H2O这五种化合物中氯的化合价由低到高的顺序为
X+H2 (3)Y+NaOH→G+Q+H2O (4)Z+NaOH→Q+X+H2O这五种化合物中氯的化合价由低到高的顺序为
A. Q、G、Z、Y、X B. G、Y、Q、Z、X
C. G、Y、Z、Q、X D. Z、X、G、Y、Q
-
G、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的化学式,但知道它们在一定条件下具有如下的转换关系(未配平):
(1)G→Q+NaCl (2)Q+H2O→X+H2↑
(3)Y+NaOH→G+Q+H2O (4)Z+NaOH→Q+X+H2O
这五种化合物中氯的化合价由低到高的顺序是____________________________________
-
G、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的化学式,但知道它们在一定条件下具有如下的转换关系(为配平):
①G→Q+NaCl
②Q+H2O →X+H2
③ Y+NaOH →G+Q+H2O
④Z+NaOH→Q+X+H2O
这五种化合物中 氯的化合价由低到高的顺序为
A.QGZYX B.GYQZX C.GYZQX D.ZXGYQ
-
G、Q、X、Y、Z均为氯的含氧化合物,我们不了解它们的分子式或化学式,但知道它们在一定条件下具有如下的转换关系(未配平):
(1)G→Q十NaCl
(2)Y十NaOH→G十Q十H2O
(3)Q+H2O X+H2
X+H2
(4)Z十NaOH→Q十X十H2O
这五种化合物中氯的化合价由低到高的顺序为( )
A.QGZYX
B.GYQZX
C.GYZQX
D.ZXGYQ
-
X、Y、Z、W均为含氮元素的化合物,我们不了解它们的化学式,但知道它们在一定条件
下有如下转换关系(未配平,反应全是氧化还原反应):(1) X→Y+ O2 (2) Z + Y→H2O + W (3) Y + SO2→Z + SO3 则这四种化合物中氮的化合价由高到低的顺序为
A.Z W Y X B.X Y W Z C.YW ZX D.ZW X Y
Q+NaCl
X+H2
G+Q+H2O
Q+X+H2O
ClO2+H++Cl―+H2O,分解时,刚加入硫酸时的反应很慢,随后突然迅速放出气态的二氧化氯。写出配平的化学方程式 。