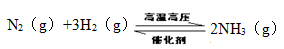-
(化学-化学与技术)
金属铝的生产是以Al2O3为原料,在熔融状态下进行电【解析】
2Al2O3 4Al+3O2
4Al+3O2
请回答下列问题:
(1)冰晶石(Na3AIF6)的作用是______.
(2)电解生成的金属铝是在熔融液的______(填“上层”或“下层”).
(3)阴极和阳极均由______材料做成;电解时所消耗的电极是______(填“阳极”或“阴极”).
(4)铝是高耗能产品,废旧铝材的回收利用十分重要.在工业上,最能体现节能减排思想的是将回收铝做成______(填代号).
a.冰晶石 b.氧化铝 c.铝锭 d.硫酸铝.
-
(化学-化学与技术)
 金属铝的生产是以Al2O3为原料,在熔融状态下进行电【解析】
金属铝的生产是以Al2O3为原料,在熔融状态下进行电【解析】

请回答下列问题:
 (1)冰品石(Na3AlF6)的作用是 。
(1)冰品石(Na3AlF6)的作用是 。
(2)电解生成的金属铝是在熔融液的 (填“上层”或“下层”)。
 (3)阴极和阳极均由 材料做成;电解时所消耗的电极是 (填“阳极”或“阴极”)。
(3)阴极和阳极均由 材料做成;电解时所消耗的电极是 (填“阳极”或“阴极”)。
(4)铝是高耗能产品,废旧铝材的回收利用十分重要。在工业上,最能体现节能减排思想的是将回收铝做成 (填代号)。
 a.冰品石 b.氧化铝 c.铝锭 d.硫酸铝
a.冰品石 b.氧化铝 c.铝锭 d.硫酸铝
-
Ⅰ.金属铝的生产是以Al2O3为原料,在熔融状态下进行电【解析】

请回答下列问题:
 (1)冰晶石(Na3AlF6)的作用是 。
(1)冰晶石(Na3AlF6)的作用是 。
(2)电解生成的金属铝是在熔融液的 (填“上层”或“下层”)。
 (3)电解时所消耗的电极是 (填“阳极”或“阴极”)。
(3)电解时所消耗的电极是 (填“阳极”或“阴极”)。
(4)铝是高耗能产品,废旧铝材的回收利用十分重要。在工业上,最能体现节能减排思想的是将回收铝做成 (填代号)。
 a.冰晶石 b.氧化铝 c.铝锭 d.硫酸铝
a.冰晶石 b.氧化铝 c.铝锭 d.硫酸铝
Ⅱ.钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在_________部分发生反应
(2)炼钢时,除磷的化学方程式为_________;加入硅、锰和铝的目的是_______。
(3)不锈钢含有的Cr元素是在炼钢过程的氧吹_______(填“前”或“后”)加入,
原因是_____________。
(4)炼铁和炼钢生产中,尾气均含有的主要污染物是_________。从环保和经济角度考虑,上述尾气经处理可用作________。
-
下列叙述正确的是( )
A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂
B.金属铝的生产是以Al2O3为原料,在熔融状态下进行电解
C.Si是半导体材料,所以用Si作光导纤维
D.NaHCO3溶液中含有少量Na2CO3可以用澄清石灰水除去
-
Ⅰ.铝是地壳中含量最高的金属元素,其单质及其合金在生产生活中的应用十分广泛。
(1)金属铝的生产是以Al2O3为原料,与冰晶石(Na3AlF6)在熔融状态下进行电解,则化学方程式为________ 。
其电极均由石墨材料做成,则电解时不断消耗的电极是 (填“阴极”或“阳极”)。
(2)对铝制品进行抗腐蚀处理,可延长其使用寿命。以处理过的铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极反应式为 。
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,化学反应为:2Al+3Ag2O+2NaOH+3H2O 2Na[Al(OH)4]+6Ag, 则负极的电极反应式为________
2Na[Al(OH)4]+6Ag, 则负极的电极反应式为________
,正极附近溶液的pH (填“变大”、“不变”或“变小”)。
Ⅱ.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
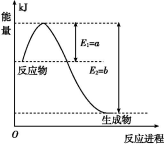
(1)如图是在一定温度和压强下N2和H2反应生成1 mol NH3过程中能量变化示意图,请写出合成氨的热化学反应方程式: ________(ΔH的数值用含字母a、b的代数式表示)。
(2)工业合成氨的反应为N2(g)+3H2(g) 2NH3(g)。在一定温度下,将一定量的N2和H2通入体积为1 L的密闭容器中,反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是 。
2NH3(g)。在一定温度下,将一定量的N2和H2通入体积为1 L的密闭容器中,反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是 。
A.增大压强 B.增大反应物的浓度
C.使用催化剂 D.降低温度
Ⅲ.铁及其化合物在生活、生产中有广泛应用。请回答下列问题:黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为:3FeS2+8O2 6SO2+Fe3O4,有3 mol FeS2参加反应,转移 mol电子。
6SO2+Fe3O4,有3 mol FeS2参加反应,转移 mol电子。
(2)氯化铁溶液称为化学试剂中的“多面手”,写出SO2通入氯化铁溶液中反应的离子方程式: 。
-
I、铝是地壳中含量最高的金属元素,其单质及其合金在生产生活中的应用十分广泛。
(1)金属铝的生产是以Al2O3为原料,与冰晶石(Na3AlF6)在熔融状态下进行电解,则化学方程式为:________________________________________________ .其电极均由石墨材料做成,则电解时不断消耗的电极是 ________________________________________________;(填“阴极”或“阳极”)。
(2)对铝制品进行抗腐蚀处理,可延长其使用寿命.以处理过的铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极反应式为________________________________________________________________________ ;
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,化学反应为2Al+3Ag2O+2NaOH+3H2O═2Na[Al(OH)4]+6Ag,则负极的电极反应式为________________ ________________,正极附近溶液的pH________________________________________(填变大、不变或变小)。
II、氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
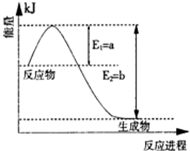
(1)图是在一定温度和压强下N2和H2反应生成1molNH3过程中能量变化示意图,请写出合成氨的热化学反应方程:________________________________________________________________________(△H的数值用含字母a、b的代数式表示)。
(2)工业合成氨反应如下,
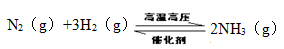
在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中,反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是________________________ 。
A.增大压强 B.增大反应物的浓度 C.使用催化剂 D.降低温度
Ⅲ、铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为:

有3mol FeS2参加反应,转移________________________ mol电子。
(2)氯化铁溶液称为化学试剂中的“多面手”,写出SO2通入氯化铁溶液中反应的离子方程式________________________________________________________________________________________________________________________________________________________ 。
-
(12分)【化学—化学与技术】
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成。

(1)工业上采用电解氧化铝和冰晶石(Na3AlF6)熔融体的方法冶炼得到金属铝:2Al2O3 4Al+3O2↑。
4Al+3O2↑。
加入冰晶石的作用为_______________________。
(2)上述工艺所得铝材中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池中阳极的电极反应式为________,下列可作阴极材料的是______。
a.铝材 b.石墨 c.铅板 d.纯铝
(3)阳极氧化能使金属表面生成致密的氧化膜。以稀硫酸为电解液,铝阳极发生的电极反应式_______________________。在铝阳极氧化过程中,需要不断地调整电压,理由是_________________。
(4)下列说法正确的是__________________。
a.阳极氧化是应用原电池原理进行金属材料表面处理的技术
b.铝的阳极氧化可增强铝表面的绝缘性能
c.铝的阳极氧化可提高金属铝及其合金的耐腐蚀性,但耐磨性下降
d.铝的阳极氧化膜富多孔性,具有很强的吸附性能,能吸附染料而呈各种颜色
-
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成。请回答下列问题:
(1)工业上采用电解氧化铝-冰晶石(Na3AlF6)熔融体的方法冶炼得到金属铝:
2Al2O3  4Al+3O2↑加入冰晶石的作用:_______________________________。
4Al+3O2↑加入冰晶石的作用:_______________________________。
(2)上述工艺所得铝材中往往含有少量Fe和Si等杂质,可用电解方法进一步提纯,该电解池中阳极的电极反应式为 ,下列可作阴极材料的是________________。
A.铝材 B.石墨 C.铅板 D.纯铝
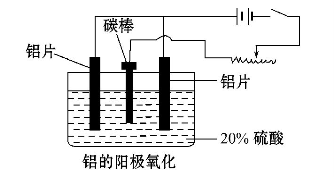
(3)阳极氧化能使金属表面生成致密的氧化膜。以稀硫酸为电解液,铝阳极发生的电极反应式为__________________________________。
(4)在铝阳极氧化过程中,需要不断地调整电压,理由是____________ 。
(5)下列说法正确的是 。
A. 阳极氧化是应用原电池原理进行金属材料表面处理的技术
B. 铝的阳极氧化可增强铝表面的绝缘性能
C. 铝的阳极氧化可提高金属铝及其合金的耐腐蚀性,但耐磨性下降
D. 铝的阳极氧化膜富有多孔性,具有很强的吸附性能,能吸附染料而呈各种颜色
-
下列叙述正确的是( )
A.汽油、柴油和植物油都是碳氢化合物
B.浓H2SO4具有吸水性,可用来干燥氨气
C.金属铝的生产是以Al2O3为原料,在熔融状态下进行电解
D.糖类、蛋白质、油脂属于天然高分子化合物
-
工业上通常以铝土矿(主要成分为Al2O3)为原料制备无水氯化铝:2Al2O3+6Cl2 4AlCl3+3O2 ↑。请回答下列问题:
4AlCl3+3O2 ↑。请回答下列问题:
(1)上述反应涉及的元素中,最外层有2个未成对电子的元素是__________;简单离子的离子半径最小的元素,其原子核外有_____种不同能级的电子。
(2)已知元素周期表中,镓(31Ga)与铝元素同一主族,写出Ga的最外层电子排布式:______
(3)镓(Ga)有两种天然同位素,一种是 ,其原子在天然同位素原子中所占的百分比为60%。实验测得溴化镓(GaBr3)的摩尔质量为309.8 g/mol,则由此推知镓的另一种同位素是_________。
,其原子在天然同位素原子中所占的百分比为60%。实验测得溴化镓(GaBr3)的摩尔质量为309.8 g/mol,则由此推知镓的另一种同位素是_________。
(4)为促进反应的进行,实际生产中需加入焦炭,其原因是________。