-
(1)中国古代四大发明之一——黑火药,它的爆炸反应为:2KNO3 + 3C+S A + N2↑+ 3CO2↑(已配平)
A + N2↑+ 3CO2↑(已配平)
①除S外,上列元素的电负性从大到小依次为_________。
②在生成物中,A的电子式________,含极性共价键的分子的中心原子轨道杂化类型为_____________。
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为________。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为________,Q2+的未成对电子数是__________。
(3)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H2O)6-n]x++xR-H→Rx[CrCln(H2O)6-n]x++xH+,交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成。将含0.0015 mol [CrCln(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200 mol·L-1NaOH溶液25.00 ml,可知该配离子的化学式为_______。
-
(1)中国古代四大发明之一--黑火药,它的爆炸反应为S+ 2KNO3+ 3C 3CO2↑+ A + N2↑(已配平)
3CO2↑+ A + N2↑(已配平)
①除S外,上列元素的电负性从大到小依次为__________。
②生成物A的晶体类型为__________,含极性共价键的分子的中心原子轨道杂化类型为_______。
③已知CN-与N2结构相似,推算HCN分子中 键与
键与 键数目之比为____________。
键数目之比为____________。
(2)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_________。
(3)下列有关说法正确的是______________。
A.镧、锰、氧分别位于周期表f、d、p区
B.氧的第一电离能比氮的第一电离能大
C.铬的堆积方式与钾相同,则其堆积方式如图

D.锰的电负性为1.59 ,Cr的电负性为1.66,说明锰的金属性比铬强
(4)含有Cu2+ 的溶液中加入过量氨水,发现生成深蓝色溶液,试写出反应的离子方程式:_______。
(5)氮化硼形成立方晶体,晶体结构类似金刚石,如图所示。

已知:该晶体密度为ρg·㎝-3,NA代表阿伏加德罗常数的值。
①该晶体的化学式为______________。
②在该晶体中,B与N形成共价键的键长(d)为________________________pm(列式即可)。
-
(1)中国古代四大发明之一一黑火火药,它的爆炸反应为;S+2KNO3+3C  3CO2↑+A+N2↑(已配平)
3CO2↑+A+N2↑(已配平)
①除S外,上列元素的电负性从大到小依次为______.
②在生成物中,A的晶体类型为_______,含极性共价键的分子的中心原子轨道杂化类型为_______.
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为_________.
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为______,Q2+的未成对电子数是________.
(3)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)]6-nx+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H2O)]6-nx++xR-H→Rx[CrCln(H2O)]6-n+xH+交换出来的H+经中和测定,即可求出x和n,确定配离子的组成。将含0.0015mol[CrCln(H2O)]6-nx+的溶液,与R-H完全交换后,中和生成的H+需浓度为0.1200mol▪L-1NaOH溶液25.00mL,该配离子的化学式为______.
-
Ⅰ.黑火药是中国古代四大发明之一,已知它在爆炸时发生反应的化学方程式为:
S+2KNO3+3C==A+N2↑+3CO2↑(已配平,A特指某一晶体);请回答下列问题:
(1)S外,上述元素的电负性从大到小依次为________________(填写元素符号)。
(2)在生成物中,A的晶体类型为__________,含极性共价键的分子内的中心原子轨道杂化类型为。
(3)已知CN-与N2为等电子体,推算HCN分子中σ键与π键数目之比为___________。
Ⅱ.原子序数小于36的元素E和G,在周期表中既处于同一周期又位于同一族,且原子序数G比E多2。则G元素的基态原子外围电子(价电子)排布式为;E3+离子的核外未成对电子数是___________。
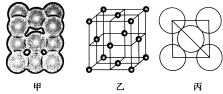
Ⅲ.若某金属单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。则晶胞中该原子的配位数为;该晶胞的空间利用率为________________。该单质晶体中原子的堆积方式为四种基本堆积方式中的____________。
Ⅳ.在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6﹣n]x+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R—H),可发生离子交换反应:[CrCln(H2O)6﹣n]x++xR—HRx [CrCln(H2O)6﹣n]+xH+;交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成。现将含0.0015mol[CrCln(H2O)6﹣n]x+的溶液,与R—H完全交换后,中和生成的H+需浓度为0.1200mol·L-1NaOH溶液25.00mL,可知该配离子的化学式为,中心离子的配位数为_________。
[CrCln(H2O)6﹣n]+xH+;交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成。现将含0.0015mol[CrCln(H2O)6﹣n]x+的溶液,与R—H完全交换后,中和生成的H+需浓度为0.1200mol·L-1NaOH溶液25.00mL,可知该配离子的化学式为,中心离子的配位数为_________。
-
黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为S(s)+2KNO3(s)+3C(s)=K2S(s) +N2(g) +3CO2 (g) △H = xkJ•mol-1。已知:
①碳的燃烧热△H1 =a kJ • mol-1 ;
②S(s)+2K(s) =K2S(s) △H2=b kJ•mol-1 ;
③2K(s)+N2(g)+3O2(g)=2KNO3(s) △H 3=ckJ•mol-1。
则x为
A.a+b-c B.c+3a-b C.3a + b-c D.c + a- b
-
黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为
S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H=xkJ•mol-1
已知:碳的燃烧热△H1=akJ•mol-1
S(s)+2K(s)═K2S(s)△H2=bkJ•mol-1
2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=ckJ•mol-1则x为
A.3a+b-c B.c-3a-b C.a+b-c D.c-a-b
-
黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为: S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H=x kJ•mol﹣1 已知:碳的燃烧热△H1=a kJ•mol﹣1S(s)+2K(s)═K2S(s)△H2=b kJ•mol﹣12K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=c kJ•mol﹣1 则x为( )
A. 3a+b﹣c B. c﹣3a﹣b C. a+b﹣c D. c﹣a﹣b
-
黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g) △H=x kJ/mol
已知:碳的燃烧热△H1=a kJ/mol
S(s)+2K(s)=K2S(s) △H2=b kJ/mol
2K(s)+N2(g)+3O2(g)=2KNO3(s) △H3=c kJ/mol,则x为( )
A.a+b-c B.c-3a-b
C.3a+b-c D.c-a-b
-
黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2 (g) △H=xkJ·mol-l
已知:碳的燃烧热△H1=a kJ·mol-l
S(s)+2K(s)=K2S(s) △H2=b kJ·mol-1
2K(s)+N2(g)+3O2(g)=2KNO3(s) △H3 =c kJ·mol-l
则x为( )
A.c-3a-b B.3a+b-c C.a+b-c D.c-a-b
-
黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g) ΔH=xkJ·mol-1
已知:碳的燃烧热 ΔH1=akJ·mol-1
S(s)+2K(s)=K2S(s) ΔH2=bkJ·mol-1
2K(s)+N2(g)+3O2(g)=2KNO3(s) ΔH3=ckJ·mol-1
则x为
A. 3a+b-c B. c +3a-b C. a+b-c D. c+a-b

[CrCln(H2O)6﹣n]+xH+;交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成。现将含0.0015mol[CrCln(H2O)6﹣n]x+的溶液,与R—H完全交换后,中和生成的H+需浓度为0.1200mol·L-1NaOH溶液25.00mL,可知该配离子的化学式为,中心离子的配位数为_________。

