-
已知KNO3、Cu(NO3)2、AgNO3三种硝酸盐热分解的反应方程式如下(条件都是加热):
①2KNO3=2KNO2+O2↑
②2Cu(NO3)2=2CuO+4NO2↑+O2↑
③2AgNO3=2Ag+2NO2↑+O2↑
今有某固体可能由上述三种硝酸盐中的一种或几种组成.取适量该固体充分加热,得到一定量的气体,将这些气体通入水中,结果全部被吸收,没有剩余,回答:
(1)该固体是否可能只由一种盐组成?若可能,指出是哪种盐,若不可能,说明原因.______.
(2)若固体是混合物,指出它的可能组成(即物质的量之比),若没有这种组成,也请说明______.高三化学解答题中等难度题查看答案及解析
-
固体硝酸盐加热易分解且产物较复杂。已知KNO3、Cu(NO3)2、AgNO3三种硝酸盐的热分解反应方程式如下:
I.2KNO3
2KNO2+O2↑
II.2Cu(NO3) 2
2CuO+4NO2↑+O2↑
III.2AgNO3
2Ag+2NO2↑+O2↑
(1)某固体可能由KNO3、Cu(NO3)2、AgNO3三种硝酸盐中的一种或几种组成。取适量该固体充分加热,得到一定量气体。若该气体经水充分吸收后,剩余气体的体积在同温同压下为吸收前的1/6。 (忽略氧在水中的溶解)
①若该固体只是由一种盐组成,则该盐为________ 。
②若该固体是混合物,则该混合物的可能组成为________。
(2)某学习小组以Mg(NO3)2为研究对象,通过实验探究其热分解的产物,设计如下图所示的实验装置(图中加热、夹持仪器等均省略):
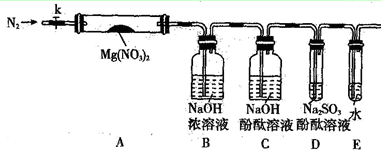
【实验步骤】
a.仪器连接后,放入固体试剂之前,关闭k,微热硬质玻璃管A。
b.称取Mg(NO3)2固体3.7g置于A中,先通入一段时间N2,再关闭k,用酒精灯加热硬质玻璃管A。
c.待样品完全分解,A 装置冷却至室温、称量,测得剩余固体的质量为1.0g 。
①步骤a的目的是________;
②依据已知的三个方程式,再根据剩余固体的质量写出Mg(NO3)2热分解方程式为:________。
③若A中固体为AgNO3,用以上实验装置进行实验时,D 中的现象为________,用离子方程式表示出现该现象的原因:_____________________________ 。
④从实验安全的角度判断该实验装置有无缺陷?若有,应如何改进?________。
高三化学填空题极难题查看答案及解析
-
某校化学兴趣小组的同学对硝酸盐的受热分解进行探究。他们设计了如下装置分别加热了Ca(NO3)2、Cu(NO3)2、AgNO3三种固体。(加热及夹持装置未画出)
(1)甲同学加热的是Ca(NO3)2。加热过程发现:装置②中产生 气泡,部分石蕊试液被压至装置③中;用带火星的木条检验②中的气体,木条复燃;分析装置①中剩余的固体得知,剩余固体中含有N元素,且显+3价。请写出Ca(NO3)2受热分解后生成产物的化学式:、________。
(2)乙同学加热的是Cu(NO3)2。加热过程发现:装置②中也有气泡产生,但在上升的过程中消失。石蕊试液逐渐变为红色,液体几乎不被压至装置③中。装置①中的固体逐渐变为黑色。请写出Cu(NO3)2受热分解的化学方程式:;
(3)丙同学加热的是AgNO3。加热过程发现:装置②中也有气泡产生,但在上升的过程中气泡部分消失,剩余的气体也能使带火星的木条复燃。石蕊试液也逐渐变为红色,有少量液体被压至装置③中。装置①中的固体逐渐变为黑色。丙同学据此写出了AgNO3受热分解可能的两种化学方程式:学科
(Ⅰ)4AgNO3 2Ag2O+4NO2↑+O2↑,
(Ⅱ)2AgNO3 2Ag+2NO2↑+O2↑。
Ⅰ、Ⅱ中正确的是________,并说明理由:。
请你设计一个简单的实验证明你的结论是正确的:________。
(4)由上述3个实验的结果,请你推测硝酸盐受热分解的规律:________。
(5)标况下如丙同学操作,称量ag硝酸银,受热完全分解后,读取量筒体积为bml,求硝酸银的分解率:____________(化简成整数比例关系,可不用化成小数)
高三化学填空题中等难度题查看答案及解析
-
(11) 某校化学兴趣小组的同学对硝酸盐的受热分解进行探究。他们设计了如下装置分别加热了Ca(NO3)2、Cu(NO3)2、AgNO3三种固体。(加热及夹持装置未画出)
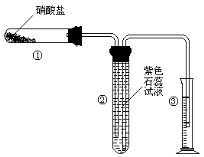
(1)甲同学加热的是Ca(NO3)2。加热过程发现:装置②中产生 气泡,部分石蕊试液被压至装置③中;用带火星的木条检验②中的气体,木条复燃;分析装置①中剩余的固体得知,剩余固体中含有N元素,且显+3价。请写出Ca(NO3)2受热分解后生成产物的化学式: 、 。
(2)乙同学加热的是Cu(NO3)2。加热过程发现:装置②中也有气泡产生,但在上升的过程中消失。石蕊试液逐渐变为红色,液体几乎不被压至装置③中。装置①中的固体逐渐变为黑色。请写出Cu(NO3)2受热分解的化学方程式: ;
(3)丙同学加热的是AgNO3。加热过程发现:装置②中也有气泡产生,但在上升的过程中气泡部分消失,剩余的气体也能使带火星的木条复燃。石蕊试液也逐渐变为红色,有少量液体被压至装置③中。装置①中的固体逐渐变为黑色。丙同学据此写出了AgNO3受热分解可能的两种化学方程式:
(Ⅰ)4AgNO3
2Ag2O+4NO2↑+O2↑ (Ⅱ)2AgNO3
2Ag+2NO2↑+O2↑。
Ⅰ、Ⅱ中正确的是 ,并说明理由: 。
请你设计一个简单的实验证明你的结论是正确的: 。
(4)由上述3个实验的结果,请你推测硝酸盐受热分解的规律: 。
(5)标况下如丙同学操作,称量ag硝酸银,受热完全分解后,读取量筒体积为bml,求硝酸银的分解率:____________(化简成整数比例关系,可不用化成小数)
高三化学填空题困难题查看答案及解析
-
为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究:
(查阅资料)2KNO3
2KNO2+O2↑ Fe(NO3)2
FexOy+NO2↑+O2↑
实验一:探究Fe(NO3)2热分解固体产物中铁元素的价态。该小组甲同学将分解后的固体产物溶于足量的稀H2SO4得到相应两份溶液,进行以下探究实验。
(1)(提纯猜想)
猜想一:铁元素只显+2价;
猜想二:铁元素_____________;
猜想三:铁元素既有+2价又有+3价。
(实验操作)①向一份溶液中滴入KSCN溶液;向另一份溶液中滴入酸性KMnO4稀溶液。
(2)(实验现象)实验①_____________________;实验②____________________。
(3)(实验结论)猜想二成立,则Fe(NO3)2分解的化学方程式是_________________。
实验二:
(4)探究Fe(NO3)2热分解气体产物的性质。小组乙同学进行料如下实验,请完成实验空缺部分内容。限选试剂和用品:浓H2SO4溶液、4mol/LNaOH溶液、0.1mol/LBaCl2溶液、带火星的木条、0.1mol/L酸性KMnO4溶液、蒸馏水。
实验步骤
预期现象和结论
步骤1:取少量Fe(NO3)2固体于试管中,加热分解。
____________________________________,说明分解产生的气体中含有NO2。
步骤2:将产生的气体依次通过盛有足量_________________、浓硫酸的洗气瓶,______________________在最后一个出口检验。
_____________________________________,说明分解产生的气体中含O2。
实验三:KNO3中混有Fe(NO3)2,为确定其中铁元素的含量,小组丙同学进行如下实验:①取混合物样品10g,充分加热分解;②将固体产物溶解、过滤,取沉淀进行洗涤、干燥,称得其质量为3.2g。则混合物中铁元素的质量分数为__________________。(保留三位有效数字,相对原子质量:Fe:56 O:16)
高三化学实验题中等难度题查看答案及解析
-
为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究:
【查阅资料】2KNO3
2KNO2+O2↑ Fe(NO3)2
FexOy+NO2↑+O2↑
实验一:探究Fe(NO3)2热分解固体产物中铁元素的价态。该小组甲同学将分解后的固体产物溶于足量的稀H2SO4得到相应两份溶液,进行以下探究实验。
(1)【提纯猜想】
猜想一:铁元素只显+2价;
猜想二:铁元素________;
猜想三:铁元素既有+2价又有+3价。
【实验操作】①向一份溶液中滴入KSCN溶液;向另一份溶液中滴入酸性KMnO4稀溶液。
(2)【实验现象】实验①________;实验②________。
(3)【实验结论】猜想二成立,则Fe(NO3)2分解的化学方程式是________。
实验二:
(4)探究Fe(NO3)2热分解气体产物的性质。小组乙同学进行料如下实验,请完成实验空缺部分内容。限选试剂和用品:浓H2SO4溶液、4mol/LNaOH溶液、0.1mol/LBaCl2溶液、带火星的木条、0.1mol/L酸性KMnO4溶液、蒸馏水。
实验步骤
预期现象和结论
步骤1:取少量Fe(NO3)2固体于试管中,加热分解。
________,说明分解产生的气体中含有NO2。
步骤2:将产生的气体依次通过盛有足量________
________、浓硫酸的洗气瓶,________
________在最后一个出口检验。
________,说明分解产生的气体中含O2。
实验三:KNO3中混有Fe(NO3)2,为确定其中铁元素的含量,小组丙同学进行如下实验:①取混合物样品10g,充分加热分解;②将固体产物溶解、过滤,取沉淀进行洗涤、干燥,称得其质量为3.2g。则混合物中铁元素的质量分数为________。(保留三位有效数字,相对原子质量:Fe-56 O-16)
高三化学实验题极难题查看答案及解析
-
硝酸盐受热分解的产物与硝酸盐的组成以及受热的温度等因素有关。
Ⅰ.一定条件下硝酸铵受热分解的化学反应方程式为:NH4NO3→HNO3+N2 +H2O(未配平)
(1)该反应中发生还原反应的过程是_______→________。
(2)反应中被氧化与被还原的氮原子数之比为__________;现有1mol NH4NO3分解,生成的氧化产物的物质的量是________mol。
Ⅱ.硝酸铵受撞击或高温发生爆炸的化学反应方程式为:m NH4NO3→n O2+p N2+q H2O
(3)下列关于该方程式中化学计量数的说法正确的是_________(选填字母编号)。
a.m=1 b.n=2 c.p=3 d.q=4
(4)若反应过程中共转移3.01×1023个电子,则反应可产生气体的体积为_____(标准状况)。
高三化学填空题中等难度题查看答案及解析
-
U常见化合价有+4和+6,硝酸铀酰[UO2(NO3)2]加热可发生如下分解反应:
UO2(NO3)2 —— UxOY + NO2↑+ O2↑(未配平),在600K时,将气体产物收集于试管中并倒扣于水中气体全部被吸收,水充满试管。则生成的铀的氧化物化学式是
A.UO3 B.UO2 C.2UO2·UO3 D.UO2·2UO3
高三化学选择题中等难度题查看答案及解析
-
U常见化合价有+4和+6,硝酸铀酰[UO2(NO3)2]加热可发生如下分解反应:UO2(NO3)2→UxOY+NO2↑+O2↑(未配平),在600K时,将气体产物收集于试管中并倒扣于水中气体全部被吸收,水充满试管.则生成的铀的氧化物化学式是( )
A.UO3 B.UO2 C.2UO2•UO3 D.UO2•2UO3
高三化学选择题中等难度题查看答案及解析
-
(11分)现有某金属硝酸盐化学式为M(NO3)2,为了探究其热分解产物,某化学小组开展探究性学习:
[查阅资料]金属活泼性不同,其硝酸盐分解产物不同。如,2KNO3
2KNO2+O2↑,
2Cu(NO3)2
2CuO+2NO2↑+O2↑,4AgNO3
4Ag+4NO2↑+O2↑
[提出猜想]猜想1 M(NO3)2
M(NO2)2+O2↑
猜想2 2 M(NO3)2
2MO+4NO2↑+O2↑
猜想3 。
[设计实验]为了探究上述猜想,设计如下实验装置:

实验步骤:①连接仪器;②检查装置气密性;③取一定量样品装于大试管,并重新连接好仪器;④加热;⑤……
(1)写出猜想3的化学方程式:________;
(2)测定气体体积应选择________(填A或B);不选另一个装置的理由是 ________;
(3)实验收集到一定量气体,为了检验收集气体的成分,其操作方法是 ________;
(4)在实验后的水里加入适量碳酸氢钠粉末,溶液中产生大量气体,说明________正确(填:猜想1.猜想2或猜想3);
(5) 该小组测得两组数据:①实验前样品质量为Wg,收集到气体体积为V L;
②实验前样品质量为Wg,完全分解后测得固体产物质量为m g;
请你选择其中一组数据,计算M的相对原子质量为 ________。
高三化学实验题简单题查看答案及解析