-
氮及其化合物在生产生活中用途广泛。请回答:
I.在微生物作用下,土壤中的NH4+最终被O2氧化为NO3-,该反应的离子方程式为________。
Ⅱ.氨气是重要的化工原料。已知:25℃时,NH3·H2O的电离常数kb=1.79×10-5,该温度下,1.79mol/LNH4Cl溶液的pH约为_____________。
Ⅲ.汽车在行驶过程中有如下反应发生:
ⅰ.N2(g)+O2(g) 2NO(g) △H=+180.7kJ/mol
2NO(g) △H=+180.7kJ/mol
ⅱ.2NO(g)+2CO(g) N2(g)+2CO2(g) △H=-746.5kJ/mol
N2(g)+2CO2(g) △H=-746.5kJ/mol
(1)能表示CO燃烧热的热化学方程式为__________________。
(2)反应ⅱ在________(填“较高”或“较低”)温度下能自发进行。
(3)T温度时,向10L恒容密闭容器中充入2molNO和2molCO发生反应ii,5min时达到平衡,测得0~5min内该反应速率v(N2)=0.016mol·L-1·min-1。
①T温度时,该反应的平衡常数K=____________________。
②平衡时容器内压强与起始时容器内压强之比为_________________。
(4)一定条件下,向起始容积为5L的恒压密闭容器充入1molN2和1molO2发生反应i。O2的平衡转化率(α)与温度(T)的关系如图1所示;正反应的平衡常数(K)与温度(T)的关系如图2所示。
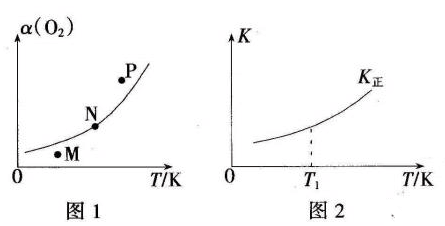
①图1中,M、N、P三点所对应的状态下,v(正)>v(逆)的是_______(填字母),理由为______。
②T1温度时,K正=1,则O2的平衡转化率为________(保留三位有效数字);在图2中画出逆反应平衡常数(K逆)与温度(T)的关系曲线。________
-
铁及其化合物在日常生活中用途比较广泛。
(1)高铁酸钠(Na2FeO4)是一种新型的绿色消毒剂和高容量电池材料。将Fe(NO3)3与NaClO混合后,在碱性条件下发生反应可制得高铁酸钠,该反应的离子方程式为_____________________________________。
(2)四氧化三铁(Fe3O4)常用作颜料、磁流体材料、催化剂和电子材料等。共沉淀法是目前制备纳米Fe3O4的重要方法之一,其流程如图所示:
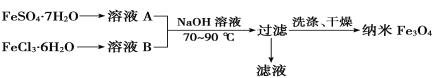
①为得到较纯净的纳米Fe3O4,FeSO4·7H2O与FeCl3·6H2O的物质的量之比最好为________。但实际操作时,却很难控制这一比例,原因是___________________________________________。
②在最佳投料比条件下,检验Fe3O4是否沉淀完全的实验操作是_________________________。
(3)绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。测定绿矾产品中FeSO4·7H2O含量的方法如下:
a.称取3.0 g绿矾产品,配制成250.00 mL溶液;
b.量取25.00 mL a中溶液于锥形瓶中;
c.用0.01000 mol·L-1酸性KMnO4溶液滴定至终点,消耗KMnO4溶液的平均体积为20.00 mL。滴定时发生反应的离子方程式为5Fe2++MnO4-+8H+===5Fe3++Mn2++4H2O。
①滴定终点的现象是_______________________________________________________________________。
②产品中FeSO4·7H2O的质量分数为________(小数点后保留1位数字)。
③若用上述方法测定的样品中FeSO4·7H2O的质量分数偏低(测定过程中产生的误差可忽略),可能的原因有________________________________________________________________________。
-
I.氮和氮的化合物在国防、工农业生产和生活中都有极其广泛的用途。请回答下列问题:
(1)亚硝酰氯(结构式为 )是有机合成中的重要试剂,它可由
)是有机合成中的重要试剂,它可由 和
和 在常温常压条件下反应制得,反应方程式为:
在常温常压条件下反应制得,反应方程式为: 。已知几种化学键的键能数据如表所示:
。已知几种化学键的键能数据如表所示:
则
 ________
________ 。
。
(2)在一个恒容密闭容器中充入 和
和 发生(1)中的反应,在温度分别为
发生(1)中的反应,在温度分别为 ℃、
℃、 ℃时测得
℃时测得 的物质的量(单位:mol)与时间的关系如下表所示:
的物质的量(单位:mol)与时间的关系如下表所示:
| t/min 温度 | 0 | 5 | 8 | 13 |
| 
| 2 | 1.5 | 1.3 | 1.0 |
| 
| 2 | 1.15 | 1.0 | 1.0 |
① ________
________ (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。
②温度为 时,起始时容器内的压强为
时,起始时容器内的压强为 ,则该反应的平衡常数
,则该反应的平衡常数 ________(用平衡分压代替平衡浓度计算,分压
________(用平衡分压代替平衡浓度计算,分压 总压
总压 物质的量分数)(化为最简式)。
物质的量分数)(化为最简式)。
(3)近年来,地下水中的氮污染已成为世界性的环境问题。在金属 、
、 和依(
和依( )的催化作用下,
)的催化作用下, 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),其工作原理如图所示。
),其工作原理如图所示。
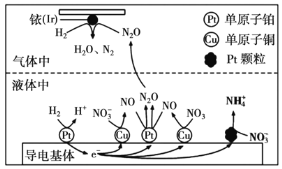
① 表面发生反应的化学方程式为:________。
表面发生反应的化学方程式为:________。
②若导电基体上的 颗粒增多,造成的后果是________。
颗粒增多,造成的后果是________。
Ⅱ.利用电化学原理,将 、
、 和熔融
和熔融 制成燃料电池,模拟工业电解法精炼银,装置如下图所示。
制成燃料电池,模拟工业电解法精炼银,装置如下图所示。
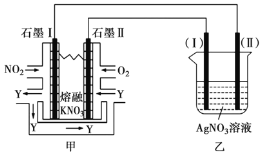
(4)①甲池工作时, 转变成绿色硝化剂
转变成绿色硝化剂 ,可循环使用,则石墨Ⅱ附近发生的电极反应方程式为________。
,可循环使用,则石墨Ⅱ附近发生的电极反应方程式为________。
②若用10A的电流电解50min后,乙中阴极得到 ,则该电解池的电解效率为________%。(保留小数点后一位。通过一定电量时阴极上实际沉积的金属质量与通过相同电量时理论上应沉积的金属质量之比叫电解效率。法拉第常数为
,则该电解池的电解效率为________%。(保留小数点后一位。通过一定电量时阴极上实际沉积的金属质量与通过相同电量时理论上应沉积的金属质量之比叫电解效率。法拉第常数为 )
)
-
硫及其化合物在生产生活中应用广泛。回答下列问题:
(1)铁铵矾是一种化学物质,分子式是 NH4Fe(SO4)2·12H2O,其溶于水后,溶液中的离子浓度大小关系为__________________。
(2)已知某溶液中含有 CO32-、SO42-等离子,取一定量的该溶液,向其中滴加BaCl2溶液,当 CO32-开始沉 淀时,溶液中c(CO32-)/c(SO42-)为_______________。(已知 Ksp(BaSO4 )=1.0×10-10 ,Ksp(BaCO3)=2.5×10-9 )
(3)已知:S2Cl2(l)+Cl2(g)=2SCl2(l) ΔH=-50.2kJ·mol-1 。断裂 1molCl-Cl键、1molS-S键分别需要吸收 243kJ、268kJ 的能量,则断裂 1mol S-Cl键需要吸收的能量为____kJ。
(4)用 NaOH 溶液吸收烟气中的 SO2,将所得的 Na2SO3 溶液进行电解,可以制备H2SO4,其原理如下图所示(电极材料为石墨)。

阳极的电极反应式为______________________;其中可循环使用的物质是________。
-
硫及其化合物在生产生活中应用广泛。回答下列问题:
(1)铁铵矾是一种化学物质,分子式是NH4Fe(SO4)2·12H2O,其溶于水后,溶液中的离子浓度大小关系为_____________________。
(2)已知某溶液中含有CO32-、SO42-等离子,取一定量的该溶液,向其中滴加BaCl2溶液,当CO32-开始沉淀时,溶液中 =_____。(已知Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=2.5×10-9)
=_____。(已知Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=2.5×10-9)
(3)已知:S2Cl2(l)+Cl2(g)=2SCl2(l) ΔH=-50.2 kJ·mol-1。断裂1mol Cl-Cl键、1mol S-S键分别需要吸收243kJ、268kJ的能量,则断裂1mol S-Cl键需要吸收的能量为_____________kJ。
(4)某容积不变的密闭容器中发生如下反应:2SO2(g)+O2(g)  2SO3(g) △H=-197 kJ·mol-1。
2SO3(g) △H=-197 kJ·mol-1。
①下列能说明反应达到平衡状态的是 ________________
a.体系压强保持不变 b.混合气体的密度保持不变
c.SO3和O2的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol SO2
②向同温、同体积的两个密闭容器中分别充入气体:(甲)2 mol SO2 和1 mol O2;(乙) 1 mol SO2 和0.5 mol O2 ;恒温、恒容下反应达平衡时,两个容器内的压强大小关系为____(用p甲、p乙表示)。
(5)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可以制备H2SO4,其原理如下图所示(电极材料为石墨)。

阳极的电极反应式为___________________________________。
-
氮及其化合物在生活、生产、科研中有广泛用途。
(1)己知反应 I : 2NH3(g) +CO2(g)=NH2CO2NH4(s) △H=-159.5kJ/mol
反应Ⅱ:NH2CO2NH4(s) =CO(NH2)2 (s)+ H2O(g) △H=+116.5 kJ/mol
反应Ⅲ:H2O(l) = H2O(g) △H=+44.0 kJ/mol
则工业上以二氧化碳、氨为原料合成化肥尿素和液态水的热化学方程式为________________________。(2)用NH3催化还原NxOy可以消除氮氧化物的污染。如有反应4NH3(g)+6NO(g)  5N2(g)+6H2O(l) △H<0,相同条件下在2 L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。
5N2(g)+6H2O(l) △H<0,相同条件下在2 L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。

①0~4分钟在A催化剂作用下,反应速率υ(N2)=______。
②下列说法不正确的是____________
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea (C)
B.使用催化剂A达平衡时,N2最终产率更大
C.单位时间内H-O与N-H键断裂的数目相等时,说明反应已经达到平衡
D.若在恒容绝热的密闭容器中发生反应,当平衡常数不变时,说明反应已经达到平衡
(3)用焦炭还原NO的反应为:2NO(g)+C(s) N2(g)+CO2(g),向容积均为1L的甲、乙、 丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、 丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
| t/min | 0 | 40 | 80 | 120 | 160 |
| n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)(乙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
| n(NO)(丙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
①该反应为_____________________(填“放热”或“吸热”)反应。
②在上述条件下乙容器达到平衡时,NO的转化率=_____________________。
(4)①银氨溶液中存在平衡:Ag+(aq)+2NH3(aq) Ag(NH3)2+(aq),该反应平衡常数的表达式为K稳=___________________。
Ag(NH3)2+(aq),该反应平衡常数的表达式为K稳=___________________。
②查阅资料可知:常温下,K稳[Ag(NH3)2+]=1.10×107,Ksp[AgCl]=1.76×10-10。
计算得到可逆反应AgCl(s)+2NH3(aq) Ag(NH3)2+(aq)+Cl-(aq)的化学平衡常数K=_____(保留4位有效数字)。
Ag(NH3)2+(aq)+Cl-(aq)的化学平衡常数K=_____(保留4位有效数字)。
-
氮及其化合物在生活、生产、科研中有广泛用途。
(1)己知反应 I : 2NH3(g) +CO2(g)=NH2CO2NH4(s) △H=-159.5kJ/mol
反应Ⅱ:NH2CO2NH4(s) =CO(NH2)2 (s)+ H2O(g) △H=+116.5 kJ/mol
反应Ⅲ:H2O(l) = H2O(g) △H=+44.0 kJ/mol
则工业上以二氧化碳、氨为原料合成化肥尿素和液态水的热化学方程式为________________________。(2)用NH3催化还原NxOy可以消除氮氧化物的污染。如有反应4NH3(g)+6NO(g)  5N2(g)+6H2O(l) △H<0,相同条件下在2 L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。
5N2(g)+6H2O(l) △H<0,相同条件下在2 L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示。

①0~4分钟在A催化剂作用下,反应速率υ(N2)=______。
②下列说法不正确的是____________
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea (C)
B.使用催化剂A达平衡时,N2最终产率更大
C.单位时间内H-O与N-H键断裂的数目相等时,说明反应已经达到平衡
D.若在恒容绝热的密闭容器中发生反应,当平衡常数不变时,说明反应已经达到平衡
(3)用焦炭还原NO的反应为:2NO(g)+C(s) N2(g)+CO2(g),向容积均为1L的甲、乙、 丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、 丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
| t/min | 0 | 40 | 80 | 120 | 160 |
| n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)(乙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
| n(NO)(丙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
①该反应为_____________________(填“放热”或“吸热”)反应。
②在上述条件下乙容器达到平衡时,NO的转化率=_____________________。
(4)①银氨溶液中存在平衡:Ag+(aq)+2NH3(aq) Ag(NH3)2+(aq),该反应平衡常数的表达式为K稳=___________________。
Ag(NH3)2+(aq),该反应平衡常数的表达式为K稳=___________________。
②查阅资料可知:常温下,K稳[Ag(NH3)2+]=1.10×107,Ksp[AgCl]=1.76×10-10。
计算得到可逆反应AgCl(s)+2NH3(aq) Ag(NH3)2+(aq)+Cl-(aq)的化学平衡常数K=_____(保留4位有效数字)。
Ag(NH3)2+(aq)+Cl-(aq)的化学平衡常数K=_____(保留4位有效数字)。
-
氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如图。
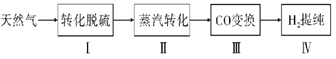
请回答下列问题:
I.转化脱硫:将天然气压入吸收塔,30℃时,在T·F菌作用下,酸性环境中脱硫过程示意图如下。
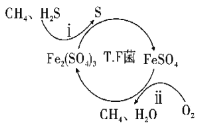
(1)过程i的离子反应方程式为__。
(2)已知:
①Fe3+在pH=1.9时开始沉淀pH=3.2时沉淀完全。
②30℃时,在T·F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如表。
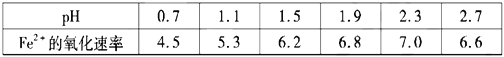
下列说法正确的是___
A.在转化脱硫中,最佳的pH范围是1.5<pH<1.9
B.在转化脱硫中需要不断补充Fe2(SO4)3
C.在转化脱硫中是O2间接地把H2S氧化为S
D.在转化脱硫中CH4作为还原剂被氧化
Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合如图回答问题。

(3)①该过程的热化学方程式是__。
②比较压强p1和p2的大小关系:p1__p2(选填“<”、“>”或“=”)。
Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.提纯:将CO2和H2分离得到H2的过程示意图如图。
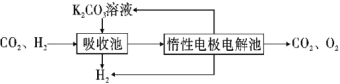
(4)吸收池中发生反应的离子方程式是__。
-
铁单质及其化合物在生活、生产中应用广泛。请回答:
(1)钢铁在空气中发生吸氧腐蚀时,正极的电极反应是________。
(2)由于氧化性Fe3+>Cu2+氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是________。
(3)硫酸铁可作絮凝剂,常用于净水,其原理是________ (用离子方程式表示)。在使用时发现硫酸铁不能将酸性废水中的悬浮物沉降除去,其原因是________。
(4)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4十4CO 3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是________。
3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是________。
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是________(填字母)。
陈述Ⅰ 陈述Ⅱ 判断
A 铁是地壳中含量最高的金属元素 铁是人类最早使用的金属材料 Ⅰ对;Ⅱ对;有
B 常温下铁与稀硫酸反应生成氢气 一定温度下氢气能还原氧化铁得到铁 Ⅰ对;Ⅱ对;无
C 铁属于过渡元素 铁和铁的某些化合物可用作催化剂 Ⅰ错;Ⅱ对;无
D 在空气中铁表面形成致密氧化膜 铁不能与氧气反应 Ⅰ对;Ⅱ对;有
-
含氯消毒剂在生产生活中有着广泛的用途。完成下列填空:
(1)工业上将氯气溶于一定浓度的氢氧化钠溶于可制得“84消毒液”,反应的离子方程式为_________。
(2)“84消毒液”(主要成分是NaClO)不能和洁厕剂(主要成分是浓盐酸)混用。混用时反应的化学方程式是_______________________________;“84消毒液”不能对钢铁制品进行消毒,原因是____________。
(3)工业常用石灰乳和氯气反应制取漂粉精,其主要设备是氯化塔,将含有3%-6%水分的石灰乳从塔顶部喷洒而入,氯气从塔的最底层通入。这样加料的目的是__________;处理从氯化塔中逸出气体的方法是_____。
(4)二氧化氯(ClO2)是一种黄绿色易溶于水的气体。工业上常用NaClO3和Na2SO3溶液混合并加入H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为_________。
(5)在用二氧化氯进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+生成ClO2-和MnO2的离子方程式为___________________________。
2NO(g) △H=+180.7kJ/mol
N2(g)+2CO2(g) △H=-746.5kJ/mol












